Nieuwe publicaties
Eiwit verantwoordelijk voor genetische ontstekingsziekte geïdentificeerd
Laatst beoordeeld: 02.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Een team van onderzoekers onder leiding van dr. Hirotsugu Oda van het CECAD Cluster of Excellence for Aging Research aan de Universiteit van Keulen heeft de rol ontdekt die een bepaald eiwitcomplex speelt bij bepaalde vormen van immuundysregulatie. Deze resultaten kunnen leiden tot de ontwikkeling van nieuwe therapeutische benaderingen gericht op het verminderen van auto-inflatie en het "herstellen" van het immuunsysteem van patiënten die lijden aan een genetische disfunctie van dit eiwitcomplex.
Het onderzoek, "Biallelic human SHARPIN loss of function induces autoinflammation and immunodeficiency", werd gepubliceerd in het tijdschrift Nature Immunology.
Het lineaire ubiquitine-assemblerende complex (LUBAC), bestaande uit de eiwitten HOIP, HOIL-1 en SHARPIN, wordt al lang erkend vanwege zijn cruciale rol bij het handhaven van de immuunhomeostase. Eerdere studies bij muizen hebben de ernstige gevolgen van SHARPIN-verlies aangetoond, wat leidt tot ernstige dermatitis als gevolg van overmatige celdood in de huid. De specifieke gezondheidsgevolgen van SHARPIN-deficiëntie bij mensen zijn echter nog onduidelijk.
Het onderzoeksteam rapporteerde voor het eerst twee personen met een SHARPIN-tekort die symptomen van auto-inflatie en immuundeficiëntie vertonen, maar onverwachts geen dermatologische problemen vertonen zoals bij muizen.
Na verder onderzoek bleek dat deze personen een verminderde canonieke NF-κB-respons hadden, een belangrijk immuunreactiepad. Ze hadden ook een verhoogde vatbaarheid voor celdood veroorzaakt door leden van de tumornecrosefactor (TNF)-superfamilie. Behandeling van één SHARPIN-deficiënte patiënt met anti-TNF-therapie, die specifiek TNF-geïnduceerde celdood remt, resulteerde in volledige remissie van de auto-inflatie op cellulair niveau en in de klinische presentatie.
De studie toont aan dat overmatige en ongecontroleerde celdood een cruciale rol speelt bij genetische ontstekingsziekten bij de mens. Oda's team voegde SHARPIN-deficiëntie toe als een nieuw lid van een groep genetische ontstekingsziekten bij de mens die zij "aangeboren afwijkingen van celdood" noemen.
Bescherming tegen immuundysregulatie. Het onderzoek werd gestart in het laboratorium van Dr. Dan Kastner van de National Institutes of Health (NIH) in de Verenigde Staten. Wetenschappers daar hadden de gelegenheid om een patiënt te observeren met een kindertijd met onverklaarde episodes van koorts, artritis, colitis en immuundeficiëntie.
Na het verkrijgen van informed consent voerden ze exoomsequentieanalyse uit op de patiënt en zijn familieleden en ontdekten dat de patiënt een verwoestende genetische variant in het SHARPIN-gen had, die leidde tot onmeetbare niveaus van het SHARPIN-eiwit. Ze ontdekten ook dat de cellen van de patiënt een verhoogde neiging vertoonden om af te sterven, zowel in gekweekte cellen als in biopten van de patiënt.
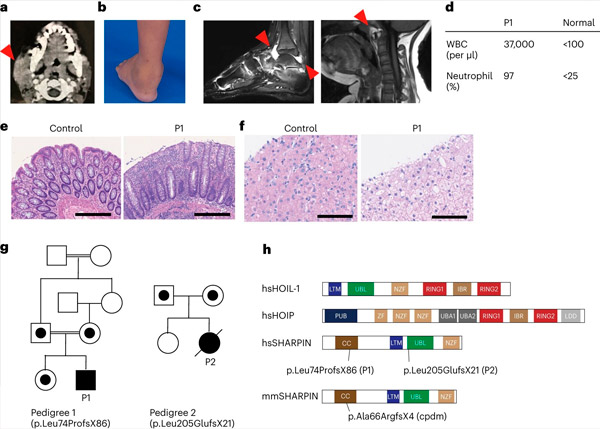
Een tekort aan SHARPIN bij mensen veroorzaakt auto-ontsteking en leverglycogeenose. Bron: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
Het team ontdekte ook dat de ontwikkeling van lymfoïde kiemcentra – gespecialiseerde microstructuren in de neusamandelen die cruciaal zijn voor de rijping van de B-cellen in ons immuunsysteem en daarmee voor de productie van antilichamen – aanzienlijk werd verminderd door een verhoogde B-celsterfte. Deze bevindingen verklaren de immunodeficiëntie van de patiënten en benadrukken de belangrijke rol van LUBAC bij het handhaven van de immuunhomeostase bij mensen.
"Onze studie benadrukt het cruciale belang van LUBAC bij de bescherming tegen immuundysregulatie. Door de moleculaire mechanismen die ten grondslag liggen aan LUBAC-deficiëntie te verhelderen, effenen we de weg voor nieuwe therapeutische strategieën gericht op het herstellen van de immuunhomeostase", aldus Oda, hoofdauteur van de studie.
Hij voegde eraan toe: "Een van de patiënten met SHARPIN-deficiëntie zat al jaren in een rolstoel voordat we hem voor het eerst zagen. Zijn enkels waren ontstoken en lopen was te pijnlijk. Dankzij de genetische diagnose konden we de juiste moleculaire route bepalen die aan zijn aandoeningen ten grondslag ligt."
Sinds de patiënt anti-TNF-therapie is gaan volgen, is hij al bijna zeven jaar symptoomvrij. "Als clinicus en wetenschapper ben ik blij dat ik met ons onderzoek een positieve impact kan hebben op het leven van een patiënt", concludeerde Oda.
