Oorzaken en pathogenese van prostaatadenoom
Last reviewed: 01.06.2018

We hanteren strikte richtlijnen voor bronnen en linken alleen naar gerenommeerde medische websites, academische onderzoeksinstellingen en, waar mogelijk, medisch peer-reviewed onderzoek. De nummers tussen haakjes ([1], [2], enz.) zijn klikbare links naar deze onderzoeken.
Als u van mening bent dat onze content onjuist, verouderd of anderszins twijfelachtig is, selecteer deze dan en druk op Ctrl + Enter.
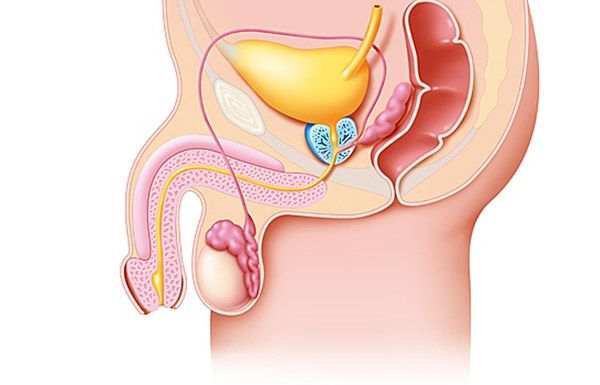
Het begrijpen van de pathogenese van prostaatadenoom (prostaatklier) is onmogelijk zonder rekening te houden met moderne gegevens over de anatomie en morfologie ervan. De moderne theorie over de ontwikkeling van prostaatadenoom (prostaatklier) is gebaseerd op het zonale concept van de prostaatstructuur, waarbij in de prostaatklier verschillende gebieden worden onderscheiden die verschillen in de histologische en functionele kenmerken van de cellulaire elementen waaruit ze bestaan. Dit zijn de perifere, centrale en transitionele (transiënte) zones, evenals het gebied van het voorste fibromusculaire stroma en het preprostatische segment.
Ter hoogte van de zaadbuis openen de uitstroomopeningen van de zaadleider zich. De wand van het proximale deel van de urethra bestaat uit longitudinale gladde spiervezels. De preprostatische (genitale) sluitspier, gevormd door een dikke laag gladde spiervezels, omsluit het proximale deel van de urethra vanaf de blaashals tot aan de bovenkant van de zaadbuis en voorkomt retrograde ejaculatie.
Histologisch onderzoek heeft aangetoond dat de groei van prostaatadenomen (prostaatklieren) begint in de centrale en de overgangszones van de prostaat. De overgangszone van de prostaat bestaat uit twee afzonderlijke klieren die zich direct achter de inwendige sluitspier van de blaas bevinden. De uitscheidingskanalen van deze zone bevinden zich aan de laterale wand van de urethra, vlakbij de zaadbuis. De proximale overgangszone bevat de klieren van de periurethrale zone; deze grenzen aan de inwendige sluitspier van de blaas en liggen parallel aan de as van de urethra. Adenomateuze klieren kunnen zich zowel in de overgangszone als in de para-urethrale zone ontwikkelen. Naast nodulaire hyperplasie heeft de overgangszone de neiging om met de leeftijd te groeien.
De prostaatklier speelt een belangrijke rol bij de ontwikkeling van symptomen van prostaatkanker (adenoom). Bij honden is de prostaatklier dan ook slecht ontwikkeld en zelfs bij ernstige hyperplasie ontwikkelen zich zelden symptomen van de ziekte. De prostaatklier brengt de druk van het vergrote prostaatweefsel over op de urethra, waardoor de weerstand in de urethra toeneemt.
Prostaatadenoom (prostaatklier): pathofysiologie
Het prostaatgedeelte van de urethra is verlengd en vervormd tot 4-6 cm of meer, voornamelijk als gevolg van het gebied van de achterwand dat zich boven de zaadbuis bevindt. De blaashals is opgetild en vervormd, het lumen wordt spleetvormig. Hierdoor neemt de natuurlijke kromming van de urethra toe, en bij een ongelijkmatige ontwikkeling van de laterale lobben wordt de urethra ook in dwarsrichting gebogen, waardoor deze een zigzagvormig uiterlijk kan krijgen. Gapen van het lumen van de blaashals als gevolg van het falen van het urethra-sfinctermechanisme tijdens de detrusorcompensatie wordt klinisch gemanifesteerd door urine-incontinentie.
Ook de urineblaas ondergaat ingrijpende veranderingen. De reactie op de ontwikkeling van een obstructie verloopt in drie fasen: prikkelbaarheid, compensatie en decompensatie. In de eerste fase van infravesicale obstructie reageert de urineblaas met toenemende detrusorcontracties, waardoor tijdelijk het functionele evenwicht en volledige urinelozing mogelijk is. Verdere ontwikkeling van de obstructie leidt tot compensatoire hypertrofie van de urineblaaswand, die een dikte van 2-3 cm kan bereiken. In dit geval kan de wand een trabeculair uiterlijk krijgen door verdikte en uitpuilende spierbundels.
De eerste fase van de trabeculaire ontwikkeling wordt morfologisch gekenmerkt door hypertrofie van gladde spiercellen. De voortgang van dit proces leidt tot scheiding van gehypertrofieerde spierelementen en opvulling van de ruimtes ertussen met bindweefsel. Tussen de trabeculae ontstaan holtes, zogenaamde valse divertikels, waarvan de wanden geleidelijk dunner worden door de toegenomen intravesicale druk. Dergelijke divertikels zijn vaak talrijk en bereiken soms aanzienlijke afmetingen.
De elastische eigenschappen van de detrusor worden bepaald door de aanwezigheid van collageen, dat in het gladde spierweefsel 52% van de totale hoeveelheid eiwit uitmaakt. Naarmate het compensatievermogen uitgeput raakt en de atrofie toeneemt, worden de blaaswanden dunner. De detrusor verliest zijn vermogen om samen te trekken en te rekken, waardoor de capaciteit van de blaas aanzienlijk toeneemt tot 1 liter of meer. Gelijktijdige ontstekings- en trofische veranderingen leiden tot een uitgesproken sclerose van de spierlaag van de blaaswand en een afname van het collageengehalte. Het gehalte aan bindweefsel wordt gelijk aan of groter dan het gehalte aan spierelementen.
De mate van herstel van de normale structuur van de blaaswand hangt af van de duur van de obstructie van de urineafvoer. Als gevolg van langdurige obstructie ontstaan onomkeerbare morfologische veranderingen, die leiden tot uitgesproken functionele stoornissen van de blaas en zelfs met chirurgische behandeling niet kunnen worden verholpen. Ernstige infravesicale obstructie leidt tot verhoogde druk in de blaas, verminderde urineafvoer vanuit de nieren en de ontwikkeling van vesico-ureterale en renale reflux, evenals pyelonefritis. De urineleiders verwijden, verlengen, worden kronkelig, ureterohydronefrose en chronisch nierfalen ontstaan. De pathogenese van veranderingen in de nieren en de bovenste urinewegen bij patiënten met prostaatkanker is complex en hangt af van vele factoren: leeftijdsgebonden veranderingen, bijkomende ziekten die hun functionele capaciteit beïnvloeden, de ontwikkeling van obstructieve uropathie.
In het eerste stadium van obstructieve uropathie voorkomen het behoud van het fornica-apparaat van de calyces en de integriteit van het epitheel van de verzamelbuizen van de papillen het optreden van reflux in het nierbekken en de penetratie van de infectie in het nierparenchym op een opstijgende manier. Naarmate ureterohydronefrose zich ontwikkelt, treedt structurele vervorming van de nierkelkgewelven op, wat gunstige omstandigheden creëert voor het optreden van reflux in het nierbekken-tubuli, en vervolgens in het nierbekken-veneuze en renale reflux in het nierbekken-lymfatische reflux.
Als gevolg van verhoogde intrapelvische druk en nierbekken-nierreflux wordt de renale hemodynamiek aanzienlijk verstoord, gevolgd door de ontwikkeling van structurele veranderingen in de intraorganische arteriën in de vorm van hun obliteratie en diffuse stenose. Hemodynamische stoornissen leiden tot ernstige metabole verschuivingen en ernstige ischemie van het nierweefsel. Obstructieve uropathie resulteert in een progressieve verslechtering van alle indicatoren van de functionele toestand van de nieren. Een karakteristiek kenmerk van dit proces is een vroege aantasting van het concentrerend vermogen van de nieren, die zich voornamelijk manifesteert door een sterke afname van de reabsorptie van Na-ionen en een toename van hun uitscheiding met de urine. Verminderde nierfunctie bij stadium I prostaatkankeradenoom wordt waargenomen bij 18% van de patiënten. Bij stadium II compliceert chronisch nierfalen het beloop van de ziekte bij 74%, waarbij 11% van hen een terminaal stadium heeft. Chronisch nierfalen wordt vastgesteld bij alle patiënten met prostaatkanker stadium III, waarbij het intermitterende stadium bij 63% van de onderzochte patiënten wordt waargenomen en het terminale stadium bij 25%.
Urineweginfecties spelen een fundamentele rol in de pathogenese van nieraandoeningen bij prostaatkanker en compliceren het beloop van de ziekte aanzienlijk. Pyelonefritis en nierfalen zijn verantwoordelijk voor tot 40% van de doodsoorzaken bij patiënten met prostaatkanker. Chronische pyelonefritis bij patiënten met prostaatkanker wordt in 50-90% van de gevallen waargenomen.
Ontsteking van bacteriële oorsprong treedt voornamelijk op in het interstitiële peritubulaire weefsel. In de pathogenese van secundaire pyelonefritis bij prostaatkankeradenoom spelen urostase en de ontwikkeling van vesicoureterale en reflux in het nierbekken de hoofdrol. De infectie dringt de nier binnen via de blaas. Urineweginfecties gaan gepaard met de meeste gevallen van prostaatkankeradenoom. Chronische cystitis werd waargenomen bij 57-61% van de poliklinische patiënten en 85-92% van de opgenomen patiënten. In dit opzicht kan de pathogenese van chronische pyelonefritis bij patiënten met prostaatkankeradenoom als volgt worden weergegeven: infravesicale obstructie → blaasdisfunctie → cystitis → insufficiëntie van de vesicoureterale verbindingen → vesicoureterale reflux → chronische pyelonefritis.
De aanwezigheid van een gelijktijdig ontstekingsproces in de prostaat speelt een grote rol bij de vorming van het klinische beeld bij prostaatadenoom. De frequentie van chronische prostatitis bij prostaatadenoom bedraagt volgens laboratorium-, chirurgische en autopsiegegevens respectievelijk 73%, 55,5% en 70%. Veneuze stase, compressie van de afvoergangen van de acini door hyperplastisch weefsel van de klier en het oedeem ervan zijn voorwaarden voor het ontstaan van chronische ontsteking. Morfologisch onderzoek van het chirurgische materiaal toonde aan dat het ontstekingsproces in de meeste gevallen gelokaliseerd was in de periferie van de klier. Gelijktijdige chronische prostatitis kan zich klinisch manifesteren als dysurie, wat een differentiële diagnose vereist met urinewegaandoeningen die worden veroorzaakt door het prostaatadenoom zelf. De aanwezigheid ervan leidt ook tot een toename van het aantal vroege en late postoperatieve complicaties, in verband waarmee maatregelen nodig zijn om chronische prostatitis te identificeren en te desinfecteren tijdens de conservatieve behandeling of ter voorbereiding op een operatie.
Blaasstenen in adenomen worden secundair gevormd als gevolg van blaasledigingsstoornissen. Ze worden bij 11,7-12,8% van de patiënten aangetroffen. Ze hebben meestal een regelmatige ronde vorm, kunnen enkelvoudig of meervoudig voorkomen en zijn qua chemische samenstelling uraten of fosfaten. Nierstenen gaan in 3,6-6,0% van de gevallen gepaard met prostaatadenomen.
Een veel voorkomende complicatie van prostaatkanker is volledige acute urineretentie, die zich in elk stadium van de ziekte kan ontwikkelen. In sommige gevallen is dit het culminatiepunt van het obstructieve proces in combinatie met decompensatie van het contractiele vermogen van de detrusor, terwijl het zich in andere gevallen plotseling ontwikkelt tegen de achtergrond van matige symptomen van urineerproblemen. Vaak is dit de eerste klinische manifestatie van prostaatkanker. Volgens de literatuur wordt deze complicatie waargenomen bij 10-50% van de patiënten, meestal in stadium II van de ziekte. Uitlokkende factoren voor de ontwikkeling van deze complicatie kunnen een schending van het dieet (alcoholgebruik, specerijen), hypothermie, constipatie, voortijdige lediging van de blaas, stress en het gebruik van bepaalde medicijnen (anticholinergica, kalmeringsmiddelen, antidepressiva, diuretica) zijn.
De belangrijkste factoren bij de ontwikkeling van acute urineretentie zijn de groei van hyperplastisch weefsel, functionele veranderingen in de tonus van de nek en de spieren van de blaas en een verminderde microcirculatie van de bekkenorganen met de ontwikkeling van prostaatoedeem.
In het beginstadium van acute urineretentie leidt een verhoogde contractiele activiteit van de detrusor tot een toename van de intravesicale druk. In de daaropvolgende stadia, door het uitrekken van de blaaswand en een afname van het contractievermogen, daalt de intravesicale druk.
