Medisch expert van het artikel
Nieuwe publicaties
Fusobacteriën: vriend of vijand?
Laatst beoordeeld: 06.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
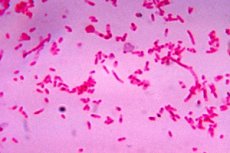
Volgens de in de microbiologie aanvaarde classificatie zijn fusobacteriën prokaryoten en gramnegatieve anaërobe bacteriën die in het lichaam van mensen en andere zoogdieren leven en deel uitmaken van de constante normale microbiocenose of microflora. Hun familie - Fusobacteriaceae - telt meer dan anderhalf dozijn soorten.
Morfologie van Fusobacteriën en kenmerken van hun metabolisme
Fusobacteriën hebben een eencellige, spoelvormige structuur (fusus in het Latijn) dankzij de puntige uiteinden aan beide zijden. De staafjes kunnen dik en dun, recht en gebogen zijn, en soms ook draadvormig. De lengte van deze bacteriën varieert van 0,0005 tot 0,008 mm en ze hebben geen bewegingsorganen, hoewel sommige bronnen beweren dat ze peritricheuze (over het gehele oppervlak verspreide) flagellen hebben.
Bacteriologen merken op dat deze micro-organismen geen sporen vormen, dat wil zeggen dat ze zich bij verslechtering van de leefomstandigheden niet kunnen ontwikkelen tot cellen met een dicht membraan. Fusobacteriën planten zich voort door mitotische splitsing van één cel in tweeën met horizontale overdracht van genen die geconcentreerd zijn in de nucleoid.
De morfologie van fusobacteriën bepaalt mede de leefomgeving van hun kolonies: de slijmvliezen van de mondholte, de luchtwegen, het urogenitale gebied en het onderste deel van het spijsverteringskanaal - de dikke darm. Hun aanwezigheid in het bloed is niet vastgesteld, maar fusobacteriën hebben dit niet nodig, omdat ze voedingsstoffen ontvangen via de fermentatie van glucose, sucrose, maltose en enkele aminozuren.
De basis van het metabolisme van deze micro-organismen is dus het biochemische proces van anaërobe (zonder zuurstof) dissimilatie van koolhydraten onder invloed van enzymen. De metabolieten zijn laagmoleculair boterzuur (butaanzuur), koolstofdioxide en waterstof. Om energie te verkrijgen, hebben bacteriën waterstof nodig. De ionen hiervan worden opgenomen door het oppervlakte-eiwit van fusobacteriën adhesine A (FadA) en vervolgens de cel in getransporteerd.
Overigens is boterzuur zeer belangrijk voor het behoud van de intestinale homeostase (absorptie van water en elektrolyten) en voor de regeneratie van slijmachtige epitheelcellen; artsen hebben een verband vastgesteld tussen een tekort aan dit zuur in de darm en de ontwikkeling van lokale ontstekingsziekten (bijvoorbeeld colitis ulcerosa). Naast fusobacteriën wordt boterzuur ook geproduceerd door bacteriën van het geslacht Clostridium.
Over de voorwaardelijke pathogeniciteit van fusobacteriën
Fusobacteriën worden, net als de meeste gramnegatieve anaerobe bacteriën, door bacteriologen beschouwd als opportunistische pathogenen, maar er zijn stammen waarvan wetenschappers de verhoogde pathogeniciteit niet langer in twijfel trekken. Dit geldt met name voor Fusobacterium necrophorum, dat in de mondholte en darmen leeft, en Fusobacterium nucleatum, dat tandplak als leefgebied heeft gekozen.
Hoe werkt hun pathogenische mechanisme? Het buitenste oppervlak van het cytoplasmatisch membraan van fusobacteriën bestaat uit gepolymeriseerde vetten, eiwitten en koolhydraten in de vorm van lipopolysacchariden, wat bacteriële toxische stoffen (endotoxinen) zijn en tegelijkertijd antigenen. Dat wil zeggen dat deze verbindingen een immuunreactie van het lichaam en een ontstekingsreactie veroorzaken zonder duidelijke exogene (externe) invloed op individuele systemen en organen.
Er wordt aangenomen dat de pathogeniciteit van sommige bacteriën van de familie Fusobacteriaceae zich alleen manifesteert bij een verzwakte immuniteit. Er moet echter rekening mee worden gehouden dat ze zeer agressief kunnen zijn, aangezien fusobacteriën fosfolipase A produceren - een enzym dat lipiden van celmembranen afbreekt en bacteriën toegang geeft tot cellen van alle weefsels. Micro-organismen gebruiken dit enzym echter doorgaans niet "alleen", maar in de aanwezigheid van pathogene micro-organismen neemt de activiteit aanzienlijk toe. Wanneer het slijmvlies beschadigd raakt door streptokokken of stafylokokken, maken fusobacteriën gebruik van de gelegenheid om dieper door te dringen en necrotische weefselontsteking te veroorzaken. Het meest illustratieve voorbeeld van een dergelijk synergetisch effect is gangreneuze faryngitis (of Simanovsky-Plaut-Vincent-angina), die ontstaat als gevolg van een infectie van het slijmvlies door gramnegatieve bacteriën Spirochaetales Borrelia vincentii, Prevotella intermedia en Fusobacterium nucleatum.
Welke ziekten worden veroorzaakt door fusobacteriën?
Laten we nu eens een aantal ziekten opnoemen die door fusobacteriën worden veroorzaakt, of preciezer gezegd, pathologieën die zich ontwikkelen met hun meer dan actieve deelname. Artsen rekenen onder andere de volgende ziekten:
- pulpitis van cariëse tanden;
- gingivitis;
- tandvleesaandoening (parodontitis);
- osteomyelitis van de kaak;
- flegmonen van verschillende lokalisaties;
- tonsillitis en paratonsillitis (phlegmoneuze tonsillitis);
- chronische sinusitis;
- retrofaryngeaal abces na streptokokken-tonsillitis met necrose en sepsis (syndroom van Lemierre);
- bronchiëctasieën;
- etterende longontsteking;
- longabces;
- empyeem van het longvlies;
- hersenabcessen;
- etterende ontsteking van de buikorganen;
- erosieve balanitis en balanoposthitis;
- acute colpitis (vaginitis) en vulvitis;
- purulent-septische complicaties van medische abortussen;
- colitis ulcerosa;
- ziekte van Crohn;
- bloedvergiftiging.
Onderzoekers van Harvard Medical School en het Dana-Faber Cancer Institute voerden een genomische analyse uit van colorectale kankertumoren en vonden daarin een abnormaal groot aantal fusobacteriën F. nucleatum. Tot op heden zijn er studies gaande om de hypothese te bevestigen (of te weerleggen) dat fusobacteriën betrokken zijn bij de ontwikkeling van colon- en rectumkanker. Feit is dat het bacteriële oppervlakte-eiwit adhesine A (dat we hierboven noemden) zich bindt aan het transmembraanglycoproteïne van menselijke epitheelcellen E-cadherine. Dit eiwit zorgt voor intercellulaire adhesie in onze weefsels en kan kankercellen aan elkaar "lijmen", waardoor hun invasie wordt voorkomen. Maar fusobacteriën neutraliseren het, waardoor ongehinderde proliferatie van kankercellen begint. [ 4 ], [ 5 ]
Behandeling van Fusobacteriën
De behandeling van fusobacteriën, of beter gezegd de medicamenteuze behandeling van fusobacteriële ziekten, gebeurt met antibiotica.
Van de antibacteriële middelen geven artsen de voorkeur aan de middelen die het meest effectief zijn tegen F. nucleatum en F. necrophorum: clindamycine, carbenicilline, cefoxitine, cefoperazon, cefamandol, fosfimycine, ornidazol. Het voorschrijven van een specifiek medicijn hangt uiteraard af van de diagnose en het klinische beeld van de ziekte.
Carbenicilline (handelsnamen: Carbecin, Fugacillin, Microcillin, Pyocyanil, enz.) werkt uitsluitend op gramnegatieve bacteriën en wordt gebruikt bij peritonitis, sepsis, meningitis en osteomyelitis als onderdeel van een complexe therapie.
Het cefalosporine-antibioticum van de tweede generatie Cefoxitine (Mefoxine, Atralxitine, Boncefin) wordt aanbevolen voor een breed scala aan ziekten met een bacteriële oorzaak, waaronder tonsillitis, longontsteking, urineweginfecties, botten, gewrichten, huid en weke delen. Het wordt voorgeschreven om infectieuze complicaties na een operatie te voorkomen.
En het medicijn Fosfomycine (Fosfomycine trometamol, Monural, Urofosfabol) wordt gebruikt voor urologische bacteriosen - recidiverende cystitis of niet-specifieke urethritis (enkele dosis 3 g).
Aan het begin van dit artikel beloofden we de mate van gevaar voor de mens van de kleine eencellige fusobacterie te onderzoeken. Ja, hij kan pathogeen zijn, maar aan de andere kant kan een mens zijn aanwezigheid in de microflora niet uitbannen.


 [
[