Medisch expert van het artikel
Nieuwe publicaties
Osteoblastoclastoom
Laatst beoordeeld: 29.06.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
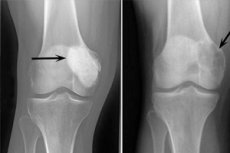
Osteoblastoclastoom is een tumor die zowel goedaardig als kwaadaardig kan zijn en verschillende skeletbotten aantast. Aanvankelijk werd de pathologie gigantocellulaire tumor genoemd (sinds 1912), 10 jaar later stelde Dr. Stewart de naam osteoclastoom voor. Pas in 1924 introduceerde professor Rusakov de verfijnde term "osteoblastoclastoom", die beter overeenkwam met de cellulaire samenstelling van het neoplasma.
Tegenwoordig wordt osteoblastoclastoom beschouwd als een echte neoplasma, een tumor van het zachte weefsel met een uitgebreid vaatnetwerk. De enige juiste behandelingsoptie is verwijdering van de tumor in het gezonde weefsel, soms gelijktijdig met bottransplantatie. [ 1 ]
Epidemiologie
De incidentie van bottumoren wereldwijd varieert van 0,5 tot 2%. Volgens Amerikaanse statistieken komen osteosarcoom (ongeveer 34% van de gevallen), chondrosarcoom (27%) en Ewing-tumor (18-19%) het meest voor. Chordomen, fibrosarcomen, fibrosarcomen, histiocytomen, reusceltumoren en angiosarcomen komen minder vaak voor.
De incidentie is sterk gecorreleerd met de leeftijd. Zo wordt de eerste golf van tumorgroei waargenomen in de adolescentie (rond de leeftijd van 16 jaar) en de tweede golf op middelbare leeftijd.
Osteoblastoclastoom is een relatief veel voorkomende tumor. Het komt voor bij ongeveer 2-30% van alle bottumoren. Vrouwen worden vaker getroffen, maar ook mannen kunnen er last van krijgen, vooral tussen de 18 en 40 jaar. Kinderen jonger dan 12 jaar worden zelden getroffen, maar zelfs in deze leeftijdscategorie is de incidentie niet uitgesloten. Er zijn beschrijvingen van familiale en erfelijke gevallen van osteoblastoclastoom.
Meestal (ongeveer 75%) wordt de tumor aangetroffen in de lange buisvormige botten, veel minder vaak worden platte en kleine botten aangetast.
Bij lange buisvormige botten is vooral de epimetafyse aangedaan, en bij kinderen de metafyse. Het neoplasma zaait niet uit in het gebied van het epifysair en gewrichtskraakbeen. Zeer zelden wordt het probleem in de diafyse gevonden (minder dan 0,5% van de gevallen).
Er wordt opgemerkt dat met de ontwikkeling van de geneeskunde de incidentie van osteoblastoclastoom stabiel blijft, maar de sterftecijfers aanzienlijk zijn gedaald. De belangrijkste en meest waarschijnlijke oorzaak van pathologie wordt beschouwd als de impact van ioniserende straling. De risico's zijn dus verhoogd bij mensen die hoge doses radiotherapie hebben ondergaan, evenals bij patiënten die zijn geïnjecteerd met radio-isotopen (voor diagnostische of therapeutische doeleinden). Andere veel voorkomende etiologische factoren zijn ongunstige ecologie en erfelijkheid. [ 2 ]
Oorzaken osteoblastoclastomen
Osteoblastoclastoom is een brandpunt van pathologisch veranderde cellen die in vrijwel elk deel van het skelet kunnen voorkomen. Ondanks de structurele afwijkingen blijven pathologische cellen zich delen, net als in gezond weefsel. Hun structuur wijkt sterk af van de norm, wat inhoudt dat de eigenschappen van het direct aangetaste bot en de typische functie ervan worden vervangen. Pathologisch veranderde kwaadaardige cellen ontwikkelen een neiging tot ongecontroleerde, vaak snelle vermenigvuldiging, waardoor het tumorvolume toeneemt. Voorheen normaal botweefsel kan door de structuren van het neoplasma worden verdrongen, en individuele pathologische cellen kunnen worden gescheiden en met bloed of lymfe naar andere, verder gelegen anatomische zones worden getransporteerd. Op deze manier ontstaan metastasen.
Het is bekend dat de bron van maligne osteoblastoclastomen elke maligne neoplasma kan zijn, waar dan ook in het lichaam (inclusief tumoren van inwendige organen). De verspreiding van het proces verloopt via metastasen. Maar de meeste osteoblastoclastomen (zowel goedaardig als kwaadaardig) zijn primaire neoplasmen die als eerste verschijnen en zich op dezelfde plaats ontwikkelen.
Over het algemeen zijn osteoblastoclastomen multifactoriële tumoren waarvan de exacte oorzaken momenteel nog niet zijn vastgesteld. De volgende aandoeningen kunnen leiden tot neoplasmata:
- Een immuundeficiëntietoestand;
- Aangeboren weefselveranderingen;
- Mutagene omgevingsinvloeden;
- Hormonale veranderingen;
- Bijkomende pathologieën en verwondingen (trauma is vaak aanwezig in de anamnese).
Risicofactoren
Er is een gebrek aan precieze gegevens over de oorzaken van osteoblastoclastoomvorming. Deskundigen suggereren echter dat een aantal factoren een verhoogd risico op botoncopathologieën met zich meebrengen:
- Erfelijkheid. In veel gevallen is de aanleg voor tumorgroei genetisch bepaald. Dit kan met name het geval zijn bij het Leigh Fraumeni-syndroom, dat predisponeert voor de ontwikkeling van diverse neoplasmata, waaronder kankergezwellen en sarcomen.
- De ziekte van Paget. De ziekte kan één of meerdere botten aantasten en behoort tot de pretumorale pathologieën. Bij patiënten met deze aandoening verdikken en broosen de botten tegelijkertijd, wat resulteert in frequente pathologische fracturen. Osteosarcoom komt voor in ongeveer 8% van de gevallen van ernstige ziekte van Paget.
- Meerdere botwoekeringen, exostosen.
- Meerdere osteochondromen (inclusief erfelijke).
- Meerdere enchondromen (risico is klein maar nog steeds aanwezig).
- Blootstelling aan straling (waaronder intense straling die wordt gebruikt om andere tumorprocessen te behandelen en de effecten van radioactief radium en strontium).
Een speciale risicocategorie betreft bestralingsbehandelingen op kinder- en jonge leeftijd, waarbij doses van meer dan 60 Gray worden toegediend.
Deskundigen wijzen erop dat niet-ioniserende straling, met name microgolf- en elektromagnetische straling, die afkomstig is van elektriciteitskabels, mobiele telefoons en huishoudelijke apparaten, geen risico's op osteoblastoclastomen met zich meebrengt.
Pathogenese
De pathogenetische kenmerken van het ontstaan en de ontwikkeling van osteoblastoclastomen worden niet volledig begrepen, vanwege de complexiteit van de pathologie. De basisoorzaak van tumorvorming is een falende celdifferentiatie als gevolg van een verstoorde werking van het immuunsysteem. Dit leidt tot de groei van een tumor bestaande uit "verkeerde", ongedifferentieerde cellen, die de eigenschappen van het neoplasma bepalen en structureel lijken op onrijpe cellen. Als de celstructuur bijna normaal is, maar niet normaal, wordt gesproken van een goedaardig osteoblastoclastoom. Bij uitgesproken veranderingen in de celstructuur wordt de tumor toegeschreven aan kwaadaardige processen. Voor een dergelijk neoplasma zijn een verandering in de antigene celplooi, ongecontroleerde groei en celdeling kenmerkend. Samen met het verlies aan specificiteit van de celstructuur lijdt ook de functionaliteit eronder. Maligne osteoblastoclastomen onderscheiden zich onder andere van goedaardige osteoblastoclastomen door het proces van invasie in nabijgelegen gezonde weefsels. Bij goedaardige bottumoren is er geen sprake van uitgroei tot gezonde structuren, is er geen neiging tot snelle groei en verspreiding door het lichaam, en is er geen neiging tot willekeurige zelfvernietiging en vergiftiging door producten van de ontbinding van de tumor.
De botstructuur wordt in alle gevallen vernietigd, ongeacht de goedaardigheid van de pathologie. Als gevolg hiervan wordt het aangetaste botsegment broos en broos. Vaak is een pathologische fractuur die zelfs onder minimale belasting optreedt, de reden om een arts te raadplegen.
Het is belangrijk om op te merken: de goedaardigheid van het proces is altijd een voorwaardelijke toestand, omdat er risico's op maligniteit bestaan en als de goedaardige focus wordt getransformeerd, ontstaat er kwaadaardig osteoblastoclastoom.
Symptomen osteoblastoclastomen
Het klinische beeld bij osteoblastoclastomen hangt voornamelijk af van de lokalisatie en het stadium van het pathologische proces. In de regel wordt de tumor gekenmerkt door de volgende kenmerken:
- Het neoplasma is solitair;
- Tast vooral de buisvormige botten van de onderste of bovenste ledematen aan;
- Wordt minder vaak aangetroffen bij platte botten;
- Er is een zeurende pijn in het aangetaste segment;
- Het huid- en vaatpatroon ter hoogte van de pathologische focus neemt toe;
- Het zieke ledemaat is misvormd (lokale volumetoename);
- Het werk van het gewricht dat het dichtst bij het osteoblastoclastoom ligt of van de ledemaat als geheel is verstoord;
- Palpatoir bepaalde, verdichte focus met een karakteristieke "perkamentknisper".
Over het algemeen kunnen symptomen worden onderverdeeld in lokale en algemene symptomen. Lokale symptomen worden visueel waargenomen - met name de aanwezigheid van een kromming of uitstulping van het botfragment. De aandacht wordt ook gevestigd op de verandering in de huid boven de pathologische focus: een duidelijk vaatpatroon is zichtbaar, de weefsels zijn gezwollen of afgeplat. De tumor kan worden gepalpeerd - vaak pijnloos, maar heeft een karakteristieke structuur. Kwaadaardige tumoren zijn meestal knobbelig en onregelmatig van vorm.
Het aangrenzende gewricht kan bewegingsbeperking en aanhoudende pijn vertonen. Door compressie van bloedvaten en zenuwbanen is de gevoeligheid vaak verminderd en treedt aanhoudende zwelling op. Ook het lymfestelsel reageert: nabijgelegen lymfeklieren worden groter.
De algemene symptomatologie is kenmerkender voor maligne osteoblastoclastomen en is het gevolg van de vergiftigingsprocessen van het lichaam. Patiënten kunnen last hebben van:
- Koorts, koortsachtige aandoeningen;
- Onuitputtelijkheid;
- Constante zwakte;
- Slaperigheid of slapeloosheid, eetluststoornissen;
- Overmatig zweten 's nachts;
- Instorten.
Er is ook een klein percentage osteoblastoclastomen, die meestal klein en klinisch niet zichtbaar zijn. Ze worden om andere redenen een toevallige bevinding tijdens radiologisch of beeldvormend onderzoek.
Eerste tekenen van osteoblastoclastoom-ossificatie
- Versnelling van de groei van het neoplasma.
- Verhoogd pijnsyndroom.
- Uitbreiding van de diameter van de destructieve focus, of transformatie van de cellulair-trabeculaire vorm in een lytische vorm.
- Desintegratie van de corticale laag over een relatief lang gebied.
- Verlies van helderheid van configuraties van de destructieve focus.
- Desintegratie van de sluitplaat die het medullaire kanaal blokkeerde.
- Periostale reactie.
Maligniteit van osteoblastoclastomen is gebaseerd op klinische en radiologische indicatoren en wordt noodzakelijkerwijs bevestigd door morfologische diagnose van tumorweefsels.
Naast oscoplastificatie van een aanvankelijk goedaardige neoplasma is er ook sprake van een primair kwaadaardig osteoblastoclastoom. Een dergelijke tumor is in feite een type sarcoom met osteogene oorzaak.
De locatie van maligne osteoblastoclastomen is dezelfde als bij benigne osteoblastoclastomen. Röntgenfoto's tonen een destructieve focus in het botweefsel zonder duidelijke contouren. De destructie van de corticale laag is uitgebreid en breidt zich vaak uit naar zachte weefselstructuren.
Tekenen om maligne osteoblastoclastoom te onderscheiden van de osteogene vorm van osteoclastisch sarcoom:
- De overwegend oudere leeftijd van de patiënten;
- Minder levendige symptomatologie;
- Een gunstiger prognose op lange termijn.
Osteoblastoclastoom bij kinderen
Osteoblastoclastoom bij kinderen is zeldzaam: er zijn slechts twee of drie gevallen per miljoen kinderen. Opgemerkt dient te worden dat onder alle pediatrische patiënten de leeftijdsgroep ouder dan 10-15 jaar het grootst is.
Wetenschappers kunnen de exacte oorzaak van osteoblastoclastoom bij kinderen niet achterhalen. Vermoedelijk houdt de pathologie verband met de intensieve groei van het lichaam van het kind, en met een genetische factor.
Er zijn ook aanwijzingen voor mogelijke oorzaken zoals blootstelling aan radioactieve stoffen (met name radiotherapie) en chemotherapie (het gebruik van cytostatica). Veel chemotherapiemedicijnen kunnen het genetische materiaal van botcellen vernietigen, wat leidt tot de ontwikkeling van tumoren.
Bovendien is het risico op osteoblastoclastoom hoger bij kinderen met bepaalde aangeboren afwijkingen, zoals bilateraal retinoblastoom of het Li-Fraumeni-syndroom. Er bestaat ook een causaal verband met de ziekte van Paget.
Het is ook bekend dat artsen bij de overgrote meerderheid van de kinderen (ongeveer 90%) geen van de hierboven genoemde risicofactoren kunnen vaststellen.
Het is moeilijk om het beloop van osteoblastoclastoom bij kinderen te voorspellen, omdat het afhangt van de kenmerken van de specifieke tumor, de lokalisatie ervan, de mate van verspreiding op het moment van diagnose, de tijdigheid van de behandeling en de volledigheid van de verwijdering van de neoplasma.
De kwaliteit van de behandeling van osteoblastoclastomen heeft de afgelopen 2-3 decennia grote vooruitgang geboekt. Het therapeutische protocol is gecombineerd en het genezingspercentage is gestegen tot meer dan 70-80%. Een gunstig resultaat kan worden bereikt als de tumor radicaal operatief wordt verwijderd en het effect wordt geconsolideerd met een voldoende chemotherapiekuur. Kinderen met een benigne osteoblastoclastoom hebben de beste kans op herstel.
Wanneer specifieke cijfers over genezen patiënten worden bekendgemaakt, zien we slechts algemene cijfers: geen enkele statistiek kan de kansen voor een bepaald kind nauwkeurig voorspellen en bepalen. Onder 'herstel' verstaan we primair 'afwezigheid van tumorvorming in het lichaam', aangezien moderne therapeutische benaderingen een langdurige afwezigheid van recidief kunnen garanderen. Men mag echter de mogelijkheid van ongewenste bijwerkingen en late complicaties niet vergeten. Daarom moet elke behandeling, ongeacht de complexiteit ervan, uitmonden in hoogwaardige revalidatiemaatregelen. Bovendien hebben kinderen nog steeds lange tijd orthopedische zorg nodig.
Vormen
De classificatie van botweefselneoplasmata is vrij breed. Er wordt vooral gekeken naar variaties in de celstructuur en morfologische kenmerken van het tumorproces. Tumoren worden daarom onderverdeeld in twee categorieën:
- Osteogene (gevormd op basis van botcellen);
- Neosteogeen (gevormd in bot onder invloed van andere celtypen - bijvoorbeeld vaat- of bindweefselstructuren).
Osteoblastoclastomen van het bot zijn overwegend goedaardige tumoren. Desondanks hebben ze vaak een agressieve groei en dragen ze bij aan de vernietiging en verdunning van botweefsel, waardoor chirurgische ingrepen noodzakelijk zijn. Tegelijkertijd kunnen reuzencelosteoblastoclastomen ook kwaadaardig zijn.
Afhankelijk van de klinische en radiologische parameters en het morfologische beeld worden drie basisvormen van osteoblastoclastomen onderscheiden:
- De cellulaire vorm komt vooral voor bij ouderen en wordt gekenmerkt door een trage ontwikkeling. De diagnose toont een verdikte, klonterige zwelling, zonder dat de tumorhaard klinisch kan worden onderscheiden van gezonde botzones.
- De cystevorm manifesteert zich allereerst met pijn. Palpatoir wordt het symptoom van "perkamentcrunch" vastgesteld. Visueel wordt een benige tumor met een glad convexe, koepelvormige configuratie opgemerkt.
- De lytische vorm wordt beschouwd als een zeldzame variant van de pathologie, die vooral in de adolescentie wordt vastgesteld. Het tumorproces ontwikkelt zich snel genoeg, de patiënt begint pijn te ervaren, ook bij palpatie.
Een reuzenceltumor kan zich op vrijwel elk bot van het skelet vormen, hoewel de buisvormige botten van de ledematen, ribben en wervelkolom iets vaker worden aangetast. Osteoblastoclastoom van de onderkaak komt twee keer zo vaak voor als in de bovenkaak. Palpatoir wordt een dicht neoplasma met verweekte zones opgemerkt. De meest voorkomende klachten van patiënten: de aanwezigheid van een uitstulping die bloedt en ongemak veroorzaakt bij het kauwen van voedsel. Naarmate het probleem vordert, wordt het aangevuld met een verminderde functie van het kaakgewricht. Van de buisvormige botten treft de tumor vaker het dijbeen en het scheenbeen. Osteoblastoclastoom van het dijbeen komt voornamelijk voor bij mensen van middelbare leeftijd. De ziekte gaat gepaard met een verminderde functie van het corresponderende gewricht, er treedt kreupelheid op en de huid boven het neoplasma is bedekt met een uitgesproken vaatpatroon.
Naast de bovenstaande classificatie zijn er centrale en perifere vormen van pathologie, hoewel er geen morfologische verschillen tussen beide bestaan. Perifeer osteoblastoclastoom is gelokaliseerd in het tandvlees, en de centrale vorm ontwikkelt zich in het bot en wordt gekenmerkt door de aanwezigheid van meerdere bloedingen (daarom is de tweede naam voor centraal osteoblastoclastoom een bruine tumor). De bruine kleur wordt veroorzaakt door de afzetting van erytrocyten, die afbreken onder vorming van hemosiderine.
Kwaadaardige bottumoren doorlopen de volgende stadia in hun ontwikkeling:
- In het bot en één musculofasciaal segment bevinden zich T1-foci van 3-5 cm.
- De T2-haarden strekken zich niet verder dan 10 cm uit langs het bot, maar reiken niet verder dan één fasciaal omhulsel.
- De T3-haarden verlaten de grenzen van één musculofasciaal geval en groeien uit naar een nabijgelegen geval.
- De T4-haarden ontspringen uit de huid of neurovasculaire stammen.
Op vergelijkbare wijze worden de mate van betrokkenheid van de lymfeklieren en de verspreiding van metastasen gecategoriseerd.
Complicaties en gevolgen
Tot de complicaties van osteoblastoclastoom behoort elke toename van de activiteit van het neoplasma, die vooral vaak optreedt tegen de achtergrond van een lange periode van rust. In sommige gevallen gaat het om kwaadaardige degeneratie van het tumorproces, of uitgroei in gevoelige nabijgelegen anatomische structuren.
- Uitbreiding naar de zenuwstam veroorzaakt neuropathisch pijnsyndroom door de invloed op de grote zenuw. Deze pijn verdwijnt vrijwel niet na het gebruik van conventionele pijnstillers, waardoor de patiënt letterlijk uitgeput raakt.
- De verspreiding naar de bloedvaten kan gecompliceerd worden door plotselinge, hevige bloedingen en hematoomvorming.
Complicaties zijn niet uitgesloten, die gepaard gaan met een schending van de functie van nabijgelegen gewrichten: de groei van osteoblastoclastoom blokkeert in een dergelijke situatie de adequate werking van het bewegingsapparaat, wat leidt tot een beperkte bewegingsvrijheid en het optreden van pijnsyndroom.
De meest voorkomende complicaties van osteoblastoclastoom zijn pathologische fracturen in het getroffen gebied. Het probleem doet zich zelfs voor bij een kleine traumatische impact, omdat het botweefsel extreem broos en instabiel wordt.
Daarnaast spreken specialisten ook over specifieke algemene en lokale bijwerkingen die kenmerkend zijn voor maligne osteoblastoclastomen:
- De vorming van uitzaaiingen op afstand en dichtbij;
- Vergiftiging van het lichaam met afbraakproducten.
Als er enige tijd na de eerste diagnostische maatregelen toch metastasen worden vastgesteld, wijst dit op de ineffectiviteit van de behandeling en op progressie van de tumor.
Een aparte reeks complicaties is het ontstaan van een nieuwe tumor of algemene pathologie als gevolg van chemotherapie of bestraling van de osteoblastoclastoombothaard.
Diagnostics osteoblastoclastomen
Diagnostische methoden die worden gebruikt om osteoblastoclastoom op te sporen, zijn onder meer:
- Klinisch, wat inhoudt dat er uitwendig onderzoek en palpatie van het pathologisch veranderde gebied plaatsvindt;
- Röntgenfoto (anteroposterieure en laterale radiografie, indien geïndiceerd - gerichte en schuine radiografie);
- Tomografisch (met behulp van computer- of magnetische resonantiebeeldvorming);
- Radio-isotoop;
- Morfologisch, wat histologische, histochemische en cytologische analyse omvat van biomateriaal verkregen tijdens punctie of trepanobiopsie;
- Laboratorium.
De arts bestudeert zorgvuldig de ziektegeschiedenis, stelt de eerste tekenen vast, specificeert de locatie en het type pijnsyndroom, de kenmerken ervan, houdt rekening met de resultaten van eerdere onderzoeken en behandelprocedures en beoordeelt de dynamiek van de algemene toestand van de patiënt. Bij een vermoeden van pathologie van de lange buisvormige botten let de specialist op de aanwezigheid van zwelling, motorische beperkingen in de nauwere gewrichten, evenals op neurologische symptomen, spierzwakte en hypotrofie. Het is belangrijk om de inwendige organen zorgvuldig te onderzoeken op mogelijke uitzaaiingen.
Bij alle patiënten worden algemene bloed- en urinetests afgenomen om de eiwit- en eiwitfracties, fosfor en calcium en siaalzuren te bepalen. Ook de enzymatische activiteit van fosfatasen, een definitietest en de index van C-reactief proteïne (CRP) moeten worden bepaald. Indien het nodig is om osteoblastoclastoom van myloom te onderscheiden, moet de patiënt een urinetest ondergaan om de aanwezigheid van pathologisch Bence-Jones-eiwit te bepalen.
Radiologische diagnose is essentieel voor de diagnose van osteoblastoclastoom. Verplichte controles en gerichte röntgenfoto's, hoogwaardige tomografie, maken het mogelijk om de locatie, het type pathologische focus en de verspreiding ervan naar andere weefsels en organen te verduidelijken. Dankzij CT is het mogelijk om de toestand van de weke delen en de dunste botstructuren in het benodigde vlak te verduidelijken, diepe foci van pathologische destructie te identificeren, hun parameters binnen de botgrenzen te beschrijven en de mate van schade aan de omliggende weefsels te bepalen.
Tegelijkertijd wordt MRI beschouwd als de meest informatieve diagnostische procedure, die een aantal voordelen heeft ten opzichte van zowel radiografie als CT. De methode stelt u in staat om zelfs de dunste weefsellagen te onderzoeken en pathologische afwijkingen in beeld te brengen met behulp van een ruimtelijk driedimensionaal beeld.
Verplichte instrumentele diagnostiek bestaat uit morfologisch onderzoek. Biomateriaal wordt beoordeeld, verkregen via aspiratie en trepanobiopsie, of tijdens resectie van botsegmenten samen met het neoplasma. Punctiebiopsie wordt uitgevoerd met behulp van speciale naalden en radiologische controle.
De volgende röntgenverschijnselen worden als typisch voor osteoblastoclastoom beschouwd:
- Porositeitsbeperking;
- Homogeniteit van botlysis bij het type dunne trabeculisatie;
- De aanwezigheid van pseudocystische lucenties met de structuur van eigenaardige "zeepbellen".
Dit röntgenbeeld gaat gepaard met de afwezigheid van primaire of secundaire reactieve osteoformatieve periostose. Er wordt verdunning en atrofie van de corticale laag waargenomen.
Maligne osteoblastoclastoom als gevolg van intensieve vasculaire groei gaat gepaard met een toename van veneuze stase. Vasculaire veranderingen vertonen het uiterlijk van een neoplasma met overvloedige vascularisatie.
Differentiële diagnose
Het is soms erg moeilijk om osteoblastoclastoom te identificeren. Er ontstaan problemen bij de differentiële diagnose van de ziekte met osteogeen sarcoom en botcysten bij patiënten van verschillende leeftijden. Volgens de statistieken werd osteoblastoclastoom in meer dan 3% van de gevallen verward met osteogeen sarcoom en in bijna 14% met botcyste.
De tabel vat de belangrijkste symptomen van deze pathologieën samen:
Indicatoren |
Osteoblastoclastoom |
Osteogene osteoplastische sarcoom |
Botcyste |
Meest voorkomende incidentieleeftijd |
20 tot 30 jaar oud |
20 tot 26 jaar oud |
Kinderen jonger dan 14 jaar |
Locatie |
Epimetafysaire regio |
Epimetafysaire regio |
Metadiafysegebied |
Botreconfiguratie |
Ernstige asymmetrische uitstulping. |
Kleine dwarsuitbreiding |
Een spoelvormige uitstulping. |
Configuratie van de destructieve focus |
De contouren zijn duidelijk |
De contouren zijn vaag, er is geen duidelijkheid |
De contouren zijn duidelijk |
De toestand van het wervelkanaal |
Bedekt door een afsluitplaat |
Open aan de grens met het neoplasma |
Geen verandering. |
Conditie van de corticale laag |
Dun, vezelig, onderbroken. |
Uitdunnen, verwoest |
Dun, plat |
Sclerose verschijnselen |
Atypisch |
Cadeau |
Atypisch |
Periostale reactie |
Afwezig |
Aanwezig op een manier die lijkt op een "periostaal vizier" |
Afwezig |
De toestand van de epifyse |
De bladschijf is dun en golvend. |
In het beginstadium blijft een deel van de epifyse intact |
Geen verandering. |
Nabijgelegen botgedeelte |
Geen verandering. |
Tekenen van osteoporose |
Geen verandering. |
Voor verplichte aandacht zijn indicatoren nodig zoals de leeftijd van de patiënt, de duur van de pathologie, de locatie van het aangetaste aandachtspunt en andere anamnestische informatie die in de tabel staat aangegeven.
De volgende diagnostische fouten komen het meest voor wanneer osteoblastoclastoom wordt verward met dergelijke pathologische processen:
- Aneurysmatische cyste (gelokaliseerd in de diafyse of metafyse van lange buisvormige botten);
- Monoaxiale vorm van fibreuze osteodysplasie (manifesteerd zich voornamelijk in de kindertijd, gepaard gaand met kromming van de botten zonder botbolvorming);
- Hyperparathyroïde osteodystrofie (geen duidelijke afbakening van de focus ten opzichte van het gezonde botgebied, geen duidelijke botuitstulping);
- Solitaire kankerachtige botmetastasen (gekenmerkt door destructieve haarden met gebogen, "aangevreten" contouren).
Het is belangrijk om te onthouden dat een goedaardig osteoblastoclastoom altijd kan transformeren en kwaadaardig kan worden. De oorzaken van maligniteit zijn nog niet precies vastgesteld, maar wetenschappers denken dat trauma en hormonale veranderingen (bijvoorbeeld tijdens de zwangerschap) hieraan bijdragen. Volgens sommige waarnemingen is maligniteit ook opgetreden bij herhaalde reeksen bestralingen op afstand.
Symptomen van ossificatie:
- Het neoplasma begint snel te groeien;
- De pijn wordt erger;
- De omvang van de destructieve focus neemt toe en de cellulair-trabeculaire fase gaat over in de lytische fase;
- De corticale laag is aan het afbreken;
- De contouren van de destructieve focus worden onduidelijk;
- De vergrendelingsplaat stort in;
- Er is een periostale reactie.
Bij de differentiatie van primair maligne neoplasma (osteogene osteoclastisch sarcoom) en maligne osteoblastoclastoom wordt speciale aandacht besteed aan de pathologieduur en de beoordeling van het radiologische beeld in de dynamiek. Op de röntgenfoto van het primair maligne neoplasma is er geen botuitsteeksel te zien, typisch voor een osteoblastoclastoom, er zijn geen botbruggen en er is een gescleroseerde zone met onduidelijke contouren zichtbaar. Bij maligniteit is er echter vaak een klein deel van de sluitplaat aanwezig, dat vroeger als barrière voor het gezonde botsegment diende.
Met wie kun je contact opnemen?
Behandeling osteoblastoclastomen
De enige juiste behandeling voor patiënten met osteoblastoclastoom is een operatie. De meest milde ingreep vindt plaats in de beginfase van de tumorontwikkeling en bestaat uit het verwijderen van het aangetaste weefsel en het opvullen van de holte met een transplantaat. Het transplantaat wordt uit een ander gezond bot van de patiënt gehaald. Een dergelijke ingreep is het meest gunstig en minder traumatisch, maar in sommige gevallen ook minder radicaal. Verwijdering van het aangetaste botfragment samen met het neoplasma wordt beschouwd als een betrouwbaardere methode, die de kans op tumorgroei tot een minimum beperkt.
Als het een verwaarloosd osteoblastoclastoom van grote omvang betreft, dat bijzonder gevoelig is voor maligniteit of al kwaadaardig is, wordt vaak een gedeeltelijke of volledige amputatie van de ledemaat overwogen.
Over het algemeen wordt de tactiek van de chirurgische behandeling van osteoblastoclastomen gekozen afhankelijk van de locatie, de verspreiding en de agressiviteit van de pathologische focus.
Als de tumor de lange buisvormige botten aantast, is het raadzaam om aandacht te besteden aan de volgende chirurgische ingrepen:
- Randresectie met alloplastie of autoplastiek voor benigne, vertraagde processen, foci met een cellulaire structuur en in de periferie van de epimetafyse. Fixatie met metalen schroeven.
- Wanneer een cellulair osteoblastoclastoom zich uitbreidt tot het midden van de botdiameter, worden twee derde van de condylus, een deel van de diafyse en het gewrichtsoppervlak gereseceerd. Het defect wordt opgevuld met een allogeen gewrichtskraakbeentransplantaat. Het wordt stevig vastgezet met bouten en schroeven.
- Bij epimetafyse-cariës over de gehele lengte of bij een pathologische fractuur worden tactieken zoals segmentale resectie met articulaire excisie en het opvullen van het defect met een allotransplantaat gebruikt. Fixatie vindt plaats met een gecementeerde staaf.
- Bij een pathologische fractuur en maligniteit van het osteoblastoclastoom in de proximale femurregio wordt een totale heupprothese geplaatst.
- Bij resectie van de uiteinden in de gewrichtszone van de knie wordt de techniek van allopolysubstance transplantatie met fixatie gebruikt. Een totale endoprothese met een verlengde titanium steel verdient vaak de voorkeur om een aansluitende radiotherapie te garanderen.
- Als de pathologische focus zich aan het distale uiteinde van de tibia bevindt, wordt resectie met botplastische enkelartrodese uitgevoerd. Als het talusbot is aangetast, wordt het geëxtirpeerd met extensieartrodese.
- Bij cervicale wervelkolomlaesies wordt een anterieure toegang tot de C1 en C2 wervels uitgevoerd. Een anterolaterale toegang heeft de voorkeur. Op Th1-Th2 niveau wordt een anterieure toegang met schuine sternotomie naar de derde intercostale ruimte gebruikt (vaten worden voorzichtig naar beneden verschoven). Als de tumor de lichamen van 3-5 thoracale wervels aantast, wordt een anterolaterale toegang met resectie van de derde rib uitgevoerd. De scapula wordt naar achteren verschoven zonder de musculatuur af te snijden. Als het osteoblastoclastoom in de thoracolumbale regio tussen Th11 en L2 wordt gevonden, is de operatie van keuze een rechtszijdige thoracofrenolumbotomie. Toegang tot het anterieure deel van de bovenste 3 wervels van het sacrum is moeilijker. Een anterolaterale retroperitoneale rechtszijdige toegang met zorgvuldige drainage van de vasculaire stammen en ureter wordt aanbevolen.
- Indien de wervellichamen ernstig zijn vernietigd of de pathologie zich heeft uitgebreid naar de boogregio in de thoracale en lumbosacrale wervelkolom, wordt in dit geval een transpediculair-translaminaire fixatie van de wervelkolom uitgevoerd, waarna de vernietigde wervels worden verwijderd met een verdere autoplastiek.
- Als een goedaardige vorm van osteoblastoclastoom wordt vastgesteld in de wenkbrauw en het ischias, wordt het pathologisch veranderde segment verwijderd in gezond weefsel, zonder bottransplantaat. Als de bodem en het dak van het acetabulum zijn aangetast, wordt resectie uitgevoerd met verdere bottransplantaat om het defect te vervangen, met fixatie met spongiose-fixatie.
- Als het darmbeen, de borstkas of het ischiasbeen is aangetast, wordt een alloplastie met een structureel allotransplantaat, transplantosteosynthese, cementgebonden plastische implantatie en repositionering van de prothesekop in een kunstmatige holte uitgevoerd.
- Als het sacrum en L2 zijn aangetast, wordt een interventie in twee fasen uitgevoerd, bestaande uit posterieure toegangsresectie van het pathologisch veranderde onderste sacrale fragment (tot S2 ), transpediculaire fixatie en verwijdering van het neoplasma van de anterieure zijde door retroperitoneale methode met bottransplantaat.
In elke specifieke situatie bepaalt de arts de meest geschikte chirurgische ingreepmethode. Daarbij overweegt hij of het mogelijk is om de nieuwste technologieën toe te passen om de resultaten van de behandeling te verbeteren en de normale kwaliteit van leven van de patiënt te garanderen.
Het voorkomen
Er is geen specifieke preventie van osteoblastoclastoom. Dit komt allereerst door onvoldoende onderzoek naar de oorzaken van de ontwikkeling van dergelijke tumoren. Veel experts benadrukken het voorkomen van trauma aan het botstelsel als een van de belangrijkste preventiepunten. Er is echter geen bewijs voor de directe invloed van trauma op de vorming van bottumoren. Trauma vestigt in veel gevallen slechts de aandacht op het bestaande tumorproces en heeft geen duidelijke betekenis voor het ontstaan van de pathologische focus, maar kan tegelijkertijd bijdragen aan de groei ervan.
We mogen niet vergeten dat osteoblastoclastomen zich vaak vormen in botten die eerder zijn blootgesteld aan ioniserende straling, bijvoorbeeld voor de behandeling van andere tumorprocessen. Radio-geïnduceerde neoplasmata ontstaan meestal niet eerder dan drie jaar na blootstelling aan straling.
Tot de niet-specifieke preventieve maatregelen behoren:
- Het afleren van slechte gewoontes;
- Een gezonde levensstijl leiden;
- Kwalitatieve en duurzame voeding;
- Matige, regelmatige fysieke activiteit;
- Preventie van verwondingen, tijdige behandeling van pathologische processen in het lichaam, stabilisatie van de immuniteit.
Prognose
Pathologische fracturen komen vaak voor in het aangetaste botweefsel. In dit geval hebben goedaardige neoplasmata, mits een radicale behandelingsmethode wordt toegepast, een gunstige prognose, hoewel de mogelijkheid van recidieven en maligniteit van de pathologische focus niet wordt uitgesloten. Een ongunstige uitkomst van een goedaardig osteoblastoclastoom is niet uitgesloten indien de focus wordt gekenmerkt door actieve groei en uitgesproken botvernietiging. Een dergelijke tumor kan snel een volledig botsegment vernietigen, wat leidt tot de ontwikkeling van een pathologische fractuur en een aanzienlijke aantasting van de botfunctie. Bij dergelijke patiënten is het vaak moeilijk om het defect in het botweefsel operatief te vervangen en ontstaan complicaties die samenhangen met het niet genezen van de fractuur.
De gemiddelde vijfjaarsoverleving voor alle varianten van maligne osteoblastoclastomen, zowel bij kinderen als volwassenen, bedraagt 70%, wat als zeer goed kan worden beschouwd. We kunnen dus concluderen dat dergelijke neoplasmata in veel gevallen succesvol genezen. Uiteraard zijn ook aspecten zoals het type tumor, het stadium, de mate van laesie en de maligniteit van groot belang.
Het is duidelijk dat het maligne osteoblastoclastoom de grootste bedreiging vormt. In deze situatie kunnen we alleen spreken van een gunstige prognose bij vroege detectie, toegankelijke chirurgische lokalisatie en gevoeligheid van de focus voor chemopreventieve middelen en radiotherapie.

