Medisch expert van het artikel
Nieuwe publicaties
Anaplastisch meningioom
Laatst beoordeeld: 29.06.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
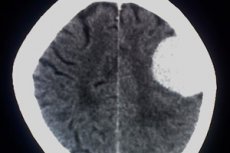
Arachnoïdaal endothelioom of anaplastisch meningeoom is een tumorpathologie die ontstaat vanuit arachnoïdaal endotheelweefsel. De tumor behoort tot de categorie relatief kwaadaardig en wordt volgens de WHO-classificatie ingedeeld in de derde graad van maligniteit.
Anaplastisch meningeoom wordt gekenmerkt door snelle groei en intensieve penetratie in de omliggende gezonde structuren, met daaropvolgende vernietiging. De tumor wordt als agressief-current beschouwd en kan al na enkele maanden groeien en grote volumes bereiken. Het maligne proces heeft een goed gedefinieerde structurele cellulaire atypie. [ 1 ]
Epidemiologie
Anaplastisch meningeoom ontstaat uit de cellen van het arachnoïdale medulla. Het is de meest voorkomende primaire tumor van het centrale zenuwstelsel. Het is meestal gelokaliseerd in het gebied van de schedel (convexitaal meningeoom), de bovenste sagittale sinus (parasagittaal meningeoom) en de vleugels van het hoofdbeen.
Het is minder vaak dat de tumor op andere plaatsen van de schedelbasis wordt aangetroffen:
- In de voorste of achterste schedelgroeve;
- Van de knobbel van het Turkse zadel;
- Van de kleine hersenentent;
- Laterale ventrikels;
- Van de oogzenuwschede.
Ongeveer 6% van de meningeomen bevindt zich in het wervelkanaal.
Anaplastisch meningeoom treft vooral oudere en middelbare patiënten. Bij kinderen wordt de ziekte slechts in geïsoleerde gevallen aangetroffen. Vrouwen hebben de ziekte iets vaker dan mannen, wat te wijten is aan frequente hormonale veranderingen. [ 2 ]
Oorzaken anaplastisch meningioom
Wetenschappers kunnen geen duidelijke oorzaak voor anaplastisch meningeoom geven. Vermoedelijk zijn er enkele provocerende factoren die verband houden met het ontstaan van de ziekte, zoals:
- Blootstelling aan straling (nucleair, blootstelling aan straling).
- Erfelijke aanleg.
- Negatieve effecten van vergiftigingen, chemicaliën die via de luchtwegen, slijmvliezen en voedingsmiddelen het lichaam kunnen binnendringen.
- Traumatisch hoofdletsel, schedel- en hersenletsel (vooral met verre gevolgen).
Mogelijke risico's kunnen zijn: roken, chronische infectieziekten, wonen in de buurt van hoogspanningsleidingen, een slecht voedingspatroon met veel onnatuurlijke voedingsmiddelen, regelmatige stress en een negatieve psycho-emotionele stemming.
Een van de onderwerpen ter overweging zijn kankerverwekkende stoffen in voedsel. We hebben het dan over margarines en gehydrogeneerde oliën, worst en halffabrikaten, snacks en chips, zoete frisdranken, enzovoort. Al deze producten veroorzaken onherstelbare schade, vooral tegen de achtergrond van een lage consumptie van plantaardige voedingsmiddelen. Al deze producten veroorzaken onherstelbare schade, vooral tegen de achtergrond van een lage consumptie van plantaardige voedingsmiddelen.
Exogene factoren omvatten altijd de omgeving, waaronder ioniserende straling, vochtigheid en luchtvervuiling. De relatie met de incidentie van oncologie is in dit geval direct. Atypische cellen beginnen te groeien, delen zich ongecontroleerd en vormen een anaplastisch meningioom. [ 3 ]
Risicofactoren
Het is belangrijk om op de hoogte te zijn van de risicofactoren die de kans op het ontwikkelen van een anaplastisch meningeoom vergroten:
- Gevorderde leeftijd;
- Oncologische pathologieën in de anamnese (zelfs succesvol behandeld);
- Kankerpathologieën bij bloedverwanten;
- Roken, alcoholmisbruik;
- Stofwisselingsstoornissen, hoofdtrauma;
- Bepaalde infectieuze processen - bijvoorbeeld het humaan papillomavirus;
- Blootstelling aan chemische en giftige stoffen;
- Ioniserende effecten (waaronder ultraviolette straling).
De risico's van CNS-neoplasieën, waaronder anaplastisch meningioom, worden herhaaldelijk verhoogd tegen de achtergrond van immunosuppressie, veroorzaakt door medicamenteuze therapie bij weefsel- en orgaantransplantaties, en ook in andere gevallen van ernstige verzwakking of stress van het immuunsysteem. [ 4 ]
Pathogenese
Bij sommige patiënten kan de ontwikkeling van een anaplastisch meningeoom te wijten zijn aan de aanwezigheid van een van de erfelijke aandoeningen, met name neurofibromatose type I en II, enzovoort. De meeste van deze syndromen worden overgedragen via autosomaal dominante overerving. Het aandeel erfelijke aandoeningen bedraagt echter niet meer dan 5-6%. Het resterende percentage primaire anaplastische meningeomen komt sporadisch voor, dat wil zeggen zonder een duidelijk omschreven oorzaak.
Typisch voor dit tumorproces is de diffuse groei met penetratie (uitlopers) in het gezonde hersenweefsel.
De vraag naar provocerende factoren bij de ontwikkeling van anaplastisch meningeoom is nog steeds actueel. Er is een grote kans op genetisch bepaalde ziekten, maar erfelijkheid prevaleert niet in alle gevallen. Mogelijke mutaties uiten zich in een schending van het aantal chromosomen en DNA-schade. Deze veranderingen beïnvloeden niet het hele organisme, maar alleen de weefsels van een bepaalde lokalisatie. Verworven of generatieve mutaties zijn gebaseerd op het concept van "kankerfactoren", maar worden niet altijd "erfelijk" overgedragen.
Het pathogene mechanisme van de ontwikkeling van meningiomen moet daarom individueel worden bekeken. Mensen die de ziekte al eens in hun naaste familie hebben gehad, zijn vatbaarder voor het optreden van het pathologische proces. Als er tumoren van het centrale zenuwstelsel in de familie voorkomen, verdubbelt het risico op een anaplastisch meningioom zelfs.
Symptomen anaplastisch meningioom
De symptomatologie van een anaplastisch meningeoom is divers en hangt voornamelijk af van de lokalisatie en prevalentie van het pathologische proces. De belangrijkste plaats bij het bepalen van het klinische beeld wordt ingenomen door de evaluatie van neurologische symptomen.
- Algemene cerebrale symptomen:
- Hoofdpijn;
- Verhoogde bloeddruk, hydrocefalie.
- Focale neurologische symptomen:
- Vermindering of verlies van bepaalde functies, met name motorische en sensorische stoornissen, disfunctie van de hersenzenuwen, psychische en spraakstoornissen, geheugenstoornissen, enz.;
- Epileptische aanvallen.
- Endocriene aandoeningen (wanneer de hypofyse erbij betrokken is).
Afhankelijk van het beloop kunnen aplastische meningeomen openlijk en asymptomatisch zijn. De eerste tekenen verschijnen vaak abrupt, bijvoorbeeld in de vorm van een epileptiforme of hydrocefalie-occlusieve aanval of een bloeding.
De meest voorkomende eerste verschijnselen van de ziekte:
- Pijn in het hoofd (dof, constant, neiging tot verergering);
- Braken, misselijkheid die geen verband houdt met de voedselconsumptie;
- Duizeligheid, vestibulaire stoornissen;
- Visuele beperking, spraakbeperking;
- Epileptische aanvallen;
- Verminderd gevoel, verzwakking van de ledematen, parese of verlamming (vaker eenzijdig).
Stages
Graadclassificatie van meningeomen:
- Goedaardige gezwellen, die niet in het omliggende weefsel uitzaaien.
- Kwaadaardige haarden met een hoog recidiefpercentage, relatief agressieve en snelle groei.
- Kwaadaardige haarden met een hoog recidiefpercentage, snelle groei en aantasting van omliggend hersenweefsel.
Chang-classificatie:
- T1 - neoplasma met een diameter tot 30 cm, gelokaliseerd in de cerebellaire vermis en het dak van de vierde ventrikel.
- T2 - neoplasma met een diameter groter dan 30 mm, met uitgroei in het aangrenzende weefsel of met gedeeltelijke vulling van de vierde ventrikel.
- T3A - een nidus met een diameter van meer dan 30 mm die in het gebied van de cerebrale conduit of in het foramen van Luschka en Majandie groeit en hydrocefalie veroorzaakt.
- T3B - haarden groter dan 30 mm, die doorgroeien naar de hersenstam.
- T4 - massa groter dan 30 mm met hydrocefalie veroorzaakt door blokkade van de uitstroombaan van hersen- en ruggenmergvocht en met uitlopers in de hersenstam.
- M0 - geen metastasen.
- M1-microscopie toont tumorcellen in het hersenvocht.
- M2 - metastase in de subpautijnse ruimte van de 3e en 4e ventrikel.
- M3 - metastase naar de subpautijnse ruimte van het ruggenmerg.
- M4 - metastase buiten het centrale zenuwstelsel.
Vormen
Meningeomen hebben verschillende histologische species-affiliatie. Volgens dit principe worden de volgende pathologietypen onderscheiden:
- Een meningothelioom omvat mozaïekachtige cellen met een ronde of ovale kern en een matige hoeveelheid chromatine. Het tumorstroma heeft een kleine vasculatuur en dunne bindweefselvezels die de celvelden omringen. De structuur is typisch en bestaat uit een gelaagdheid van plaveiselceltumorcellen, met een verkalkt centraal deel van de focus.
- Fibreus meningeoom wordt gekenmerkt door fibroblastachtige structuren die parallel gerangschikt en met elkaar verweven zijn in de vorm van bundels met bindweefselvezels. De kernen zijn langwerpig van vorm.
- Het overgangsneoplasma bestaat uit elementen van een fibreus en meningotheliomateus meningioom.
- Een psammomateuze neoplasie bestaat uit vele psammomen.
- Bij een angiomateuze meningeoom is er sprake van een goed ontwikkeld vaatnetwerk.
- Microcystisch meningeoom bestaat uit meerdere microscopisch kleine cysten, omgeven door tumorcellen met een stervormige configuratie.
- Secretoir meningioom is een zeldzame tumor die de neiging heeft componenten uit te scheiden die hyaline insluitsels vormen.
- Bij metaplastisch meningioom vinden er transformaties plaats van meningotheliale structuren naar structuren van andere typen.
Complicaties en gevolgen
De kans op recidief van het anaplastisch meningeoom na behandeling wordt geschat op 60-80%. De overlevingskans bedraagt doorgaans niet meer dan twee jaar.
In het postoperatieve stadium is het mogelijk dat zich complicaties van infectieuze en inflammatoire aard ontwikkelen, waaronder wondettering, meningitis, etterende processen in de schedelbeenderen, enz. Zulke complicaties vereisen intensieve antibiotische therapie, soms herhaalde chirurgische ingrepen. [ 5 ]
Bij patiënten met bloedstollingsstoornissen of een neiging tot hypertensie in de eerste postoperatieve fase kan er een inwendige bloeding ontstaan in het operatiegebied. [ 6 ]
Andere mogelijke complicaties zijn:
- Terugkeer van anaplastisch meningeoom (recidief);
- Uitbreiding van dochtertumorhaarden naar andere weefsels en organen (metastasering).
Diagnostics anaplastisch meningioom
Magnetic resonance imaging (MRI) van de hersenen wordt beschouwd als de diagnostische standaard voor verdenking op een primaire tumor van het centrale zenuwstelsel. Contrastmiddelinjectie, T1-modi zonder contrastversterking, T2-modi, T2 FLAIR, T1 met contrastversterking, in drie projecties of in SPGR-modus worden gebruikt. Deze methoden bieden de meest complete informatie over de locatie, omvang en structuur van het neoplasma, de penetratie in aangrenzende weefsels en de uitgroei in bloedvaten.
Het basiscriterium voor de uiteindelijke diagnose van anaplastisch meningeoom is de uitkomst van histologisch onderzoek. De belangrijkste kenmerken van een zeer kwaadaardig tumorproces zijn celatypie, polymorfisme, een klein cytoplasmatisch volume, hoge mitotische activiteit, dichte lokalisatie van celelementen, proliferatie van vasculair endotheel, gebieden met puntbloedingen en weefselnecrose, en een veranderde intercellulaire matrix.
In ernstige gevallen met een groot risico op sterfte kan de diagnose van anaplastisch meningioom worden gesteld op basis van klinische en radiologische informatie. [ 7 ]
Bloedonderzoek - algemeen en biochemisch - wordt voorgeschreven als onderdeel van de standaard diagnostische maatregelen. De kwaliteit van de bloedstolling, de kans op bloedarmoede en ontstekingsprocessen worden beoordeeld.
- Uitgebreid klinisch bloedonderzoek.
- Bloedbiochemie (ureum, creatinine, totaal eiwit, albumine, totaal bilirubine, lactaatdehydrogenase, alanine-aminotransferase, aspartaat-aminotransferase-waarden).
- Studie van het bloedstollingssysteem, indicatoren van hemostase.
- Bloedonderzoek naar tumormarkers (plasma AFP, choriongonadotrofine, lactaatdehydrogenase-activiteit).
Moleculair genetische analyse van IDH1-IDH2-genmutaties in het biomateriaal en beoordeling van MGMT-genmethylering worden aanbevolen.
In de meeste gevallen wordt instrumentele diagnose gesteld:
- Met een CT-scan met contrast;
- MRI met contrast.
Het voordeel van vroege diagnostische maatregelen mag niet worden onderschat, omdat anaplastisch meningioom in de loop van de tijd sneller groeit en agressiever wordt ten opzichte van naburige weefsels en structuren, wat een directe bedreiging voor het leven van de patiënt kan vormen. [ 8 ]
Differentiële diagnose
Differentiële diagnose wordt uitgevoerd bij niet-oncologische pathologieën - bijvoorbeeld bij bloedingen bij patiënten met arteriële of arterioveneuze malformaties, bij een demyeliniserend proces van het type pseudotumorose, bij ontstekingsziekten van de hersenen (abcessen, toxoplasmose, enz.).
Daarnaast worden primaire tumoruitlopers van het centrale zenuwstelsel en metastasen onderscheiden. Hiervoor wordt MRI (Magnetic Resonance Imaging) uitgevoerd, waarmee anaplastische meningeomen met een vrij hoge nauwkeurigheid kunnen worden geïdentificeerd en de onderscheidende kenmerken van andere, vergelijkbare pathologieën kunnen worden aangetoond.
Indien geïndiceerd kan de behandelend arts een CT-scan met of zonder contrastmiddel, CT-angiografie of MR-angiografie, magnetische resonantietractografie, functionele MRI met evaluatie van de motorische gebieden en spraakcentra, CT-perfusie of MR-perfusie aanvragen.
Met wie kun je contact opnemen?
Behandeling anaplastisch meningioom
Het meningeoom is niet altijd zo gelokaliseerd dat het gemakkelijk te verwijderen is. Een operatie is alleen geïndiceerd wanneer er geen of een minimaal risico is op schade aan belangrijke functionele hersengebieden.
Anaplastisch meningeoom wordt beschouwd als een kwaadaardige tumor, hoewel het zowel de eigenschappen van kwaadaardige als goedaardige tumoren heeft. Het pathologische proces kan hersenweefsel vernietigen, samendrukken en metastasen verspreiden. Om de ziekte te stoppen, worden voornamelijk chirurgische (optimale) en radiochirurgische technieken gebruikt.
Als contra-indicatie voor een operatie geldt:
- De gevorderde leeftijd van de patiënt;
- Gebrek aan adequate toegang tot het nidus (bijvoorbeeld door de groei ervan in de sinus cavernosus).
Klassieke radiotherapie wordt praktisch niet toegepast vanwege de ineffectiviteit en de grote kans op schade aan gezonde delen van de hersenen en het ruggenmerg. In sommige gevallen wordt radiotherapie voorgeschreven in combinatie met chirurgische resectie om de pathologische focus in inoperabele gebieden te vernietigen of om het risico op reformatie van meningiomen te verminderen.
Radiotherapie met het CyberKnife-apparaat wordt beschouwd als een van de modernste en minst traumatische methoden om meningeomen met een diameter tot 35-40 mm te elimineren. Een stroom ioniserende straling wordt op de focus gericht. Het risico op schade aan omliggende structuren wordt geminimaliseerd.
Dankzij de CyberKnife kunnen anaplastische meningeomen veilig worden verwijderd. De procedure wordt poliklinisch uitgevoerd en er is geen ziekenhuisopname nodig. [ 9 ]
Medicijnen
Het is mogelijk om chemotherapie toe te dienen volgens geïndividualiseerde regimes, [ 10 ] bijvoorbeeld:
- Lomustine 100 mg/m², Vincristine 1,5 mg/m², Procarbazine 70 mg/m²;
- Temozolomide als onderdeel van chemoradiotherapie 75-100 mg/m²;
- Temozolomide 150-200 mg/m², Cisplatine of Carboplatine 80 mg/m².
De volgende regimes zijn geïndiceerd bij recidiverend anaplastisch meningeoom:
- Bevacizumab 5-10 mg/kg (dag 1, 15) en Irinotecan 125-200 mg/m² (dag 1, 15) elke 28 dagen;
- Bevacizumab 5-10 mg/kg (dag 1, 15, 29) en Lomustine 90 mg/m² (dag 1) elke 6 weken;
- Bevacizumab 5-10 mg/kg (dag 1, 15) en Lomustine 40 mg/m² (dag 1, 8, 15, 22) elke zes weken;
- Bevacizumab 5-10 mg/kg (dag 1, 15) elke 28 dagen.
Complementaire therapie wordt ook op individuele basis voorgeschreven:
- Corticosteroïden zoals dexamethason en prednisolon, in doseringen afhankelijk van de ernst van de symptomen (de minimale effectieve dosering wordt voorgeschreven). Na afname van de symptomen wordt de dosis geleidelijk verlaagd tot volledige stopzetting. Gelijktijdig met corticosteroïden wordt het gebruik van maagbeschermers (protonpompremmers) aanbevolen. Bij ernstig oedeem worden bovendien saluretica (furosemide) of osmotische diuretica (mannitol) voorgeschreven.
- Bij epileptische aanvallen of epileptische manifestaties worden anticonvulsiva gebruikt. Valproïnezuur, levetiracetam en lamotrigine hebben de voorkeur. Het gebruik van carbamazepine, fenobarbital en fenytoïne tegen de achtergrond van chemotherapie is zeer ongewenst. Om epileptische aanvallen te voorkomen, worden anticonvulsiva niet gebruikt. De therapieën worden individueel afgestemd.
- Pijnstillers worden voorgeschreven aan patiënten met letsels aan het ruggenmerg of de wervelkolom. Het zijn voornamelijk narcotische pijnstillers zoals fentanyl en trimeperidine in individuele doses.
- Correctie van de hemostase omvat de perioperatieve toediening van laagmoleculaire heparines, zoals calciumnadroparine, natriumdalteparine, enz., ter voorkoming van longembolie. Patiënten die constant bloedverdunnende medicijnen gebruiken (aspirine, clopidogrel), dienen deze uiterlijk een week voor de ingreep te vervangen door laagmoleculaire heparines. Vervolgens dient de behandeling een dag voor de operatie te worden gestaakt en 48 uur na de operatie te worden hervat.
Chirurgische behandeling
De operatie wordt uitgevoerd om de grootte van het anaplastisch meningeoom zoveel mogelijk te verkleinen, de intracraniële druk te normaliseren, de neurologische insufficiëntie te verminderen en het benodigde morfologische materiaal te verwijderen.
Voor de resectie en biopsie wordt de patiënt opgenomen op een speciale neurochirurgische afdeling of kliniek, waar specialisten ervaring hebben met het uitvoeren van neuro-oncologische interventies. Tijdens de operatie moeten microchirurgische technieken en een operatiemicroscoop worden gebruikt.
Operatieve toegang wordt verkregen door middel van bot-plastische trepanatie in de projectie van de beoogde chirurgische manipulaties.
Als de operatie anatomisch dicht bij de motorische gebieden van de cortex of de motorische banen, of in de buurt van de kernen van de hersenzenuwen, moet worden uitgevoerd, wordt er bovendien intraoperatieve elektrofysiologische bewaking uitgevoerd.
Het is optimaal om binnen twee weken na de diagnose in te grijpen. Indien dit niet gebeurt, kan dit leiden tot een snelle verslechtering van het neurologische beeld en de ontwikkeling van een levensbedreigende aandoening.
Om de operatie zo compleet en radicaal mogelijk te maken, worden neuronavigatiesuites en intraoperatieve fluorescentienavigatie met 5-aminolevuleenzuur gebruikt.
In de postoperatieve fase ondergaan patiënten bij wie een anaplastisch meningeoom is verwijderd, contrastversterkte computertomografie of magnetische resonantiebeeldvorming (MRI).
Het voorkomen
Uitlokkende factoren voor de ontwikkeling en preventiemethoden van kanker van het centrale zenuwstelsel worden voortdurend bestudeerd door wetenschappers over de hele wereld. Helaas krijgen jaarlijks duizenden mensen de diagnose meningeomen, en de meeste van deze patiënten kunnen niet genezen van de ziekte vanwege late detectie.
Het is belangrijk dat absoluut alle risicofactoren worden bekeken binnen het kader van de individuele verantwoordelijkheid voor de eigen gezondheid. Aanbevelingen over voeding, het afleren van slechte gewoonten en de noodzaak tot bescherming tegen ultraviolette straling worden door de meeste mensen vaak genegeerd. Ondanks de aanwezigheid van bewezen en logische onderliggende oorzaken, blijven mensen alcohol misbruiken, roken en producten consumeren die veel kankerverwekkende stoffen bevatten.
De eenvoudigste en meest betaalbare preventie is allereerst een gezonde levensstijl. Dit vermindert de kans op anaplastisch meningeoom en andere kwaadaardige tumoren aanzienlijk en vergroot de overlevingskansen van veel patiënten die al tegen de ziekte vechten.
Prognose
De uitkomst van de pathologie hangt af van de locatie en prevalentie van anaplastisch meningeomen. In veel gevallen komen neoplasmata terug en metastaseren ze, wat de prognose van de ziekte aanzienlijk verslechtert. Het is niet altijd mogelijk om dergelijke tumoruitlopers volledig te verwijderen. Zo zijn er bijvoorbeeld problemen met de resectie van meningeomen van de falx tentoriale hoek, de schedelbasis en de sinus cavernosus, petroclivale haarden en multipele massa's.
Vanwege de diverse en onduidelijke symptomatologie is een tijdige diagnose vaak moeilijk. Bij oudere patiënten wordt het beeld van een tumorproces soms verward met leeftijdsgebonden hersenveranderingen, wat de situatie verder verergert. Het is zeer belangrijk om het probleem tijdig te vermoeden en de patiënt door te verwijzen voor diagnostische maatregelen - magnetische resonantie en computertomografie, evenals voor overleg met een oncoloog, neurochirurg of radiotherapeut.
Gemiddeld komt anaplastisch meningeoom in 70% van de gevallen terug. De overlevingsduur is beperkt tot 1-2 jaar.

