Medisch expert van het artikel
Nieuwe publicaties
Fenylpyruvine oligofrenie of fenylketonurie
Laatst beoordeeld: 05.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Volgens de statistieken wordt bij één op de 10.000 tot 15.000 pasgeborenen een genetisch bepaalde neurocognitieve pathologie vastgesteld: fenylpyruvaat-oligofrenie, die zich ontwikkelt als gevolg van een aangeboren stoornis in de stofwisseling van het essentiële aminozuur fenylalanine.
De ziekte werd voor het eerst in de jaren 30 in Noorwegen vastgesteld door arts Ivar Foelling, die het hyperfenylalaninemie noemde. Tegenwoordig wordt de aandoening algemeen fenylketonurie genoemd, met ICD 10-code E70.0.
Oorzaken van fenylpyruvische oligofrenie
Genetische oorzaken van fenylpyruvaat-oligofrenie zijn recessieve overerving door een kind van ouders die drager zijn van twee gemuteerde allelen van het enzym fenylalaninehydroxylase (fenylalanine-4-monooxygenase). Hierdoor mist het kind dit enzym, dat nodig is voor de afbraak van fenylalanine (proteïnogeen α-amino-β-fenylpropionzuur) tot tyrosine [2-amino-3-(4-hydroxyfenyl)propionzuur].
Genetici hebben vastgesteld dat de pathogenese van deze ziekte gepaard gaat met meer dan 500 verschillende homozygote of heterozygote structurele mutaties op chromosoom 12 – in de genen van het leverenzym fenylalaninehydroxylase 12q23.2 of 12q22-q24.1. De genmutatie leidt ertoe dat de concentratie van dit enzym, dat nodig is voor de oxidatie van fenylalanine in eiwitrijk voedsel, vier keer of meer afneemt.
Dit leidt enerzijds tot een ophoping van overtollig fenylalanine in het bloed, wat giftig is voor de hersenontwikkeling. In dit geval wordt fenylalanine, dat niet kan worden omgezet in tyrosine, door deaminering afgebroken tot fenylpyrodruivenzuur (2-oxo-3-fenylpropionzuur of fenylpyruvaat). Dit zuur wordt op zijn beurt omgezet in fenylazijnzuur (fenylacetaat) en fenylmelkzuur (fenyllactaat), die een negatief effect hebben op de cellen van de hersenen en het centrale zenuwstelsel.
Aan de andere kant leiden de primaire oorzaken van fenylpyruvaat-oligofrenie (aangeboren tekort aan fenylalaninehydroxylase en het gevolg - teveel fenylalanine) tot een daling van de niveaus van andere aminozuren in de hersenen (tryptofaan, threonine, methionine, valine, isoleucine, leucine), wat het proces van biosynthese van neurotransmitters die zenuwimpulsen overbrengen - dopamine en noradrenaline - volledig verstoort en leidt tot een progressieve aantasting van de geestelijke en lichamelijke ontwikkeling bij kinderen.
Symptomen van fenylpyruvische oligofrenie
Een teveel aan fenylalanine in het lichaam uit zich bij zuigelingen. De eerste tekenen hiervan zijn: lethargie en slaperigheid, problemen met zuigen, stuiptrekkingen, braken, eczeemachtige laesies van de opperhuid en een muffe (muisachtige) geur van het lichaam, de urine en de adem (vanwege het verhoogde gehalte aan fenylacetaat, dat wordt geoxideerd tot fenylketonen).
De volgende typische symptomen van fenylpyruvaat-oligofrenie worden waargenomen: groeiachterstand, spierhyperkinesie, tremor of verminderde spierspanning, psychotische aanvallen gepaard gaande met ongemotiveerde prikkelbaarheid en woede, verminderde intellectuele vermogens of mentale retardatie.
Kinderen met fenylketonurie hebben ook last van hypopigmentatie: een aanzienlijk lichtere en dunnere huid, haarkleur en oogkleur vergeleken met hun ouders. De directe oorzaak van dit symptoom is een tekort aan tyrosine, dat, wanneer het in de melanocyten van de opperhuid wordt geoxideerd, het pigment melanine vormt.
Zoals specialisten in de kinderpsychiatrie opmerken, hangt het klinische beeld van fenylpyruvaatoligofrenie af van de mate van beschadiging van hersencellen, en kan een baby met deze aandoening gedurende de eerste levensmaanden normaal lijken. Als de ziekte niet direct na de geboorte wordt ontdekt en het kind lange tijd geen behandeling krijgt, volgen de gevolgen: onherstelbare hersenschade en de complicaties ervan in de vorm van ernstige of ernstige verstandelijke beperking (imbeciliteit of idiotie).
En dan kunnen de volgende symptomen van fenylpyruvaat-oligofrenie optreden: een kleine lichaamslengte, schedel- en gezichtsafwijkingen (microcefalie, uitstekende bovenkaak, ver uit elkaar staande tanden, verstoorde ontwikkeling van het tandglazuur), verhoogde spierspanning en peesreflexen, hyperactiviteit, slechte coördinatie van bewegingen en onhandige loop, verhoogde prikkelbaarheid en andere gedrags- en neurologische problemen tot en met psychische stoornissen.
Diagnose van fenylpyruvische oligofrenie
Vroege diagnose van fenylpyruvaat-oligofrenie en snelle behandeling zijn van groot belang. Daarmee wordt het risico op het ontwikkelen van mentale retardatie teruggebracht van 80-90% naar 6-8% (volgens CLIMB – National Information Centre for Metabolic Diseases, Verenigd Koninkrijk).
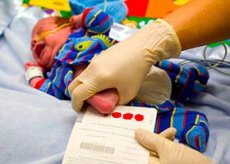
Om dit doel te bereiken, moet neonatale screening op fenylketonurie worden uitgevoerd bij zuigelingen op de derde tot vierde dag na de geboorte (in uitzonderlijke gevallen tussen de vijfde en achtste dag) met behulp van een microbiologische bloedtest op het fenylalaninegehalte, de zogenaamde Guthrie-test.
Biochemische urinetests op fenylpyruvaat tonen ook fenylketonurie aan bij pasgeborenen, maar deze test mag pas 10-12 dagen na de geboorte worden uitgevoerd. De internationale diagnostische standaard is daarom het bepalen van de concentratie fenylalanine in het bloedplasma.
Moderne instrumentele diagnostiek, gebaseerd op nieuwe technologieën zoals tandemmassaspectrometrie, stelt ons in staat om veel aangeboren stofwisselingsstoornissen op te sporen die leiden tot een verstandelijke beperking. Dit maakt differentiële diagnostiek mogelijk van genetische stofwisselingspathologieën, waaronder: galactosemie, ketonurie (stoornissen in de leucine-, isoleucine- en valinestofwisseling), homocystinurie, glutaarzuuracidurie, isovaleriaanzuuracidemie, sikkelcelanemie, tyrosinemie, congenitale hypothyreoïdie, enz.
Met wie kun je contact opnemen?
Behandeling van fenylpyruvische oligofrenie
Dieettherapie is vrijwel de enige effectieve behandeling voor fenylpyruvaatoligofrenie, waardoor de hersenen zich normaal kunnen ontwikkelen. Maar bij de start van de behandeling van kinderen ouder dan drie of vier jaar zal dieettherapie de reeds ontstane symptomen van de pathologie niet wegnemen.
Baby's met een fenylalaninehydroxylasedeficiëntie mogen geen borstvoeding krijgen. Voor hen zijn er speciale formules zonder fenylalanine: Lofenalac, Afenilak, Aminogran, Milupa pku1 (pku2 en pku3), Periflex Infanta, XP Maxamum.
Het dieet sluit de consumptie uit van vlees, vis, gevogelte, melk, eieren, kaas, kwark, ijs, peulvruchten, noten en vele andere eiwitrijke producten. Caseïnehydrolysaat wordt gebruikt als voedselvervanger voor verboden producten om de eiwitbalans in het lichaam te behouden - een mengsel van aminozuren zonder fenylalanine, gewonnen uit melkeiwit (Berlofan of Ipofenaat).
Vroeger dachten artsen dat het gebruik van mengsels zonder fenylalanine en het volgen van een speciaal dieet tot wel 10 jaar zou moeten duren (dat wil zeggen tot het einde van de myelinisatieprocessen in de hersenen), maar nu weten we dat het stoppen van de behandeling kan leiden tot een heftiger beloop van fenylpyruvaat-oligofrenie en onomkeerbare gevolgen. Patiënten die zich aan dieetbeperkingen houden, vertonen daarentegen geen symptomen.
Tegenwoordig wordt voor de behandeling van fenylpyruvaatoligofrenie (fenylketonurie) het medicijn Kuvan gebruikt, gebaseerd op sapropterinedihydrochloride - een synthetische vervanger van de cofactor van het enzym fenylalaninehydroxylase tetrahydrobiopterine (BH4). Kuvan-tabletten, opgelost in water, worden eenmaal daags ingenomen - 's ochtends tijdens de maaltijd. De dosis wordt individueel berekend - op basis van het lichaamsgewicht van de patiënt (10 mg per kilogram). Bijwerkingen van het medicijn zijn onder andere een waterige neusafscheiding, een verstopte neus, hoofdpijn, pijn in het strottenhoofd, braken, diarree en soms buikpijn. Het gebruik van dit medicijn heft het antifenylalaninedieet niet op. In de gebruiksaanwijzing staat dat het gebruik ervan bij kinderen jonger dan vier jaar niet is onderzocht.
In dit geval wordt de behandeling van fenylpyruvaat-oligofrenie uitgevoerd onder voortdurende controle van het fenylalaninegehalte in het bloed.
Fenylpyruvaatoligofrenie of fenylketonurie is een erfelijke ziekte die niet kan worden voorkomen. Bij een kinderwens is preventie echter mogelijk: een enzymtest in het bloed en een genetische test om te bepalen of aanstaande ouders drager zijn van het gemuteerde gen. Bloedtesten op fenylalanine kunnen ook tijdens de zwangerschap worden uitgevoerd.
Zoals het Journal of Inherited Metabolic Disease schrijft: "De prognose voor patiënten met deze pathologie is, indien onbehandeld, een maximale levensverwachting van 30 jaar in de status van een gehandicapte persoon met ernstige hersenfunctiestoornissen (aangezien het fenylalaninegehalte in het bloed in de loop van de tijd zal toenemen), en met behandeling - tot op hoge leeftijd, met een hogere opleiding en een succesvolle carrière."


 [
[