Medisch expert van het artikel
Nieuwe publicaties
Fibroelastose
Laatst beoordeeld: 05.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
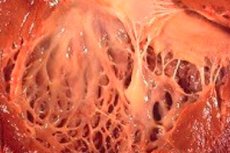
In de geneeskunde verwijst de term "fibro-elastose" naar veranderingen in het bindweefsel van het lichaam dat het oppervlak van inwendige organen en bloedvaten bedekt, veroorzaakt door een verstoring van de groei van elastische vezels. Tegelijkertijd wordt verdikking van de wanden van organen en hun structuren waargenomen, wat noodzakelijkerwijs de werking van vitale lichaamssystemen beïnvloedt, met name het cardiovasculaire en respiratoire systeem. Dit leidt op zijn beurt tot een verslechtering van het welzijn van de patiënt, met name tijdens fysieke inspanning, wat de kwaliteit en duur van het leven beïnvloedt.
Epidemiologie
Over het algemeen kunnen aandoeningen die gepaard gaan met veranderingen in het bindweefsel, resulterend in verdikking van de membranen en wanden van inwendige organen, worden onderverdeeld in twee groepen: cardiale fibro-elastose en pulmonale fibro-elastose. Hartpathologie kan zowel aangeboren als verworven zijn; bij de pulmonale vorm van de ziekte spreken we van een verworven aandoening.
Pulmonale fibro-elastose begint zich te ontwikkelen op middelbare leeftijd (dichter bij 55-57 jaar), hoewel in de helft van de gevallen de oorsprong van de ziekte in de kindertijd moet worden gezocht. Een "lichte" periode is kenmerkend, wanneer de symptomen van de ziekte afwezig zijn. Tegelijkertijd heeft de ziekte geen gendervoorkeuren en kan ze zowel vrouwen als mannen evenzeer treffen. Deze vrij zeldzame pathologie wordt gekenmerkt door veranderingen in de weefsels van het pleura en parenchym (functionele cellen) van de long, voornamelijk in de bovenkwab van de long. Omdat de etiologie en pathogenese van de ziekte onduidelijk blijven, wordt de ziekte geclassificeerd als een idiopathische pathologie. Volgens medische terminologie wordt het "pleuroparenchymateuze fibro-elastose" genoemd. [ 1 ]
Cardiale fibro-elastose is een algemene term voor een aandoening van de hartvliezen, gekenmerkt door verdikking en verminderde functionaliteit. Aangeboren vormen van de aandoening worden gekenmerkt door een diffuse (wijdverspreide) verdikking van het binnenste hartvlies. Dit is een dun bindweefsel dat de hartholte (de hartdelen) bekleedt en de hartkleppen vormt.
Bij volwassen patiënten wordt doorgaans de diagnose focale vorm van de ziekte gesteld, waarbij de binnenkant van het hart bedekt lijkt te zijn met plekken van steviger en dikker weefsel (dit kunnen niet alleen overwoekerde vezels zijn, maar ook trombotische massa's).
Bij de helft van de gevallen van cardiale fibro-elastose wordt niet alleen de wand van het orgaan dikker, maar ook de hartkleppen (de bicuspidale mitralisklep tussen atrium en ventrikel (gelijknamig), de tricuspidale aortaklep tussen linkerventrikel en aorta, en de pulmonalisklep tussen rechterventrikel en longslagader). Dit kan op zijn beurt de werking van de hartkleppen verstoren en leiden tot vernauwing van de slagaderopening, die al klein is in vergelijking met andere hartholtes.
In medische terminologie wordt endocardiale fibro-elastose endocardiale fibro-elastose genoemd (prenatale fibro-elastose, endocardiale sclerose, foetale endocarditis, enz.). Maar heel vaak kan ook de middelste spierlaag van het hartmembraan bij het proces betrokken zijn. [ 2 ]
Afwijkingen in de structuur van het myocard (de spierlaag van het hart, bestaande uit cardiomyocyten), genmutaties en ernstige infectieuze processen kunnen een veelvoorkomende vorm van fibro-elastose veroorzaken, waarbij niet alleen het endocard, maar ook het myocard bij dit proces betrokken is. Dysplastische processen in het endocard, veroorzaakt door verschillende oorzaken, treden meestal op aan de contactgrens met het spiermembraan, waardoor de contractiliteit van deze laag verstoord raakt. In sommige gevallen is er zelfs sprake van ingroei van de binnenste laag in het myocard, waarbij cardiomyocyten worden vervangen door fibroblasten en vezels, wat de geleiding van zenuwimpulsen en het ritme van het hart beïnvloedt.
Door de verdikte hartspier worden de bloedvaten in de dikte van het hartspiervlies samengedrukt. Hierdoor wordt de voeding van de hartspier verstoord (myocardischemie), wat tot necrose van het hartspierweefsel kan leiden.
Endocardiale fibro-elastose met schade aan de hartspier wordt subendocardiale of endomyocardiale fibro-elastose genoemd.
Volgens de statistieken wordt bij de meeste gevallen van deze zeldzame ziekte (slechts 0,007% van het totale aantal pasgeborenen) fibro-elastose van de linkerhartkamer vastgesteld, hoewel het proces zich in sommige gevallen ook uitbreidt naar de rechterhartkamer en de boezems, inclusief de kleppen die ze scheiden.
Cardiale fibro-elastose gaat vaak gepaard met schade aan grote kransslagaders, die eveneens met bindweefsel bedekt zijn. Op volwassen leeftijd treedt het vaak op tegen de achtergrond van progressieve vasculaire atherosclerose.
De ziekte wordt vaker vastgesteld in tropische Afrikaanse landen, onder bevolkingsgroepen met een lage levensstandaard. Dit wordt veroorzaakt door slechte voeding, frequente infecties en de consumptie van bepaalde voedingsmiddelen en planten.
Endocardiale verdikking wordt ook waargenomen in het laatste stadium van fibroplastische endocarditis van Löffler, een aandoening die vooral mannen van middelbare leeftijd treft. De pathogenese van deze ziekte wordt ook geassocieerd met infectieuze agentia die de ontwikkeling van ernstige eosinofilie veroorzaken, een aandoening die meer kenmerkend is voor inwendige parasitaire infecties. In dit geval beginnen de lichaamsweefsels (voornamelijk de hartspier en de hersenen) zuurstofgebrek (hypoxie) te ervaren. Ondanks de gelijkenissen in de symptomen van cardiale fibro-elastose en fibroplastische endocarditis van Löffler, beschouwen artsen ze als twee totaal verschillende aandoeningen.
Oorzaken fibroelastose
Fibro-elastose verwijst naar veranderingen in het bindweefsel van vitale organen: het hart en de longen. Deze veranderingen gaan gepaard met een verstoring van de orgaanfunctie en uiten zich in het uiterlijk en de conditie van de patiënt. Artsen zijn al tientallen jaren bekend met de ziekte. Fibro-elastose van de binnenwand van het hart (endocard) werd al begin 18e eeuw beschreven en vergelijkbare veranderingen in de longen begonnen 2,5 eeuw later te worden besproken. Artsen hebben echter nog geen definitieve overeenstemming bereikt over de oorzaken van de pathologische proliferatie van bindweefsel.
Het blijft onduidelijk wat precies de oorzaak is van de verstoring van de groei en ontwikkeling van bindweefsel. Maar wetenschappers identificeren bepaalde risicofactoren voor dergelijke veranderingen en beschouwen deze als mogelijke (maar niet definitieve) oorzaken van de ziekte.
In de pathogenese van pulmonale fibroelastose, een ziekte die wordt beschouwd als een aandoening van volwassenen, is een speciale rol weggelegd voor recidiverende infectieuze laesies van het orgaan, die bij de helft van de patiënten voorkomen. Infecties veroorzaken ontstekingen van het longweefsel en het borstvlies, en langdurige ontstekingen maken de patiënt vatbaarder voor vezelachtige transformatie.
Bij sommige patiënten komt fibro-elastose in de familie voor, wat wijst op een erfelijke aanleg. Er zijn niet-specifieke auto-antilichamen in hun lichaam aangetroffen, die langdurige ontstekingsprocessen van onbekende oorzaak veroorzaken.
Er bestaat een mening dat vezelachtige veranderingen in longweefsel kunnen worden veroorzaakt door gastro-oesofageale refluxziekte. Hoewel dit verband waarschijnlijk indirect is, wordt ook aangenomen dat het risico op fibroelastose hoger is bij mensen met hart- en vaatziekten of longtrombose.
Pulmonale fibroelastose op jonge en adolescente leeftijd kan aan de zwangerschap doen denken. Meestal blijft de ziekte ongeveer 10 jaar of langer verborgen, maar kan zich ook eerder manifesteren, mogelijk als gevolg van de verhoogde belasting van het lichaam van de aanstaande moeder en hormonale veranderingen. Een exacte verklaring hiervoor is er echter nog niet. Desondanks werd een vergelijkbaar beeld van het beloop van de ziekte waargenomen bij 30% van de onderzochte patiënten in de vruchtbare leeftijd.
Zwangerschap op zich kan de ziekte niet veroorzaken, maar het kan de ontwikkeling van de gebeurtenissen versnellen, wat erg triest is, omdat het sterftecijfer van de ziekte erg hoog is en de levensverwachting bij fibroelastose kort is.
In de meeste gevallen kan cardiale fibroelastose worden toegeschreven aan kinderziekten. Aangeboren afwijkingen worden al in de prenatale periode vastgesteld bij een foetus van 4-7 maanden oud, maar de diagnose kan pas na de geboorte van het kind worden bevestigd. Verschillende mogelijke negatieve factoren worden in aanmerking genomen bij de pathogenese van deze vorm van de ziekte: infectie- en ontstekingsziekten van de moeder die worden overgedragen op de foetus, afwijkingen in de ontwikkeling van de hartvliezen, een verminderde bloedtoevoer naar het hartweefsel, genetische mutaties en zuurstoftekort.
Men gelooft dat virussen van alle infecties de grootste pathogene bijdrage leveren aan de ontwikkeling van cardiale fibroelastose, omdat ze zich nestelen in de lichaamscellen, deze vernietigen en de eigenschappen van weefsels veranderen. Het ongevormde immuunsysteem van de foetus kan hem geen bescherming bieden tegen deze pathogenen, in tegenstelling tot de immuniteit van de aanstaande moeder. Deze laatste ondervindt mogelijk geen gevolgen van een virale infectie, terwijl een intra-uteriene infectie bij de foetus verschillende afwijkingen kan veroorzaken.
Sommige wetenschappers zijn van mening dat een infectie die de foetus tot de leeftijd van 7 maanden treft, een doorslaggevende rol speelt in de pathogenese van de infectieuze vorm van fibro-elastose. Later kan deze alleen nog ontstekingsziekten van het hart (myocarditis, endocarditis) veroorzaken.
Afwijkingen in de ontwikkeling van de hartmembranen en -kleppen kunnen zowel het gevolg zijn van een ontstekingsproces als van onvoldoende auto-immuunreacties. Als gevolg hiervan beginnen de cellen van het immuunsysteem de eigen cellen van het lichaam aan te vallen.
Genmutaties veroorzaken een abnormale ontwikkeling van bindweefsel, omdat genen informatie bevatten over de structuur en het gedrag van eiwitstructuren (met name collageen- en elastine-eiwitten).
Hypoxie en ischemie van het hartweefsel kunnen een gevolg zijn van een abnormale hartontwikkeling. In dit geval spreken we van secundaire fibro-elastose, veroorzaakt door aangeboren hartafwijkingen (CHD). Hieronder vallen afwijkingen die obstructie (verminderde doorgankelijkheid van het hart en de bloedvaten) veroorzaken:
- stenose of vernauwing van de aorta nabij de klep,
- coarctatie of segmentale vernauwing van de aorta op de kruising van de boog en het afdalende deel,
- atresie of het ontbreken van een natuurlijke opening in de aorta,
- onderontwikkeling van het hartweefsel (meestal de linkerkamer, minder vaak de rechterkamer en de boezems), waardoor de pompfunctie van het hart wordt beïnvloed.
Er bestaat een mening dat toxicose tijdens de zwangerschap ook een predisponerende factor kan zijn voor fibroelastose bij de foetus.
In de postnatale periode kan de ontwikkeling van cardiale fibroelastose worden bevorderd door infectieuze en inflammatoire aandoeningen van de orgaanmembranen, hemodynamische stoornissen als gevolg van verwondingen, vasculaire trombo-embolie, myocardbloedingen en stofwisselingsstoornissen (verhoogde fibrinevorming, stoornissen in de eiwit- en ijzerstofwisseling: amyloïdose, hemochromatose). Dezelfde oorzaken veroorzaken de ontwikkeling van de ziekte bij volwassenen.
Pathogenese
Bindweefsel is een speciaal weefsel van het menselijk lichaam dat deel uitmaakt van bijna alle organen, maar niet actief deelneemt aan hun functies. Bindweefsel wordt beschouwd als een ondersteunende en beschermende functie. Het vormt een soort skelet (geraamte, stroma) en beperkt de functionele cellen van het orgaan, waardoor het de uiteindelijke vorm en grootte ervan bepaalt. Met voldoende sterkte beschermt bindweefsel de orgaancellen ook tegen vernietiging en beschadiging, voorkomt het het binnendringen van ziekteverwekkers en absorbeert het met behulp van speciale macrofaagcellen verouderde structuren: afgestorven weefselcellen, vreemde eiwitten, afvalstoffen uit het bloed, enz.
Dit weefsel kan hulpweefsel worden genoemd, omdat het geen cellulaire elementen bevat die de functionaliteit van een of ander orgaan garanderen. Niettemin speelt het een vrij belangrijke rol in het leven van het lichaam. Als onderdeel van de membranen van bloedvaten zorgt bindweefsel voor de veiligheid en functionaliteit van deze structuren, waardoor de voeding en ademhaling (trofie) van de omliggende weefsels van de interne omgeving van het lichaam plaatsvinden.
Er zijn verschillende soorten bindweefsel. Het membraan dat de inwendige organen bedekt, wordt los bindweefsel genoemd. Het is een halfvloeibare, kleurloze substantie met golvende collageenvezels en rechte elastinevezels, waartussen verschillende soorten cellen willekeurig verspreid liggen. Sommige van deze cellen (fibroblasten) zijn verantwoordelijk voor de vorming van vezelachtige structuren, andere (endotheliocyten en mestcellen) vormen een doorschijnende matrix van bindweefsel en produceren speciale stoffen (heparine, histamine), weer andere (macrofagen) zorgen voor fagocytose, enz.
Het tweede type vezelig weefsel is dicht bindweefsel, dat niet veel individuele cellen bevat en dat op zijn beurt verdeeld is in wit en geel. Wit weefsel bestaat uit dicht opeengepakte collageenvezels (ligamenten, pezen, periost), en geel weefsel bestaat uit chaotisch verweven elastinevezels met insluitsels van fibroblasten (onderdeel van ligamenten, membranen van bloedvaten, longen).
Bindweefsel omvat ook: bloed, vet, bot en kraakbeen, maar daarin zijn we nog niet geïnteresseerd, omdat we met fibro-elastose veranderingen in vezelstructuren bedoelen. Elastische en veerkrachtige vezels bevinden zich alleen in los en dicht bindweefsel.
De synthese van fibroblasten en de vorming van bindweefselvezels daaruit wordt gereguleerd op hersenniveau. Dit zorgt voor de bestendigheid van de eigenschappen ervan (sterkte, elasticiteit, dikte). Indien, om een of andere pathologische reden, de synthese en ontwikkeling van hulpweefsel verstoord raakt (het aantal fibroblasten neemt toe, hun "gedrag" verandert), treedt er een proliferatie op van sterke collageenvezels of een verandering in de groei van elastische vezels (ze blijven kort, draaien), wat leidt tot een verandering in de eigenschappen van het orgaanmembraan en enkele interne structuren die bedekt zijn met bindweefsel. Ze worden dikker dan nodig, worden dichter, sterker en onelastischer en lijken op vezelig weefsel in ligamenten en pezen, wat een grote inspanning vereist om uit te rekken.
Dit soort weefsel rekt niet goed uit, waardoor de bewegingen van het orgaan beperkt worden (automatische ritmische bewegingen van het hart en de bloedvaten, veranderingen in de grootte van de longen bij het in- en uitademen). Hierdoor wordt de bloedtoevoer naar en de ademhalingsorganen verstoord, wat leidt tot zuurstoftekort.
Feit is dat de bloedtoevoer naar het lichaam plaatsvindt dankzij het hart, dat als pomp werkt, en twee bloedsomloopcircuits. De longcirculatie is verantwoordelijk voor de bloedtoevoer en gasuitwisseling in de longen, van waaruit zuurstof via de bloedstroom naar het hart wordt getransporteerd, en van daaruit naar de grote bloedsomloop en door het hele lichaam wordt verspreid, wat zorgt voor de ademhaling van organen en weefsels.
Het elastische membraan, dat de samentrekking van de hartspier beperkt, vermindert de functionaliteit van het hart, dat daardoor minder actief bloed en daarmee zuurstof pompt. Bij fibro-elastose van de longen is de ventilatie (osigenatie) verstoord; het is duidelijk dat er minder zuurstof in het bloed komt, wat, zelfs bij een normale hartfunctie, zal bijdragen aan zuurstofgebrek (hypoxie) van weefsels en organen. [ 3 ]
Symptomen fibroelastose
Cardiale en pulmonale fibroelastose zijn twee aandoeningen die gekenmerkt worden door een stoornis in de vezelsynthese in bindweefsel. Ze komen op verschillende plaatsen voor, maar zijn beide potentieel levensbedreigend, omdat ze gepaard gaan met progressief of ernstig hart- en ademhalingsfalen.
Pulmonale fibro-elastose is een zeldzame vorm van interstitiële longziekte van dit belangrijke orgaan van de luchtwegen. Deze aandoening omvat chronische pathologieën van het longparenchym met schade aan de alveolaire wanden (ontsteking, verstoring van hun structuur en structuur), de binnenbekleding van de longcapillairen, enz. Fibro-elastose wordt vaak beschouwd als een bijzondere, zeldzame vorm van progressieve pneumonie met een neiging tot vezelachtige veranderingen in de long- en pleuraweefsels.
Het is vrijwel onmogelijk om de ziekte in het begin op te sporen, omdat deze zich mogelijk pas na ongeveer 10 jaar weer voordoet. Deze periode wordt de clear interval genoemd. Het begin van pathologische veranderingen die nog geen invloed hebben op het longvolume en de gasuitwisseling, kan bij toeval worden vastgesteld tijdens een gedetailleerd longonderzoek in verband met een andere aandoening van de luchtwegen of een verwonding.
De ziekte wordt gekenmerkt door een langzame progressie van de symptomen, waardoor de eerste manifestaties van de ziekte aanzienlijk later dan het begin kunnen optreden. De symptomen verergeren geleidelijk.
De eerste tekenen van de ziekte waar u op moet letten, zijn hoesten en toenemende kortademigheid. Dergelijke symptomen zijn vaak een gevolg van een eerdere luchtwegaandoening, waardoor ze langdurig kunnen worden geassocieerd met een verkoudheid en de gevolgen daarvan. Kortademigheid wordt vaak gezien als een hartaandoening of leeftijdsgebonden veranderingen. De ziekte wordt immers vastgesteld bij mensen die de ouderdom naderen.
Zowel patiënten als artsen kunnen fouten maken bij het onderzoek, wat leidt tot late detectie van een gevaarlijke ziekte. Het is de moeite waard om aandacht te besteden aan de hoest, die bij fibro-elastose onproductief is, maar niet wordt gestimuleerd door mucolytica en expectorantia, maar wel wordt gestopt door hoestonderdrukkers. Een dergelijke aanhoudende hoest is een kenmerkend symptoom van pulmonale fibro-elastose.
Kortademigheid wordt veroorzaakt door progressief ademhalingsfalen als gevolg van verdikking van de alveolaire wanden en het longvlies, een afname van het volume en het aantal alveolaire holten in de long (het parenchym van het orgaan is op een röntgenfoto zichtbaar als een honingraat). Het symptoom verergert onder invloed van fysieke inspanning, eerst aanzienlijk, en vervolgens zelfs licht. Naarmate de ziekte vordert, verergert deze, wat leidt tot invaliditeit en overlijden van de patiënt.
De progressie van fibroelastose gaat gepaard met een verslechtering van de algemene toestand: hypoxie leidt tot zwakte en duizeligheid, het lichaamsgewicht neemt af (er ontstaat anorexia), de nagelkootjes veranderen in het type drumsticks, de huid wordt bleek en krijgt een ziekelijk uiterlijk.
De helft van de patiënten ontwikkelt aspecifieke symptomen zoals ademhalingsmoeilijkheden en pijn op de borst, kenmerkend voor een pneumothorax (gasophoping in de pleuraholte). Deze afwijking kan ook optreden als gevolg van verwondingen, primaire en secundaire longziekten, of onjuiste behandeling, waardoor de diagnose niet kan worden gesteld.
Cardiale fibro-elastose, evenals de pathologie van bindweefselgroei in de longen, wordt gekenmerkt door: een bleke huid, gewichtsverlies, zwakte (vaak paroxysmaal) en kortademigheid. Aanhoudende koorts zonder tekenen van verkoudheid of infectie kan ook worden waargenomen.
Bij veel patiënten treedt er een verandering op in de grootte van de lever. De lever neemt toe zonder symptomen van disfunctie. Zwelling van de benen, het gezicht, de armen en het sacrale gebied is ook mogelijk.
Een kenmerkende manifestatie van de ziekte is toenemend circulatoir falen in combinatie met hartfalen. In dit geval wordt tachycardie (verhoogde hartslag, vaak gecombineerd met aritmie), kortademigheid (ook bij afwezigheid van fysieke activiteit) en weefselcyanose (blauwverkleuring veroorzaakt door de ophoping van carboxyhemoglobine in het bloed, d.w.z. een verbinding van hemoglobine met koolstofdioxide als gevolg van een verstoorde bloedstroom en daarmee ook de gasuitwisseling) vastgesteld.
In dit geval kunnen de symptomen zich ofwel direct na de geboorte van een kind met deze pathologie voordoen, ofwel pas na verloop van tijd. Wanneer oudere kinderen en volwassenen worden getroffen, verschijnen de tekenen van ernstig hartfalen meestal tegen de achtergrond van een luchtweginfectie, die als trigger fungeert. [ 4 ]
Fibro-elastose bij kinderen
Als pulmonale fibroelastose een ziekte is die bij volwassenen voorkomt en vaak al in de kindertijd ontstaat, maar zich pas na lange tijd openbaart, dan manifesteert een vergelijkbare pathologie van het endocard van het hart zich vaak al vóór de geboorte van de baby en beïnvloedt diens leven vanaf de eerste momenten na de geboorte. Deze zeldzame maar ernstige pathologie is de oorzaak van de ontwikkeling van moeilijk te corrigeren hartfalen bij zuigelingen, van wie velen binnen twee jaar overlijden. [ 5 ]
Endocardiale fibroelastose bij pasgeborenen is in de meeste gevallen het gevolg van pathologische processen die zich tijdens de prenatale periode in het lichaam van de baby voordoen. Infecties van de moeder, genetische mutaties, afwijkingen in de ontwikkeling van het cardiovasculaire systeem, erfelijke stofwisselingsziekten - dit alles kan volgens wetenschappers leiden tot veranderingen in het bindweefsel in de hartvliezen. Vooral wanneer een foetus van 4-7 maanden oud aan twee of meer factoren tegelijk wordt blootgesteld.
Bijvoorbeeld, een combinatie van afwijkingen in de ontwikkeling van het hart en de kransslagaders (stenose, atresie, coarctatie van de aorta, abnormale ontwikkeling van hartspiercellen, endocardiale zwakte, enz.), die bijdragen aan weefselischemie, in combinatie met een ontstekingsproces door infectie, maakt het kind vrijwel kansloos op overleving. Hoewel afwijkingen in de orgaanontwikkeling nog steeds snel kunnen worden gecorrigeerd, kan progressieve fibro-elastose alleen worden vertraagd, maar niet genezen.
Meestal wordt cardiale fibroelastose bij de foetus al tijdens de zwangerschap ontdekt tijdens echografische diagnostiek in het tweede of derde trimester. Echografie en echocardiografie tussen 20 en 38 weken lieten hyperechogeniciteit zien, wat duidt op verdikking en verdichting van het endocard (meestal diffuus, minder vaak focaal), een verandering in de grootte en vorm van het hart (het orgaan is vergroot en neemt de vorm aan van een bal of kogel, de interne structuren worden geleidelijk gladgestreken). [ 6 ]
In 30-35% van de gevallen werd fibro-elastose vastgesteld vóór 26 weken zwangerschap, in 65-70% in de daaropvolgende periode. Bij meer dan 80% van de pasgeborenen gaat fibro-elastose gepaard met obstructieve hartafwijkingen, d.w.z. het is secundair, ondanks de vroege stadia van de detectie. Linkerventrikelhyperplasie werd vastgesteld bij de helft van de getroffen kinderen, wat de hoge prevalentie van fibro-elastose van deze specifieke hartstructuur verklaart. Pathologieën van de aorta en de hartklep, vastgesteld bij een derde van de kinderen met endocardiale proliferatie, leiden eveneens tot een vergroting (dilatatie) van de linkerventrikelkamer en een verstoring van de functionaliteit ervan.
Bij instrumenteel bevestigde cardiale fibro-elastose adviseren artsen om de zwangerschap te beëindigen. Bij bijna alle kinderen geboren van wie de moeder een medische abortus weigerde, werden de symptomen van de ziekte bevestigd. Symptomen van hartfalen, kenmerkend voor fibro-elastose, manifesteren zich binnen een jaar (zelden in het 2e-3e levensjaar). Bij kinderen met een gecombineerde vorm van de ziekte worden tekenen van hartfalen al vanaf de eerste levensdagen vastgesteld.
Aangeboren vormen van primaire en gecombineerde fibro-elastose bij kinderen hebben meestal een snel beloop met de ontwikkeling van ernstig hartfalen. Lage activiteit, lethargie van het kind, weigering om borstvoeding te geven vanwege snelle vermoeidheid, slechte eetlust en overmatig zweten wijzen op een slechte gezondheid. Dit alles leidt ertoe dat het kind niet goed aankomt. De huid van de baby is pijnlijk bleek, bij sommigen met een blauwachtige tint, meestal in de nasolabiale driehoek.
Er zijn tekenen van een zwakke immuniteit, waardoor dergelijke kinderen vaak en snel luchtweginfecties oplopen, wat de situatie compliceert. Soms vertoont het kind in de eerste dagen en maanden van zijn leven geen problemen met de bloedsomloop, maar frequente infecties en longaandoeningen kunnen een trigger zijn voor de ontwikkeling van congestief hartfalen.
Aanvullend medisch onderzoek bij pasgeborenen en jonge kinderen met verdenking op fibro-elastose of een eerder gediagnosticeerde aandoening toonde een lage bloeddruk (hypotensie), een vergroot hart (cardiomegalie), gedempte tonen bij het luisteren naar het hart, soms een systolisch geruis kenmerkend voor mitralisklepinsufficiëntie, tachycardie en kortademigheid. Bij het luisteren naar de longen werd piepende ademhaling waargenomen, wat wijst op congestie.
Schade aan de linkerhartkamer leidt vaak tot verzwakking van de spierlaag van het hart (myocard). Het normale hartritme bestaat uit twee ritmisch afwisselende tonen. Bij fibro-elastose kan een derde (en soms een vierde) toon optreden. Zo'n pathologisch ritme is duidelijk hoorbaar en lijkt qua geluid op de drietaktgang van een paard (galop), vandaar de naam galopritme.
Een ander symptoom van fibro-elastose bij jonge kinderen is het ontstaan van een hartbult. Dit komt doordat de ribben van het kind in de vroege postnatale periode niet-verbeend zijn en bestaan uit kraakbeenweefsel. De toename van de grootte van het hart leidt ertoe dat het op de "zachte" ribben gaat drukken, waardoor deze buigen en een permanent naar voren gebogen vorm aannemen (hartbult). Bij fibro-elastose bij volwassenen vormt zich geen hartbult vanwege de sterkte en stijfheid van het botweefsel van de ribben, zelfs niet bij een toename van alle structuren van het hart.
De vorming van een hartbult wijst op zichzelf slechts op een aangeboren hartafwijking, zonder de aard ervan te specificeren. In ieder geval gaat het gepaard met een vergroting van het hart en de hartkamers.
Oedeemsyndroom bij fibroelastose bij kinderen wordt zelden gediagnosticeerd, maar veel kinderen krijgen last van een vergrote lever, die gemiddeld 3 cm onder de rand van de ribbenboog begint uit te steken.
Als fibroelastose is ontstaan (bijvoorbeeld als gevolg van ontstekingsziekten van de hartvliezen), is het klinische beeld meestal langzaam progressief. De symptomen kunnen enige tijd volledig afwezig zijn, waarna zwakke tekenen van hartfunctiestoornissen optreden in de vorm van kortademigheid bij lichamelijke inspanning, een verhoogde hartslag, snelle vermoeidheid en een laag uithoudingsvermogen. Even later begint de lever te vergroten en ontstaan er oedeem en duizeligheid.
Alle symptomen van verworven fibro-elastose zijn aspecifiek, wat de diagnose van de ziekte compliceert en lijkt op cardiomyopathie, lever- en nieraandoeningen. De ziekte wordt meestal gediagnosticeerd in het stadium van ernstig hartfalen, wat de resultaten van de behandeling negatief beïnvloedt.
Complicaties en gevolgen
Fibro-elastose van hart en longen is een ernstige aandoening waarvan het beloop afhankelijk is van verschillende omstandigheden. Aangeboren hartafwijkingen compliceren de situatie aanzienlijk, maar kunnen op jonge leeftijd operatief worden verholpen. Tegelijkertijd blijft er een vrij hoog risico op overlijden (ongeveer 10%) bestaan.
Aangenomen wordt dat hoe eerder de ziekte zich ontwikkelt, hoe ernstiger de gevolgen zullen zijn. Dit wordt bevestigd door het feit dat congenitale fibro-elastose in de meeste gevallen een fulminant of acuut beloop heeft met snelle progressie van hartfalen. De ontwikkeling van acuut hartfalen bij een kind jonger dan 6 maanden wordt beschouwd als een slecht prognoseteken.
De behandeling garandeert echter geen volledig herstel van de hartfunctie, maar vertraagt slechts de progressie van de symptomen van hartfalen. Het uitblijven van dergelijke ondersteunende behandeling leidt daarentegen tot overlijden binnen de eerste twee levensjaren van de baby.
Als hartfalen in de eerste dagen en maanden van een baby wordt vastgesteld, zal het kind waarschijnlijk nog geen week overleven. De reactie op de behandeling verschilt per kind. Zonder therapeutisch effect is er vrijwel geen hoop. Maar met de geboden hulp is de levensverwachting van een ziek kind kort (van enkele maanden tot enkele jaren).
Chirurgie en correctie van aangeboren hartafwijkingen die fibro-elastose veroorzaken, verbeteren meestal de toestand van de patiënt. Met een succesvolle chirurgische behandeling van linkerventrikelhyperplasie en naleving van de voorschriften van de arts kan de ziekte een goedaardig beloop krijgen: hartfalen zal een chronisch beloop hebben zonder tekenen van progressie. Hoewel de hoop op een dergelijk resultaat gering is.
De verworven vorm van cardiale fibro-elastose wordt snel chronisch en ontwikkelt zich geleidelijk. Medicatie kan het proces vertragen, maar niet stoppen.
Pulmonale fibroelastose, ongeacht het tijdstip waarop de veranderingen in het parenchym en de membranen van het orgaan na de lichtperiode optreden, begint snel te vorderen en leidt binnen een paar jaar zelfs tot de dood, met ernstig ademhalingsfalen tot gevolg. Het trieste is dat er nog geen effectieve behandelmethoden voor de ziekte zijn ontwikkeld. [ 7 ]
Diagnostics fibroelastose
Endomyocardiale fibro-elastose, waarvan de symptomen in de meeste gevallen al op jonge leeftijd worden ontdekt, is een aangeboren aandoening. Als we de zeldzame gevallen uitsluiten waarin de ziekte zich in de late kindertijd en volwassenheid begon te ontwikkelen als complicatie van verwondingen en somatische aandoeningen, is het mogelijk om de pathologie al in de prenatale periode te identificeren, d.w.z. vóór de geboorte van het kind.
Artsen zijn van mening dat pathologische veranderingen in het endocardiale weefsel, veranderingen in de vorm van het foetale hart en enkele kenmerken van de werking ervan, kenmerkend voor fibro-elastose, al in de 14e week van de zwangerschap kunnen worden vastgesteld. Dit is echter nog steeds een vrij korte periode en het is niet uit te sluiten dat de ziekte zich wat later manifesteert, dichter bij het derde trimester van de zwangerschap, en soms zelfs een paar maanden voor de bevalling. Daarom wordt bij het monitoren van zwangere vrouwen aanbevolen om met tussenpozen van enkele weken klinische echografie van het foetale hart uit te voeren.
Aan welke tekenen kunnen artsen de ziekte tijdens de volgende echo verraden? Veel hangt af van de vorm van de ziekte. Meestal wordt fibro-elastose vastgesteld in het gebied van de linkerhartkamer, maar deze structuur is niet altijd vergroot. De verwijde vorm van de ziekte met een vergroot linkerhartkamer is gemakkelijk te bepalen tijdens een echografie door de bolvormige vorm van het hart, waarvan de top wordt weergegeven door de linkerhartkamer, de algemene toename van de grootte van het orgaan en de uitstulping van het interventriculaire septum richting de rechterhartkamer. Maar het belangrijkste teken van fibro-elastose is verdikking van het endocard, evenals hartsepta met een karakteristieke toename van de echogeniciteit van deze structuren, die wordt vastgesteld door een specifieke echografie.
Het onderzoek wordt uitgevoerd met behulp van speciale echografieapparatuur met cardiologieprogramma's. Foetale echocardiografie is niet schadelijk voor de moeder of het ongeboren kind, maar maakt het niet alleen mogelijk om anatomische veranderingen in het hart te identificeren, maar ook om de conditie van de kransslagaders, de aanwezigheid van bloedstolsels daarin en veranderingen in de dikte van de hartslijmvliezen te bepalen.
Foetale echocardiografie wordt niet alleen voorgeschreven bij afwijkingen bij het decoderen van de echo-uitslagen, maar ook bij een infectie bij de moeder (met name een virale infectie), het gebruik van sterke medicijnen, erfelijke aanleg, de aanwezigheid van stofwisselingsstoornissen en bij aangeboren hartafwijkingen bij oudere kinderen.
Foetale echocardiografie kan ook andere aangeboren vormen van fibro-elastose opsporen. Bijvoorbeeld fibro-elastose van de rechterkamer, een wijdverbreid proces met gelijktijdige schade aan de linkerkamer en aangrenzende structuren: de rechterkamer, hartkleppen, atria, gecombineerde vormen van fibro-elastose, endomyocardiale fibro-elastose met verdikking van de binnenwand van de kamers en betrokkenheid van een deel van de hartspier bij het pathologische proces (meestal gecombineerd met trombose van de hartwand).
Endocardiale fibro-elastose die vóór de geboorte wordt vastgesteld, heeft een zeer slechte prognose, dus artsen adviseren in dit geval om de zwangerschap te beëindigen. De mogelijkheid van een foutieve diagnose wordt uitgesloten door een herhaalde echo van het foetale hart, die 4 weken na het eerste onderzoek dat de pathologie aan het licht bracht, wordt uitgevoerd. Het is duidelijk dat de uiteindelijke beslissing over het beëindigen of voortzetten van de zwangerschap bij de ouders ligt, maar ze moeten zich wel bewust zijn van het leven dat ze hun kind toebedelen.
Endocardiale fibro-elastose wordt niet altijd tijdens de zwangerschap ontdekt, vooral omdat niet alle aanstaande moeders zich registreren bij een vrouwenkliniek en preventief echoscopisch onderzoek ondergaan. De ziekte van het kind in haar buik heeft vrijwel geen invloed op de toestand van de zwangere vrouw, waardoor de geboorte van een ziek kind vaak een onaangename verrassing is.
In sommige gevallen vernemen zowel de ouders als de artsen pas enkele maanden na de geboorte van de baby dat hij of zij ziek is. In dat geval kan het bloedonderzoek in het laboratorium niets laten zien, behalve een verhoogde natriumconcentratie (hypernatriëmie). De resultaten hiervan zijn echter wel nuttig bij differentiële diagnostiek om ontstekingsziekten uit te sluiten.
Er is nog hoop op instrumentele diagnostiek. Een standaardonderzoek van het hart (ECG) is niet bijzonder indicatief in het geval van fibro-elastose. Het helpt bij het identificeren van stoornissen in het hart en de elektrische geleiding van de hartspier, maar specificeert niet de oorzaken van dergelijke aandoeningen. Zo wijst een verandering in de ECG-spanning (op jongere leeftijd meestal onderschat, op oudere leeftijd juist extreem hoog) op cardiomyopathie, die niet alleen kan worden geassocieerd met hartpathologieën, maar ook met stofwisselingsstoornissen. Tachycardie is een symptoom van hartziekten. En als beide hartkamers zijn aangetast, kan het cardiogram over het algemeen normaal lijken. [ 8 ]
Computertomografie (CT) is een uitstekend niet-invasief instrument voor het detecteren van cardiovasculaire verkalking en het uitsluiten van pericarditis.[ 9 ]
Magnetic resonance imaging (MRI) kan nuttig zijn bij het detecteren van fibro-elastose, omdat biopsie invasief is. Een hypointense rand op een myocardiale perfusiesequentie en een hyperintense rand op een vertraagde versterkingssequentie zijn suggestief voor fibro-elastose.[ 10 ]
Maar dat wil niet zeggen dat het onderzoek moet worden stopgezet. Het helpt namelijk om de aard van het hart en de mate van hartfalen vast te stellen.
Wanneer symptomen van hartfalen optreden en de patiënt hierover een arts raadpleegt, krijgt hij/zij ook het volgende voorgeschreven: een röntgenfoto van de borstkas, computertomografie of magnetische resonantie beeldvorming van het hart, echocardiografie (EchoCG). In twijfelgevallen is een biopsie van hartweefsel met aansluitend histologisch onderzoek noodzakelijk. De diagnose is zeer ernstig en vereist daarom dezelfde aanpak voor de diagnose, hoewel de behandeling niet veel verschilt van de symptomatische behandeling van coronaire hartziekten en hartfalen.
Maar zelfs zo'n nauwgezet onderzoek is nutteloos als de resultaten niet worden gebruikt in de differentiële diagnostiek. ECG-resultaten kunnen worden gebruikt om acute fibro-elastose te differentiëren van idiopathische myocarditis, exsudatieve pericarditis en aortaklepstenose. Tegelijkertijd zullen laboratoriumtests geen tekenen van ontsteking (leukocytose, verhoogde bezinkingssnelheid, enz.) laten zien en temperatuurmetingen zullen geen hyperthermie aantonen.
Analyse van hartgeluiden en hartruis, veranderingen in de grootte van de atria en bestudering van de anamnese helpen om endocardiale fibro-elastose te onderscheiden van geïsoleerde mitralisklepinsufficiëntie en mitralisklepdefect.
Analyse van anamnestische gegevens is nuttig om onderscheid te maken tussen fibro-elastose en hart- en aortaklepstenose. Bij aortaklepstenose is het ook zinvol om te letten op het behoud van het sinusritme en de afwezigheid van trombo-embolie. Ook bij exsudatieve pericarditis worden geen hartritmestoornissen en trombusafzetting waargenomen, maar de ziekte manifesteert zich wel met een verhoging van de temperatuur en koorts.
De grootste moeilijkheid is het onderscheid te maken tussen endocardiale fibro-elastose en congestieve cardiomyopathie. In dit geval heeft fibro-elastose, hoewel het in de meeste gevallen niet gepaard gaat met uitgesproken hartgeleidingsstoornissen, een minder gunstige behandelprognose.
Bij gecombineerde pathologieën is het noodzakelijk om aandacht te besteden aan eventuele afwijkingen die tijdens een tomografie of echo van het hart worden vastgesteld, omdat aangeboren afwijkingen het beloop van fibro-elastose aanzienlijk compliceren. Als gecombineerde endocardiale fibro-elastose in de intra-uteriene periode wordt vastgesteld, is het niet wenselijk om de zwangerschap te handhaven. Het is veel humaner om de zwangerschap te beëindigen.
Diagnose van pulmonale fibro-elastose
De diagnose van pulmonale fibroelastose vereist ook bepaalde kennis en vaardigheden van de arts. De symptomen van de ziekte zijn namelijk nogal heterogeen. Enerzijds wijzen ze op congestieve longaandoeningen (niet-productieve hoest, kortademigheid), anderzijds kunnen ze ook een uiting zijn van hartpathologie. De diagnose van de ziekte kan daarom niet worden beperkt tot alleen het vaststellen van symptomen en auscultatie.
Bloedonderzoek bij de patiënt helpt bij het uitsluiten van inflammatoire longziekten, maar geeft geen informatie over kwantitatieve en kwalitatieve veranderingen in weefsels. De aanwezigheid van tekenen van eosinofilie helpt bij het onderscheiden van de ziekte van longfibrose, die qua manifestaties vergelijkbaar is, maar ontkent of bevestigt het bestaan van fibro-elastose niet.
Meer indicatief worden instrumentele onderzoeken beschouwd: röntgenfoto's van de borstkas en tomografisch onderzoek van de ademhalingsorganen, maar ook functionele analyses, waarbij het ademhalingsvolume, de vitale capaciteit van de longen en de druk in het orgaan worden bepaald.
Bij pulmonale fibro-elastose is het belangrijk om te letten op de afname van de externe ademhaling, gemeten tijdens spirometrie. De afname van actieve alveolaire holten heeft een aanzienlijke invloed op de vitale capaciteit van de longen (VCL), en de verdikking van de wanden van de interne structuren beïnvloedt de diffusiecapaciteit van het orgaan (DCL), die zorgt voor ventilatie en gasuitwisseling (eenvoudig gezegd: het opnemen van koolstofdioxide uit het bloed en het afgeven van zuurstof).
Kenmerkende tekenen van pleuroparenchymale fibroelastose zijn een combinatie van beperkte luchtstroom in de longen (obstructie) en verminderde longuitzetting bij inademing (restrictie), verslechtering van de externe ademhalingsfunctie, matige pulmonale hypertensie (verhoogde druk in de longen), vastgesteld bij de helft van de patiënten.
Een longbiopsie toont karakteristieke veranderingen in de interne structuur van het orgaan, waaronder: fibrose van het pleura en parenchym in combinatie met elastose van de alveolaire wanden, ophoping van lymfocyten in het gebied van verdichte alveolaire septa, transformatie van fibroblasten naar spierweefsel dat niet kenmerkend is voor deze cellen, en de aanwezigheid van oedeemvocht.
Het tomogram toont schade aan de bovenste longdelen in de vorm van pleurale verdichtingshaarden en structurele veranderingen in het longparenchym. Het vergrote bindweefsel van de longen lijkt qua kleur en eigenschappen op spierweefsel, maar het longvolume neemt af. In het parenchym worden vrij grote, luchthoudende holtes (cysten) aangetroffen. Kenmerkend zijn een onomkeerbare focale (of diffuse) verwijding van de bronchiën en bronchiolen (tractiebronchiëctasieën) en een lage ligging van de diafragmakoepel.
Bij radiologisch onderzoek worden bij veel patiënten gebieden met "matglas" en "honingraatlong" gevonden, wat wijst op een ongelijkmatige ventilatie van de longen als gevolg van de aanwezigheid van weefselverdichtingshaarden. Ongeveer de helft van de patiënten heeft vergrote lymfeklieren en lever.
Pulmonale fibroelastose moet worden onderscheiden van fibrose veroorzaakt door een parasitaire infectie en de daarmee gepaard gaande eosinofilie, endocardiale fibroelastose, longziekten met een verstoorde ventilatie en het "honingraatlongbeeld", de auto-immuunziekte histicotitis X (een vorm van deze pathologie met longschade wordt de ziekte van Hand-Schüller-Christian genoemd), uitingsvormen van sarcoïdose en longtuberculose.
Behandeling fibroelastose
Fibro-elastose, ongeacht de locatie, wordt beschouwd als een gevaarlijke en praktisch ongeneeslijke ziekte. Pathologische veranderingen in het longvlies en longparenchym kunnen niet met medicijnen worden hersteld. Zelfs het gebruik van hormonale ontstekingsremmers (corticosteroïden) in combinatie met bronchusverwijders geeft niet het gewenste resultaat. Bronchusverwijders helpen de toestand van de patiënt enigszins te verlichten door het obstructieve syndroom te verlichten, maar ze hebben geen invloed op de processen in de longen en kunnen daarom alleen als ondersteunende therapie worden gebruikt.
Chirurgische behandeling van pulmonale fibroelastose is eveneens ineffectief. De enige operatie die de situatie zou kunnen veranderen, is een donororgaantransplantatie. Maar longtransplantatie heeft helaas dezelfde ongunstige prognose. [ 11 ]
Volgens buitenlandse wetenschappers kan fibro-elastose ook worden beschouwd als een van de meest voorkomende complicaties van long- of beenmergstamceltransplantatie. In beide gevallen treden er veranderingen op in de bindweefselvezels van de longen, waardoor de externe ademhaling wordt beïnvloed.
De ziekte ontwikkelt zich zonder behandeling (en effectieve behandeling is momenteel afwezig) en ongeveer 40% van de patiënten overlijdt binnen 1,5 tot 2 jaar aan ademhalingsfalen. De levensverwachting van degenen die overblijven is eveneens ernstig beperkt (tot 10 tot 20 jaar), evenals hun vermogen om te werken. De persoon raakt arbeidsongeschikt.
Cardiale fibroelastose wordt ook beschouwd als een medisch ongeneeslijke ziekte, vooral als het een aangeboren afwijking betreft. Kinderen worden meestal niet ouder dan twee jaar. Ze kunnen alleen gered worden door een harttransplantatie, wat op zich al een zware operatie is met een hoog risico en onvoorspelbare gevolgen, vooral op zo'n jonge leeftijd.
Bij sommige baby's is het mogelijk om aangeboren hartafwijkingen operatief te corrigeren, zodat de toestand van het zieke kind niet verergert. Bij stenose van de slagader wordt een vaatverwijdende buis (shunt) geplaatst (aortocoronaire bypass). Bij verwijding van de linkerhartkamer wordt de vorm ervan snel hersteld. Maar zelfs een dergelijke operatie garandeert niet dat het kind een transplantatie kan missen. Ongeveer 20-25% van de baby's overleeft het en lijdt hun hele leven aan hartfalen, wat betekent dat ze niet als gezond worden beschouwd.
Als de ziekte wordt opgelopen, is het de moeite waard om met medicijnen voor het leven van het kind te vechten. Maar het is belangrijk om te beseffen dat hoe eerder de ziekte zich manifesteert, hoe moeilijker het zal zijn om deze te bestrijden.
Medicamenteuze behandeling is gericht op het bestrijden en voorkomen van exacerbaties van hartfalen. Patiënten krijgen de volgende hartmedicijnen voorgeschreven:
- ACE-remmers (angiotensine-converterend enzym), die de bloeddruk beïnvloeden en deze binnen normale grenzen houden (captopril, enalapril, benazepril, enz.),
- bètablokkers die worden gebruikt voor de behandeling van hartritmestoornissen, arteriële hypertensie en ter voorkoming van een hartinfarct (anapriline, bisoprolol, metoprolol),
- hartglycosiden, die bij langdurig gebruik niet alleen de werking van het hart ondersteunen (verhoging van het kaliumgehalte in cardiomyocyten en verbetering van de myocardiale geleidbaarheid), maar ook in staat zijn de mate van endocardiale verdikking enigszins te verminderen (digoxine, gitoxine, strofantine),
- kaliumsparende diuretica (spironolacton, veroshpiron, decriz), ter voorkoming van weefseloedeem,
- antitrombotische therapie met anticoagulantia (cardiomagnyl, magnicor), die de vorming van bloedstolsels en stoornissen in de bloedsomloop in de kransslagaders voorkomen.
Bij de aangeboren vorm van endocardiale fibro-elastose bevordert ondersteunende behandeling het herstel niet, maar vermindert het het risico op overlijden door hartfalen of trombo-embolie met 70-75%. [ 12 ]
Geneesmiddelen
Zoals we kunnen zien, verschilt de behandeling van endocardiale fibro-elastose praktisch niet van die van hartfalen. In beide gevallen houden cardiologen rekening met de ernst van de cardiopathie. Het voorschrijven van medicijnen is strikt individueel, rekening houdend met de leeftijd van de patiënt, bijkomende aandoeningen, de vorm en de ernst van het hartfalen.
Bij de behandeling van verworven endocardiale fibro-elastose worden medicijnen uit vijf groepen gebruikt. Laten we één medicijn uit elke groep bekijken.
Enalapril is een geneesmiddel uit de groep ACE-remmers, verkrijgbaar in de vorm van tabletten met verschillende doseringen. Het geneesmiddel verhoogt de coronaire bloedstroom, verwijdt de slagaders, verlaagt de bloeddruk zonder de hersencirculatie te beïnvloeden, vertraagt en vermindert de uitzetting van de linkerhartkamer. Het geneesmiddel verbetert de bloedtoevoer naar de hartspier, vermindert de effecten van ischemie, vermindert de bloedstolling enigszins, voorkomt de vorming van bloedstolsels en heeft een licht diuretisch effect.
Bij hartfalen wordt het medicijn voorgeschreven voor een periode van meer dan zes maanden of permanent. De behandeling wordt gestart met een minimale dosis (2,5 mg) en geleidelijk verhoogd met 2,5-5 mg om de 3-4 dagen. De permanente dosis is de dosis die goed wordt verdragen door de patiënt en die de bloeddruk binnen de normale waarden houdt.
De maximale dagelijkse dosis is 40 mg. Het kan in één keer of verdeeld over twee doses worden ingenomen.
Als de bloeddruk lager is dan normaal, wordt de dosis geleidelijk verlaagd. De behandeling met enalapril mag niet abrupt worden stopgezet. Het wordt aanbevolen om een onderhoudsdosis van 5 mg per dag in te nemen.
Het medicijn is bedoeld voor de behandeling van volwassen patiënten, maar kan ook aan een kind worden voorgeschreven (de veiligheid is niet officieel vastgesteld, maar in geval van fibro-elastose staat het leven van een kleine patiënt op het spel, dus de risicoverhouding wordt in acht genomen). De ACE-remmer wordt niet voorgeschreven aan patiënten met een intolerantie voor de bestanddelen van het medicijn, met porfyrie, zwangerschap en borstvoeding. Als de patiënt eerder Quincke-oedeem heeft gehad tijdens het gebruik van geneesmiddelen uit deze groep, is Enalapril verboden.
Voorzichtigheid is geboden bij het voorschrijven van het geneesmiddel aan patiënten met gelijktijdige aandoeningen: ernstige nier- en leverziekten, hyperkaliëmie, hyperaldosteronisme, aorta- of mitralisklepstenose, systemische bindweefselziekten, hartischemie, hersenziekten, diabetes mellitus.
Gebruik geen conventionele diuretica tijdens de behandeling met dit geneesmiddel om uitdroging en een sterk hypotensief effect te voorkomen. Gelijktijdige toediening met kaliumsparende diuretica vereist een dosisaanpassing, aangezien er een hoog risico bestaat op hyperkaliëmie, wat op zijn beurt hartritmestoornissen, toevallen, een verminderde spierspanning, toegenomen zwakte, enz. kan veroorzaken.
Het medicijn "Enalapril" wordt over het algemeen goed verdragen, maar sommige patiënten kunnen bijwerkingen ervaren. De meest voorkomende bijwerkingen zijn: een sterke bloeddrukdaling, die kan leiden tot flauwvallen, hoofdpijn en duizeligheid, slaapstoornissen, toegenomen vermoeidheid, omkeerbaar verlies van evenwicht, gehoor en gezichtsvermogen, het optreden van oorsuizen, kortademigheid, hoesten zonder sputumafscheiding, veranderingen in de samenstelling van het bloed en de urine, wat meestal wijst op een slechte werking van de lever en de nieren. Mogelijke bijwerkingen zijn: haaruitval, verminderd seksueel verlangen, opvliegers (hittegevoel en hartkloppingen, hyperemie van de gezichtshuid, enz.).
Bisoprolol is een bètablokker met selectieve werking, die bloeddrukverlagende en anti-ischemische effecten heeft en helpt bij het bestrijden van de manifestaties van tachycardie en aritmie. Het is een budgetmedicijn in tabletvorm dat de progressie van hartfalen bij endocardiale fibro-elastose voorkomt. [ 13 ]
Net als veel andere medicijnen die worden voorgeschreven voor coronaire hartziekten en hartfalen, wordt bisoprolol langdurig voorgeschreven. Het is raadzaam om het 's ochtends vóór of tijdens de maaltijd in te nemen.
De aanbevolen doseringen worden individueel gekozen, afhankelijk van de bloeddrukwaarden en de medicijnen die parallel aan dit geneesmiddel worden voorgeschreven. Gemiddeld bedraagt een enkele (ook dagelijkse) dosis 5-10 mg, maar bij een lichte drukstijging kan deze worden verlaagd tot 2,5 mg. De maximale dosis die kan worden voorgeschreven aan een patiënt met normaal functionerende nieren is 20 mg, maar alleen bij een constant hoge bloeddruk.
Verhoging van de aangegeven dosering is alleen mogelijk met toestemming van een arts. Bij ernstige lever- en nieraandoeningen wordt 10 mg echter als de maximaal toegestane dosis beschouwd.
Bij de complexe behandeling van hartfalen tegen de achtergrond van linkerventrikeldisfunctie, die meestal optreedt bij fibro-elastose, wordt een effectieve dosis gekozen door de dosering geleidelijk met 1,25 mg te verhogen. In dit geval wordt begonnen met de laagst mogelijke dosis (1,25 mg). De dosering wordt met tussenpozen van 1 week verhoogd.
Wanneer de dosis 5 mg bereikt, wordt het interval verlengd tot 28 dagen. Na 4 weken wordt de dosis verhoogd met 2,5 mg. Met inachtneming van dit interval en de norm bereiken ze 10 mg, wat de patiënt langdurig of constant moet innemen.
Als een dergelijke dosering slecht wordt verdragen, wordt deze geleidelijk verlaagd tot een comfortabel niveau. Ook mag de behandeling met een bètablokker niet abrupt worden stopgezet.
Het geneesmiddel mag niet worden voorgeschreven bij overgevoeligheid voor de werkzame stoffen of hulpstoffen van het geneesmiddel, bij acuut en gedecompenseerd hartfalen, bij cardiogene shock, bij atrioventriculair blok graad 2-3, bij bradycardie, bij aanhoudend lage bloeddruk en bij bepaalde andere hartpathologieën, bij ernstige bronchiale astma, bij broncho-obstructie, bij ernstige perifere circulatiestoornissen en bij metabole acidose.
Voorzichtigheid is geboden bij het voorschrijven van complexe behandelingen. De combinatie van bisoprolol met bepaalde antiaritmica (kinidine, lidocaïne, fenytoïne, enz.), calciumantagonisten en centrale bloeddrukverlagende middelen wordt daarom niet aanbevolen.
Onaangename symptomen en aandoeningen die mogelijk zijn tijdens de behandeling met bisoprolol: verhoogde vermoeidheid, hoofdpijn, opvliegers, slaapstoornissen, bloeddrukdaling en duizeligheid bij het opstaan, gehoorverlies, maag-darmklachten, lever- en nieraandoeningen, verminderde potentie, spierzwakte en krampen. Soms klagen patiënten over perifere bloedsomloopstoornissen, die zich uiten in een temperatuurdaling of gevoelloosheid in de ledematen, met name de vingers en tenen.
Bij gelijktijdige aandoeningen van het bronchopulmonale stelsel, de nieren, de lever en diabetes mellitus is de kans op bijwerkingen groter, wat duidt op een verergering van de aandoening.
"Digoxine" is een populaire, goedkope hartglycoside op basis van vingerhoedskruid. Het wordt uitsluitend op recept (in tabletten) verstrekt en dient onder zijn toezicht te worden gebruikt. De injectiebehandeling vindt plaats in een ziekenhuisomgeving tijdens verergering van coronaire hartziekte en hartfalen. Tabletten worden doorlopend voorgeschreven in minimaal effectieve doses, omdat het medicijn een toxisch en narcotisch effect heeft.
Het therapeutische effect bestaat uit het veranderen van de kracht en amplitude van de myocardcontracties (geeft het hart energie en ondersteunt het bij ischemische aandoeningen). Het medicijn heeft ook een vaatverwijdend (vermindert congestie) en een enigszins diuretisch effect, wat helpt bij het verlichten van zwelling en het verminderen van de ernst van ademhalingsfalen, dat zich manifesteert als kortademigheid.
Het gevaar van Digoxine en andere hartglycosiden is dat ze bij overdosering hartritmestoornissen kunnen veroorzaken, veroorzaakt door een verhoogde prikkelbaarheid van de hartspier.
Bij verergering van CHF wordt het medicijn in de vorm van injecties voorgeschreven, waarbij een individuele dosering wordt gekozen rekening houdend met de ernst van de aandoening en de leeftijd van de patiënt. Zodra de aandoening stabiliseert, wordt overgegaan op tabletten.
De standaard enkelvoudige dosis van het geneesmiddel is gewoonlijk 0,25 mg. De toedieningsfrequentie kan variëren van 1 tot 5 keer per dag met gelijke tussenpozen. In de acute fase van hartfalen kan de dagelijkse dosis 1,25 mg bedragen. Wanneer de toestand permanent stabiliseert, is een onderhoudsdosis van 0,25 (minder vaak 0,5) mg per dag noodzakelijk.
Bij het voorschrijven van het medicijn aan kinderen wordt rekening gehouden met het gewicht van de patiënt. Een effectieve en veilige dosis wordt berekend als 0,05-0,08 mg per kg lichaamsgewicht. Het medicijn wordt echter niet continu voorgeschreven, maar gedurende 1-7 dagen.
De dosering van hartglycosiden moet door een arts worden voorgeschreven, rekening houdend met de toestand en leeftijd van de patiënt. Tegelijkertijd is het zeer gevaarlijk om de dosering onafhankelijk van elkaar aan te passen of twee geneesmiddelen met een dergelijk effect tegelijkertijd te gebruiken.
"Digoxine" wordt niet voorgeschreven bij instabiele angina pectoris, ernstige hartritmestoornissen, AV-blok graad 2-3, harttamponade, het Adams-Stokes-Morgagni-syndroom, geïsoleerde bicuspideklepstenose en aortastenose, een aangeboren hartafwijking genaamd Wolff-Parkinson-White-syndroom, hypertrofische obstructieve cardiomyopathie, endo-, peri- en myocarditis, thoracaal aorta-aneurysma, hypercalciëmie, hypokaliëmie en enkele andere aandoeningen. De lijst met contra-indicaties is vrij lang en omvat syndromen met meerdere manifestaties, dus de beslissing over het gebruik van dit medicijn kan alleen door een specialist worden genomen.
Digoxine heeft ook bijwerkingen. Deze omvatten hartritmestoornissen (als gevolg van een verkeerd gekozen dosis en overdosering), verlies van eetlust, misselijkheid (vaak met braken), darmklachten, ernstige zwakte en vermoeidheid, hoofdpijn, het verschijnen van "vliegjes" voor de ogen, een daling van het aantal bloedplaatjes en bloedstollingsstoornissen, en allergische reacties. Meestal worden deze en andere symptomen geassocieerd met het innemen van hoge doses van het medicijn, minder vaak met langdurige behandeling.
Spironolacton is een mineralocorticoïde-antagonist. Het heeft een diuretisch effect en bevordert de uitscheiding van natrium, chloor en water, maar behoudt kalium, dat noodzakelijk is voor de normale werking van het hart, aangezien de geleidende functie voornamelijk op dit element gebaseerd is. Het helpt oedeem te verlichten. Het wordt gebruikt als adjuvans bij congestief hartfalen.
Bij hartfalen wordt het medicijn voorgeschreven afhankelijk van de fase van de ziekte. Bij exacerbatie kan het medicijn zowel in de vorm van injecties als in de vorm van tabletten worden voorgeschreven in een dosering van 50-100 mg per dag. Wanneer de toestand stabiliseert, wordt gedurende langere tijd een onderhoudsdosis van 25-50 mg voorgeschreven. Indien de kalium-natriumbalans verstoord raakt en de kalium-natriumspiegel daalt, kan de dosis worden verhoogd totdat een normale concentratie sporenelementen is bereikt.
In de pediatrie wordt de effectieve dosering berekend op basis van een verhouding van 1-3 mg spironolacton per kilogram lichaamsgewicht van de patiënt.
Zoals we kunnen zien is ook hier de keuze van de aanbevolen dosering individueel, zoals dat ook het geval is bij het voorschrijven van veel andere medicijnen die in de cardiologie worden gebruikt.
Contra-indicaties voor het gebruik van een diureticum kunnen zijn: een te hoog kalium- of een te laag natriumgehalte in het lichaam, een pathologie die gepaard gaat met het uitblijven van urineren (anurie), en een ernstige nieraandoening met verminderde prestaties. Het medicijn wordt niet voorgeschreven aan zwangere vrouwen en moeders die borstvoeding geven, evenals aan mensen met een intolerantie voor de bestanddelen van het medicijn.
Voorzichtigheid is geboden bij gebruik van het geneesmiddel bij patiënten met een AV-hartblok (kan verergeren), een teveel aan calcium (hypercalciëmie), metabole acidose, diabetes mellitus, menstruatieonregelmatigheden en leverziekte.
Het gebruik van dit geneesmiddel kan hoofdpijn, slaperigheid, verlies van evenwicht en bewegingscoördinatie (ataxie), vergroting van de borstklieren bij mannen (gynaecomastie) en impotentie veroorzaken, veranderingen in de aard van de menstruatie, een grovere stem en overmatige haargroei bij vrouwen (hirsutisme), pijn in de bovenbuik en maag-darmklachten, darmkoliek, nierfunctiestoornissen en een verstoorde mineraalbalans. Huid- en allergische reacties zijn mogelijk.
Bijwerkingen treden meestal op wanneer de vereiste dosis wordt overschreden. Oedeem kan optreden wanneer de dosering onvoldoende is.
"Magnicor" is een geneesmiddel dat de vorming van bloedstolsels voorkomt op basis van acetylsalicylzuur en magnesiumhydroxide. Het is een van de effectieve antitrombotische middelen die wordt voorgeschreven bij hartfalen. Het heeft een pijnstillende, ontstekingsremmende en bloedplaatjesremmende werking en beïnvloedt de ademhalingsfunctie. Magnesiumhydroxide vermindert de negatieve invloed van acetylsalicylzuur op het maag-darmslijmvlies.
Bij endomyocardiale fibro-elastose wordt het medicijn voorgeschreven voor profylactische doeleinden. De minimale effectieve dosis is daarom 75 mg, wat overeenkomt met 1 tablet. Bij cardiale ischemie als gevolg van trombusvorming en daaropvolgende vernauwing van het lumen van de kransslagaders bedraagt de startdosis 2 tabletten en komt de onderhoudsdosis overeen met de profylactische dosis.
Wanneer de aanbevolen dosering wordt overschreden, neemt het risico op moeilijk te stoppen bloedingen aanzienlijk toe.
De doseringen zijn geïndiceerd voor volwassen patiënten vanwege het feit dat het medicijn acetylsalicylzuur bevat, waarvan het gebruik op de leeftijd van jonger dan 15 jaar ernstige gevolgen kan hebben.
Het geneesmiddel wordt niet voorgeschreven aan patiënten in de kindertijd en vroege adolescentie, bij intolerantie voor acetylsalicylzuur en andere bestanddelen van het geneesmiddel, bij "aspirine"-astma (in de anamnese), bij acute erosieve gastritis, bij een maagzweer, bij hemorragische diathese, bij ernstige lever- en nierziekten en bij ernstig gedecompenseerd hartfalen.
Tijdens de zwangerschap wordt Magnicor alleen voorgeschreven in geval van extreme noodzaak en alleen in het eerste en tweede trimester, rekening houdend met de mogelijke negatieve effecten op de foetus en het verloop van de zwangerschap. In het derde trimester van de zwangerschap is een dergelijke behandeling ongewenst, omdat het bijdraagt aan een afname van de contractiliteit van de baarmoeder (verlengde weeën) en ernstige bloedingen kan veroorzaken. De foetus kan pulmonale hypertensie en nierfunctiestoornissen hebben.
Bijwerkingen van het medicijn omvatten symptomen van het maag-darmkanaal (dyspepsie, pijn in de bovenbuik en in de maag, en een zeker risico op maagbloedingen met de ontwikkeling van ijzergebreksanemie). Tegen de achtergrond van het gebruik van het medicijn zijn neusbloedingen, bloedend tandvlees en bloedingen van de urinewegen mogelijk.
Overdosering kan duizeligheid, flauwvallen en oorsuizen veroorzaken. Allergische reacties zijn niet ongewoon, vooral in het geval van overgevoeligheid voor salicylaten. Anafylaxie en ademhalingsfalen zijn echter zeldzame bijwerkingen.
De keuze van geneesmiddelen voor complexe therapie en de aanbevolen doseringen dienen strikt individueel te zijn. Bijzondere voorzichtigheid is geboden bij de behandeling van zwangere vrouwen, moeders die borstvoeding geven, kinderen en oudere patiënten.
Traditionele geneeskunde en homeopathie
Cardiale fibro-elastose is een ernstige en ernstige ziekte met een kenmerkend progressief beloop en vrijwel geen kans op herstel. Het is duidelijk dat een effectieve behandeling van een dergelijke ziekte met volksremedies onmogelijk is. Traditionele geneeswijzen, die voornamelijk neerkomen op kruidentherapie, mogen alleen als hulpmiddel en uitsluitend met toestemming van een arts worden gebruikt, om de toch al slechte prognose niet te verergeren.
Wat homeopathische middelen betreft, het gebruik ervan is niet verboden en kan deel uitmaken van een uitgebreide behandeling van hartfalen. In dit geval gaat het echter niet zozeer om de behandeling, maar om het voorkomen van de progressie van hartfalen.
De medicijnen dienen voorgeschreven te worden door een ervaren homeopaat en de vraag of ze eventueel in een complexe therapie kunnen worden opgenomen, valt onder de competentie van de behandelend arts.
Welke homeopathische middelen helpen de progressie van hartfalen bij fibroelastose te vertragen? Bij acuut hartfalen maken homeopaten gebruik van de volgende middelen: Arsenicum album, Antimonium tartaricum, Carbo vegetabilis en Acidum oxalicum. Ondanks de gelijkenis van de indicaties, baseren artsen zich bij de keuze van een effectief geneesmiddel op de uiterlijke manifestaties van ischemie in de vorm van cyanose (de mate en prevalentie ervan) en de aard van het pijnsyndroom.
Bij CHF kunnen de volgende middelen deel uitmaken van de onderhoudstherapie: Lachesis en Nayu, Lycopus (in de beginfase van hartvergroting), Laurocerasus (bij kortademigheid in rust), Latrodectus mactans (bij hartklepafwijkingen), meidoornpreparaten (vooral nuttig bij endomyocardiale letsels).
Bij een sterke hartslag kunnen de volgende middelen voor symptomatische behandeling worden voorgeschreven: Spigelia, Glonoinum (bij tachycardie), Aurum metallicum (bij hypertensie).
Om de ernst van kortademigheid te verminderen, kunnen de volgende middelen helpen: Grindelia, Spongia en Lahegis. Om hartpijn te verlichten, kunnen de volgende middelen worden voorgeschreven: Cactus, Cereus, Naya, Cuprum, Aconitum om angst tegen deze achtergrond te verlichten. Bij de ontwikkeling van hartastma zijn de volgende middelen geïndiceerd: Digitalis, Laurocerasus en Lycopus.
Het voorkomen
Preventie van verworven fibro-elastose van hart en longen bestaat uit het voorkomen en tijdig behandelen van infectie- en ontstekingsziekten, met name als het gaat om schade aan vitale organen. Een effectieve behandeling van de onderliggende ziekte helpt gevaarlijke gevolgen, waaronder fibro-elastose, te voorkomen. Dit is een uitstekende reden om goed voor uw eigen gezondheid en die van toekomstige generaties te zorgen, het zogenaamde werken aan een gezonde toekomst en een lang leven.
Prognose
De veranderingen in het bindweefsel die gepaard gaan met cardiale en pulmonale fibro-elastose worden als onomkeerbaar beschouwd. Hoewel sommige medicijnen de dikte van het endocard enigszins kunnen verminderen bij langdurige therapie, garanderen ze geen genezing. Hoewel de aandoening niet altijd fataal is, is de prognose nog steeds relatief slecht. De overlevingskans na vier jaar bedraagt 77%. [ 14 ]
De slechtste prognose, zoals we al vermeldden, is de aangeboren vorm van cardiale fibroelastose, waarbij de manifestaties van hartfalen al in de eerste weken en maanden van het leven van het kind zichtbaar zijn. Alleen een harttransplantatie kan de baby redden, wat op zich al een riskante operatie is in zo'n vroege fase, en die vóór de leeftijd van twee jaar moet worden uitgevoerd. Zulke kinderen leven meestal niet langer.
Andere operaties voorkomen alleen vroegtijdig overlijden van het kind (en niet altijd), maar kunnen hem niet volledig van hartfalen genezen. De dood treedt op met decompensatie en de ontwikkeling van ademhalingsfalen.
De prognose voor pulmonale fibroelastose hangt af van de kenmerken van de ziekte. Als de symptomen zich snel ontwikkelen, is de kans zeer klein. Als de ziekte geleidelijk vordert, kan de patiënt ongeveer 10-20 jaar leven, totdat ademhalingsfalen optreedt als gevolg van veranderingen in de longblaasjes.
Veel moeilijk te behandelen aandoeningen kunnen worden voorkomen door preventieve maatregelen te nemen. In het geval van cardiale fibro-elastose is dit allereerst het voorkomen van factoren die de ontwikkeling van het hart en de bloedsomloop van de foetus kunnen beïnvloeden (met uitzondering van erfelijke aanleg en mutaties, waartegen artsen machteloos staan). Indien deze niet kunnen worden vermeden, helpt vroege diagnostiek om de aandoening te identificeren in een stadium waarin zwangerschapsafbreking mogelijk is, wat in deze situatie als humaan wordt beschouwd.

