Medisch expert van het artikel
Nieuwe publicaties
Hartkleppen
Laatst beoordeeld: 04.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Vroeger werd gedacht dat alle hartkleppen eenvoudige structuren waren waarvan de bijdrage aan de unidirectionele bloedstroom simpelweg bestond uit passieve beweging als reactie op een toegepaste drukgradiënt. Dit begrip van "passieve structuren" leidde tot de ontwikkeling van "passieve" mechanische en biologische klepvervangers.
Het wordt nu duidelijk dat hartkleppen een complexere structuur en functie hebben. De ontwikkeling van een "actieve" hartklepvervanger veronderstelt daarom een aanzienlijke gelijkenis in structuur en functie met de natuurlijke hartklep, wat in de toekomst zeer realistisch is dankzij de ontwikkeling van weefseltechnologie.
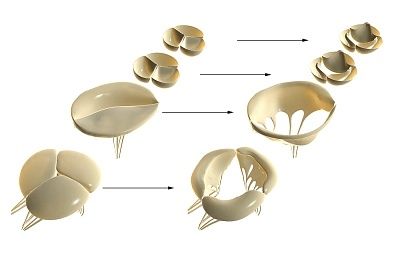
Hartkleppen ontwikkelen zich uit embryonale rudimenten van mesenchymaal weefsel tijdens de vorming van het endocard. Tijdens de morfogenese worden het atrioventriculaire kanaal (tricuspidalis- en mitralisklep) en de ventriculaire uitstroombaan (aorta- en pulmonalisklep) gevormd.
Hoe zijn hartkleppen gerangschikt?
De studie van de bloedtoevoer naar de hartkleppen werd geïnitieerd door N. Luschka (1852), die de hartvaten injecteerde met een contrastmassa. Hij ontdekte talrijke bloedvaten in de kleppen van de atrioventriculaire en halvemaanvormige kleppen van de aorta en de longslagader. Tegelijkertijd bevatten een aantal handboeken over pathologische anatomie en histologie aanwijzingen dat onveranderde menselijke hartkleppen geen bloedvaten bevatten, en dat deze laatste alleen in de kleppen voorkomen bij verschillende pathologische processen - atherosclerose en endocarditis van verschillende etiologieën. Informatie over de afwezigheid van bloedvaten was voornamelijk gebaseerd op histologisch onderzoek. Er werd aangenomen dat bij afwezigheid van bloedvaten in het vrije deel van de kleppen, hun voeding plaatsvindt door filtering van vloeistof uit het bloedplasma dat de kleppen wast. Penetratie van enkele vaten, samen met vezels van dwarsgestreept spierweefsel, in de basis van de kleppen en peeskoorden werd opgemerkt.
Bij injectie van de bloedvaten van het hart met verschillende kleurstoffen (Oost-Indische inkt in gelatine, bismut in gelatine, waterige suspensie van zwarte Oost-Indische inkt, oplossingen van karmijn of trypaanblauw) werd echter vastgesteld dat de bloedvaten de atrioventriculaire hartkleppen, de aortakleppen en de longslagader binnendringen, samen met het hartspierweefsel, maar net niet de vrije rand van de klep bereiken.
In het losse, vezelige bindweefsel van de klepslippen van de atrioventriculaire klep werden afzonderlijke hoofdvaten gevonden die verbonden waren met vaten in aangrenzende delen van het dwarsgestreepte hartspierweefsel.
Het grootste aantal bloedvaten bevond zich aan de basis van de kleppen en een relatief klein aantal in het vrije gedeelte.
Volgens KI Kulchitsky et al. (1990) bevindt zich in de mitralisklep een grotere diameter van arteriële en veneuze vaten. Aan de basis van de cuspen van deze klep bevinden zich voornamelijk de hoofdvaten met een smal lusvormig netwerk van capillairen, dat doordringt tot in het basale deel van de cusp en 10% van het oppervlak inneemt. In de tricuspidalisklep hebben de arteriële vaten een kleinere diameter dan in de mitralisklep. In de cuspen van deze klep bevinden zich voornamelijk verspreide vaten en relatief brede lussen van bloedcapillairen. In de mitralisklep wordt de voorste cusp intensiever van bloed voorzien, in de tricuspidalisklep - de voorste en achterste cuspen, die de belangrijkste sluitfunctie vervullen. De verhouding van de diameters van de arteriële en veneuze vaten in de atrioventriculaire kleppen van het hart van volwassen mensen is 1:1,5. De capillaire lussen zijn polygonaal en liggen loodrecht op de basis van de klepslippen. De vaten vormen een planair netwerk onder het endotheel aan de atriale zijde. Bloedvaten bevinden zich ook in de peeskoorden, waar ze vanuit de papillairspieren van de rechter- en linkerventrikel binnendringen op een afstand van maximaal 30% van de lengte van de peeskoorden. Talrijke bloedvaten vormen boogvormige lussen aan de basis van de peeskoorden. De hartkleppen van de aorta en de truncus pulmonalis verschillen aanzienlijk van de atrioventriculaire kleppen in termen van bloedtoevoer. De hoofdvaten met een relatief kleinere diameter naderen de basis van de halvemaanvormige lussen van de aorta- en truncus pulmonaliskleppen. De korte takken van deze vaten eindigen in capillaire lussen met een onregelmatige ovale en polygonale vorm. Ze bevinden zich voornamelijk nabij de basis van de halvemaanvormige lussen. De veneuze vaten aan de basis van de aorta- en pulmonalisklep hebben ook een kleinere diameter dan die aan de basis van de atrioventriculaire kleppen. De verhouding tussen de diameters van de arteriële en veneuze vaten in de aorta- en pulmonalisklep van het hart van volwassen mensen is 1:1,4. Korte zijtakken ontspringen aan de grotere vaten en eindigen in lussen van haarvaten met onregelmatige ovale en veelhoekige vormen.

Met de leeftijd treedt er een vergroving van bindweefselvezels op, zowel collageen als elastisch, en een afname van de hoeveelheid los, vezelig, ongevormd bindweefsel. Er ontstaat sclerose van het weefsel van de atrioventriculaire klepslippen en de halvemaanvormige slippen van de aorta- en pulmonalisklep. De lengte van de dwarsgestreepte hartspiervezels in de kleppen neemt af, en daardoor neemt het aantal bloedvaten dat de hartkleppen binnendringt af. Door deze veranderingen verliezen de hartkleppen hun elastische en veerkrachtige eigenschappen, wat van invloed is op het klepsluitingsmechanisme en de hemodynamiek.
De hartkleppen hebben netwerken van lymfecapillairen en een klein aantal lymfevaten die zijn uitgerust met kleppen. De lymfecapillairen van de cuspen hebben een karakteristiek uiterlijk: hun lumen is zeer ongelijk, dezelfde capillair heeft op verschillende plaatsen een verschillende diameter. Op plaatsen waar meerdere capillairen samenkomen, worden uitzettingen gevormd - lacunes van verschillende vormen. De lussen van de netwerken zijn vaak onregelmatig veelhoekig, minder vaak ovaal of rond. Vaak zijn de lussen van de lymfenetwerken niet gesloten en eindigen de lymfecapillairen blind. De lussen van de lymfecapillairen zijn meestal georiënteerd in de richting van de vrije rand van de cusp naar de basis. In sommige gevallen werd een tweelaags netwerk van lymfecapillairen gevonden in de cuspen van de atrioventriculaire klep.
De endocardiale zenuwplexussen bevinden zich in verschillende lagen, voornamelijk onder het endotheel. Aan de vrije rand van de klepslippen bevinden de zenuwvezels zich voornamelijk radiaal en verbinden ze zich met die van de peeskoorden. Dichter bij de basis van de slippen vormt zich een fijnmazige zenuwplexus, die aansluit op de plexus rond de vezelachtige ringen. Op de halvemaanvormige slippen is het endocardiale zenuwnetwerk dunner. Op de plaats van aanhechting van de kleppen wordt het dichter en meerlagig.
Celstructuur van hartkleppen
Interstitiële cellen in de hartkleppen, verantwoordelijk voor het behoud van de structuur van de klep, zijn langwerpig van vorm met talrijke fijne uitlopers die zich door de hele klepmatrix uitstrekken. Er zijn twee populaties interstitiële cellen in de hartkleppen die verschillen in morfologie en structuur; de ene heeft contractiele eigenschappen en wordt gekenmerkt door de aanwezigheid van contractiele fibrillen, de andere heeft secretoire eigenschappen en heeft een goed ontwikkeld endoplasmatisch reticulum en Golgi-apparaat. De contractiele functie is bestand tegen hemodynamische druk en wordt verder ondersteund door de productie van contractiele eiwitten in zowel het hart als het skelet, waaronder de zware ketens van alfa- en bèta-myosine en verschillende isovormen van troponine. Contractie van het hartklepblad is aangetoond als reactie op een aantal vasoactieve stoffen, wat suggereert dat een gecoördineerde biologische stimulus een succesvolle klepfunctie bevordert.
Interstitiële cellen zijn ook essentiële componenten van het reparatiesysteem van structuren zoals hartkleppen. De constante beweging van de klepbladen en de bijbehorende vervorming van het bindweefsel veroorzaken schade, waarop de interstitiële cellen van de klep reageren om de integriteit van de klep te behouden. Het reparatieproces lijkt essentieel te zijn voor een normale klepfunctie, en de afwezigheid van deze cellen in huidige kunstmatige klepmodellen draagt waarschijnlijk bij aan de structurele schade van bioprothesen.
Een belangrijk onderzoeksgebied in interstitiële cellen is de studie van interacties tussen deze cellen en de omliggende matrix, gemedieerd door focale adhesiemoleculen. Focale adhesies zijn gespecialiseerde interactieplaatsen tussen cellen en de matrix die het celcytoskelet via integrinen verbinden met matrixeiwitten. Ze fungeren ook als signaaltransductieplaatsen en geven mechanische informatie door van de extracellulaire matrix die reacties kan uitlokken, waaronder, maar niet beperkt tot, celadhesie, migratie, groei en differentiatie. Inzicht in de celbiologie van interstitiële klepcellen is essentieel om de mechanismen te ontrafelen waarmee deze cellen met elkaar en hun omgeving interacteren, zodat deze functie kan worden gereproduceerd in kunstmatige kleppen.
In verband met de ontwikkeling van een veelbelovende richting in de weefselengineering van hartkleppen, worden studies van interstitiële cellen uitgevoerd met behulp van een breed scala aan technieken. De aanwezigheid van het celcytoskelet wordt bevestigd door kleuring voor vimentine, desmine, troponine, alfa-actine en gladde spiermyosine, zware ketens van alfa- en bèta-myosine, lichte ketens-2 van cardiale myosine, alfa- en bèta-tubuline. Celcontractiliteit wordt bevestigd door een positieve respons op epinefrine, angiotensine II, bradykinine, carbachol, kaliumchloride en endotheel I. Cellulaire onderlinge relaties worden bepaald door functionele gapinteracties en geverifieerd door micro-injecties met carboxyfluoresceïne. Matrixsecretie wordt vastgesteld door kleuring voor prolyl-4-hydroxylase / collageen type II, fibronectine, chondroïtinesulfaat en laminine. Innervatie wordt tot stand gebracht door de nabijheid van motorische zenuwuiteinden, wat tot uiting komt in de activiteit van neuropeptide Y tyrosinehydroxylase, acetylcholinesterase, vasoactief intestinaal polypeptide, substance-P, capsicum-gen-gerelateerd peptide. Mitogene factoren worden geschat met behulp van bloedplaatjes-afgeleide groeifactor, basische fibroblastgroeifactor en serotonine (5-HT). De bestudeerde interstitiële celfibroblasten worden gekenmerkt door een onvolledige basaalmembraan, lange, dunne cytoplasmatische uitlopers, nauwe verbinding met de matrix, goed ontwikkelde onregelmatige endoplasmatisch reticulum en Golgi-apparaat, rijkdom aan microfilamenten en de vorming van adhesieve verbindingen.
Endocardcellen in de hartkleppen vormen een functionele atrombogene omhulling rond elke hartklep, vergelijkbaar met het vasculaire endotheel. De veelgebruikte methode van klepvervanging elimineert de beschermende functie van het endocard, wat kan leiden tot afzetting van bloedplaatjes en fibrine op kunstmatige kleppen, de ontwikkeling van bacteriële infecties en weefselverkalking. Een andere waarschijnlijke functie van deze cellen is de regulatie van de onderliggende interstitiële cellen in de hartkleppen, vergelijkbaar met de regulatie van gladde spiercellen door het endotheel. Er bestaan complexe interacties tussen het endotheel en aangrenzende cellen, deels gemedieerd door oplosbare factoren die door de endotheelcellen worden afgescheiden. Deze cellen vormen een enorm oppervlak bedekt met micro-uitsteeksels aan de luminale zijde, waardoor de blootstelling aan en mogelijke interactie met metabole stoffen in het circulerende bloed toeneemt.
Het endotheel vertoont vaak morfologische en functionele verschillen veroorzaakt door schuifspanningen op de vaatwand als gevolg van de bloedstroom. Dit geldt ook voor de endocardiale cellen in de hartkleppen, die een langwerpige of polygonale vorm aannemen. Veranderingen in de celstructuur kunnen optreden als gevolg van de werking van lokale hemodynamica op componenten van het celcytoskelet of secundaire effecten veroorzaakt door veranderingen in de onderliggende extracellulaire matrix. Op ultrastructureel niveau bezitten endocardiale cellen in de hartkleppen intercellulaire verbindingen, plasmavesikels, een ruw endoplasmatisch reticulum en een Golgi-apparaat. Hoewel ze zowel in vivo als in vitro von Willebrand-factor produceren, missen ze Weibel-Palade-lichaampjes (specifieke granula die von Willebrand-factor bevatten), organellen die kenmerkend zijn voor het vasculaire endotheel. Endocardiale cellen in de hartkleppen worden gekenmerkt door sterke verbindingen, functionele gap-interacties en overlappende marginale plooien.
Endocardcellen behouden hun metabole activiteit, zelfs in vitro: ze produceren von Willebrandfactor, prostacycline en stikstofoxidesynthase, vertonen angiotensine-converterend enzymactiviteit en scheiden intensief adhesiemoleculen ICAM-1 en ELAM-1 uit, die belangrijk zijn voor de binding van mononucleaire cellen tijdens de ontwikkeling van een immuunrespons. Al deze markers moeten in aanmerking worden genomen bij het kweken van een ideale celcultuur voor het creëren van een kunstmatige hartklep met behulp van tissue engineering, maar het immuunstimulerende potentieel van hartklepcellen zelf kan hun gebruik beperken.
De extracellulaire matrix van de hartkleppen bestaat uit vezelachtige collageen- en elastinemacromoleculen, proteoglycanen en glycoproteïnen. Collageen maakt 60% van het droge gewicht van de klep uit, elastine 10% en proteoglycanen 20%. De collageencomponent zorgt voor de belangrijkste mechanische stabiliteit van de klep en wordt vertegenwoordigd door collageen van type I (74%), II (24%) en V (2%). Bundels collageendraden worden omgeven door een elastinemantel, die de interacties tussen de draden medieert. De glycosaminoglycaanzijketens van proteoglycaanmoleculen hebben de neiging een gelachtige substantie te vormen waarin andere matrixmoleculen interacteren om permanente verbindingen te vormen en andere componenten worden afgezet. Glycosaminoglycanen van menselijke hartkleppen bestaan voornamelijk uit hyaluronzuur, in mindere mate uit dermatansulfaat, chondroïtine-4-sulfaat en chondroïtine-6-sulfaat, met een minimale hoeveelheid heparinesulfaat. De remodellering en vernieuwing van matrixweefsel worden gereguleerd door matrixmetalloproteïnasen (MMP's) en hun weefselremmers (TI's). Deze moleculen zijn ook betrokken bij een breder scala aan fysiologische en pathologische processen. Sommige metalloproteïnasen, waaronder interstitiële collagenasen (MMP-1, MMP-13) en gelatinasen (MMP-2, MMP-9) en hun weefselremmers (TI-1, TI-2, TI-3), worden in alle hartkleppen aangetroffen. Overmatige productie van metalloproteïnasen is kenmerkend voor pathologische aandoeningen van de hartklep.
 [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Hartkleppen en hun morfologische structuur
Hartkleppen bestaan uit drie morfologisch verschillende en functioneel belangrijke lagen van de klepmatrix: vezelig, sponsachtig en ventriculair.
De vezellaag vormt een belastingsbestendig raamwerk voor het klepblad, bestaande uit lagen collageenvezels. Deze vezels zijn radiaal geplooid, zodat de arteriële kleppen kunnen uitrekken bij het sluiten. De vezellaag bevindt zich nabij het uitgaande buitenoppervlak van deze kleppen. De vezellaag van de atrioventriculaire kleppen dient als een voortzetting van de collageenbundels van de chordae tendineae. Deze laag bevindt zich tussen de sponsachtige (inlaat) en ventriculaire (uitlaat) lagen.
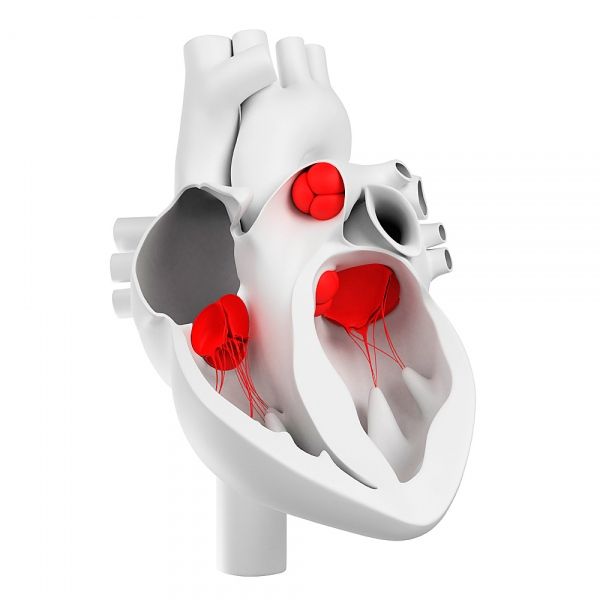
Tussen de vezelachtige en ventriculaire laag bevindt zich de sponsachtige laag (spongiosa). De sponsachtige laag bestaat uit slecht georganiseerd bindweefsel in een viskeus medium. De dominante matrixcomponenten van deze laag zijn proteoglycanen met willekeurig georiënteerd collageen en dunne laagjes elastine. De zijketens van proteoglycaanmoleculen dragen een sterke negatieve lading, wat hun vermogen om water te binden en een poreuze matrixgel te vormen beïnvloedt. De sponsachtige laag van de matrix vermindert de mechanische spanning in de hartklepbladen en behoudt hun flexibiliteit.
De ventriculaire laag is veel dunner dan de andere lagen en is rijk aan elastische vezels die het weefsel in staat stellen constante vervorming te weerstaan. Elastine heeft een sponsachtige structuur die collageenvezels omgeeft en verbindt en deze in een neutrale, gevouwen toestand houdt. De inlaatlaag van de klep (ventriculair voor arteriële kleppen en sponsachtig voor atrioventriculair) bevat meer elastine dan de uitlaatlaag, wat zorgt voor demping van de hydraulische schok wanneer de kleppen sluiten. Deze verhouding tussen collageen en elastine zorgt ervoor dat de kleppen tot 40% kunnen uitrekken zonder stabiele vervorming. Bij blootstelling aan een kleine belasting worden de collageenstructuren van deze laag georiënteerd in de richting van de belasting, waardoor de weerstand tegen verdere belastingsgroei toeneemt.
Het idee dat hartkleppen eenvoudige endocardiale duplicaties zijn, is dus niet alleen vereenvoudigd, maar ook fundamenteel onjuist. Hartkleppen zijn complexe organen met dwarsgestreepte spiervezels, bloed- en lymfevaten en zenuwelementen. Zowel in hun structuur als in hun werking zijn de kleppen integraal onderdeel van alle hartstructuren. Analyse van de normale klepfunctie moet rekening houden met de cellulaire organisatie ervan, evenals met de interactie van cellen met elkaar en de matrix. De kennis die uit dergelijke studies is verkregen, is leidend bij het ontwerp en de ontwikkeling van klepprothesen met behulp van weefselengineering.

