Medisch expert van het artikel
Nieuwe publicaties
Azoöspermie
Laatst beoordeeld: 07.06.2024

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
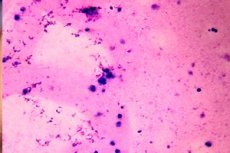
Wanneer de analyse van het ejaculaat van een man de afwezigheid van spermatozoa onthult, wordt dit azoospermie genoemd. De oorzaken van deze aandoening kunnen verschillen: van primaire en secundaire gonadale insufficiëntie (cryptorchidisme, degeneratie van het epitheel van de testiculaire tubuli, hyporchidisme, enz.) Naar andere mechanische barrières die het transport van sperma kunnen blokkeren van de testikels naar de zaadbladen. De kwaliteit van het libido mag niet worden beïnvloed. Azoospermie wordt gediagnosticeerd door herhaald microscopisch onderzoek van sperma. [1] ]
Therapie is op lange termijn, pathogenetisch.
Epidemiologie
Onvruchtbaarheid bij mannen is het onvermogen om een vrouw te bemesten. Tot op heden hebben artsen de resultaten van talloze studies, volgens welke in 40% van de onvruchtbare huwelijken de "dader" van het onvermogen om zwanger te worden, een man is. Een andere indicator voor statistieken: ongeveer 15-20% van de huwelijken heeft vergelijkbare problemen in verband met onvruchtbaarheid.
Het moderne concept van "onvruchtbaar huwelijk" houdt in dat echtgenoten niet in staat zijn om 12-24 maanden van regelmatige seksuele activiteit te bedenken zonder het gebruik van anticonceptie.
Het vermogen van een man om een vrouw te impregneren wordt bepaald door de eigenschappen van zijn zaadvloeistof en het aantal en de kwaliteit van het sperma daarin. Het ejaculaat is een gemengde secretie van de testikels en aanhangsels, evenals het kliersysteem dat wordt vertegenwoordigd door de zaadblaasjes, prostaat, Littre's en Cooper's klieren. Stermatische vloeistof is alkalisch in reactie, waarbij pH fluctueert tussen 7,0 en 7,6. Binnen dit bereik is sperma het meest comfortabel reizen. Bovendien maakt een alkalische omgeving sperma bestand tegen de zure vaginale omgeving (de gemiddelde pH in de vagina is 4,5 en is in het cervicale kanaal 7,5).
Volgens de statistieken wordt azoospermie gediagnosticeerd bij ongeveer 2% van de onvruchtbare paren.
Oorzaken Azoöspermie
Azoospermia gaat vergezeld van een schending van de vorming van sperma, waardoor de zaadvloeistof geen sperma bevat. Afhankelijk van de onderliggende oorzaken, onderscheiden experts een obstructieve en niet-obstructieve variant van pathologie.
Azoospermie houdt het verlies van het vermogen van een man in om op natuurlijke wijze zwanger te worden, en voor sommige patiënten zijn geassisteerde reproductieve technologieën ook niet succesvol.
Azoospermia kan obstructief en niet-obstructief begin hebben. In het eerste geval is de oorzaak de blokkade van de spermakanalen, en in het tweede geval is de directe productie van sperma aangetast. [2]
Problemen met sperma transport kunnen optreden vanwege de volgende redenen:
- Infectieuze en inflammatoire processen die het mannelijke reproductieve systeem beïnvloeden en het vermogen van een man om te bemesten negatief beïnvloeden;
- Traumatisch letsel, chirurgische interventies in de wervelkolom (lumbosacrale gebied), buikholte, genitale organen;
- Dilatatie en uitbreiding van de scrotale veneuze vaten (Varicocele );
- Specifieke anticonceptiemethoden zoals vasectomie -een procedure waarin de ejaculatiekanalen worden gesneden en vastgebonden;
- Aangeboren afwezigheid of fusie van de spermatische kanalen.
Niet-obstructief type azoospermie is niet gerelateerd aan de blokkade van sperma-uitscheiding, maar heeft te maken met de verstoring van de spermaproductie in het lichaam. De oorzaken die een dergelijke storing uitlokken, zijn als volgt:
- Het innemen van bepaalde medicijnen - met name antibiotica, steroïde hormonen en chemotherapie;
- Alcoholmisbruik, roken en drugsgebruik;
- Ongunstige erfelijkheid (bijv. klinefelter of kallman Syndromen);
- Hormonale onbalans die de testiculaire functionaliteit beïnvloedt;
- Retrograde ejaculatie, waarin sperma in de blaas valt in plaats van de urethra (komt voor de achtergrond van ruggenmergletsels, diabetes mellitus, enz.);
- Blootstelling aan radioactieve straling, radiotherapie;
- Ernstige of langdurige verhoging van de lichaamstemperatuur, chronische intoxicatie, vergiftiging door pesticiden, zware metalen;
- Testiculair falen.
Risicofactoren
Aangezien stoornissen van spermatogenese en azoöspermie vrij veel voorkomende problemen zijn bij mannen, hebben wetenschappers een onderzoek gestart waarin ze in staat waren om basisrisicofactoren voor de ontwikkeling van mannelijke onvruchtbaarheid te identificeren:
- Slechte gewoonten (roken, alcohol drinken);
- Onjuist dieet (consumptie van voornamelijk vet, zout en kruidig voedsel);
- Beroepsrisico's gedurende vijf jaar of meer (hoge en te lage temperatuur blootstelling, gasachtige en stoffige lucht, chemische intoxicatie);
- Ongunstige omgevingscondities;
- Het negeren van ziekten, vroegtijdig zoeken naar medische hulp, chronicisatie van pathologieën;
- Hypodynamie, overwegend zittende en zittende levensstijl;
- Overmatige psycho-emotionele stress, frequente conflicten, zorgen, angsten;
- Overmatige oefening.
Een van de leidende factoren bij de ontwikkeling van azoospermie wordt beschouwd als een ongezonde levensstijl van moderne vertegenwoordigers van de sterkere seks. Schadelijke gewoonten hebben een nogal uitgesproken negatieve impact op de gezondheid en reproductieve capaciteit van mannen, en nog meer in combinatie met andere bestaande factoren. [3]
Risicogroepen kunnen zijn:
- Patiënten die een geschiedenis hebben van seksueel overdraagbare infecties;
- Mannen die zijn blootgesteld aan ioniserende stralen of chemisch actieve stoffen;
- Personen wiens directe familieleden hebben geleden aan hormonale aandoeningen;
- Mannen met een geschiedenis van traumatisch letsel aan het externe genitale systeem.
Pathogenese
Azoospermia wordt in het algemeen uitgelokt door een van de drie basisoorzaken:
- Verminderde functie van de kanalen waardoor sperma wordt uitgescheiden.
- Verminderde testiculaire functionaliteit.
- Andere ziekten en voorwaarden.
De eerste oorzaak, verstoorde outputkanalen, is te wijten aan factoren zoals:
- Traumatische ruggenmergletsels, waarin er een ontslag van sperma-secretie is in de blaasholte;
- Prostaatoperaties (chirurgische behandeling van prostatitis, prostaatadenomen, enz.);
- Diabetes;
- Infectieuze inflammatoire pathologieën zoals tuberculose of geslachtsziekten;
- Genetische pathologieën vergezeld van metabolisch falen (bijv. Cystische fibrose);
- Aangeboren defecte afwijkingen van de VAS-uitspellen.
De tweede oorzaak, verminderde testiculaire functionaliteit, is een gevolg:
- Van niet-ingediende testikels (cryptorchidisme);
- Van lage mannelijke geslachtshormoonproductie;
- Traumatische en andere testiculaire laesies;
- Blootstelling aan straling, slechte gewoonten;
- Ontstekingsreacties met betrekking tot het testiculaire gebied;
- SOA's, orchitis;
- Genetische defecten, aangeboren anomalieën.
Naast andere pathologieën die de ontwikkeling van azoöspermie kunnen veroorzaken, noemen experts dergelijke ziekten:
- Een laesie van de hypothalamus, het hersengebied dat de productie van geslachtshormonen regelt;
- Laesie van de hypofyse - een afdeling "ondergeschikt" aan de hypothalamus, die kan worden beïnvloed als gevolg van langdurige intoxicatie (inclusief alcohol en drugs), tumorprocessen en bloedingen.
Het proces van spermatogenese is de vorming en rijping van spermatozoa: het begint in de puberteit en duurt tot de ouderdom. Mannelijke geslachtscellen worden gevormd in de kronkelige testiculaire zaadkanalen. Dit gebeurt opeenvolgend: van de proliferatie van spermatogoniums tot de processen van meiose en spermiogenese. De piekactiviteit van het proces wordt waargenomen bij een temperatuurregime van ongeveer 34 ° C. Een dergelijk regime wordt gehandhaafd, vanwege de anatomische lokalisatie van de testes, niet in de buikholte, maar in het scrotum. De spermatozoa rijpt volledig in het testiculaire aanhangsel. De hele cyclus van spermasvorming in het mannelijke lichaam duurt ongeveer 74 dagen.
Symptomen Azoöspermie
Het belangrijkste teken van azoospermie is het onvermogen van een paar om een kind te verwekken. In de regel is het met dit probleem dat mannen medische hulp zoeken, omdat in het algemeen de seksuele functie meestal niet wordt aangetast. Andere symptomen kunnen alleen verschijnen als ze worden veroorzaakt door de belangrijkste, primaire ziekte. Bijvoorbeeld, onvoldoende testiculaire functie - hypogonadisme - wordt gemanifesteerd door onderontwikkeling van het secundaire seksuele beeld, dat wordt gemanifesteerd door onderbelicht haar, vrouwelijk lichaamstype, gynaecomastie. Secretorische azoöspermie wordt vaak gedetecteerd tegen de achtergrond van testiculaire hypoplasie, verminderd seksueel vermogen, erectiestoornissen, klein penissyndroom.
Verschillende soorten obstructieve azoöspermie worden soms gepaard met een gevoel van ongemak, pijn trekken in het genitale gebied, zwelling of zwelling van het scrotum. Palpatorische stoornissen van de testikels worden vaak niet gedetecteerd, maar de aanhangsels kunnen worden vergroot - vanwege de accumulatie van mannelijke kiemcellen erin. Obstructie komt vaak tegelijkertijd voor met retrograde ejaculatie.
In de overgrote meerderheid van de gevallen merkt een man die lijdt aan azoospermie geen pathologische tekenen op. De eerste "bel" verschijnt wanneer de echtgenoten beginnen met het plannen van een zwangerschap, maar regelmatige onbeschermde seksuele contacten leiden niet tot het langverwachte resultaat: de vrouw wordt niet zwanger.
Artsen onderscheiden een aantal symptomen waaraan aandacht moeten worden besteed, omdat ze de aanwezigheid van storingen kunnen aangeven lang voordat de patiënt mannelijke onvruchtbaarheid en azoospermie vermoedt:
- Milde intermitterende pijn in het liesgebied;
- Zwelling, zwelling in het scrotale gebied;
- Verzwakking van erecties en libido;
- Een constant gevoel van vermoeidheid;
- Zwelling, vergroting van de borstklieren (gynaecomastie);
- Chronische en frequente besmettelijke processen;
Slechte haargroei in het gezicht en het lichaam, evenals andere tekenen van een waarschijnlijke afname van de productie van mannelijke geslachtshormonen.
Sperma in azoospermie
Semen evaluatie wordt als volgt uitgevoerd:
- Normosemia - 1 tot 6 ml sperma-vloeistof.
- Multisemia - Het volume sperma-vloeistof is groter dan 6 ml.
- Normospermia - Het aantal mannelijke geslachtscellen per 1 ml sperma is 60-120 miljoen.
- Polyspermie - Het aantal mannelijke geslachtscellen per 1 ml sperma-vloeistof is groter dan 120 miljoen.
- Aspermie - spermatozoa en spermatogenese cellen zijn afwezig.
- Oligozoospermia - Het aantal mannelijke geslachtscellen in de sperma-vloeistof is niet meer dan 20 miljoen per 1 ml.
- Hypospermie - Het aantal sperma ligt tussen 20 en 60 miljoen sperma per 1 ml.
- Azoospermia - spermatozoa zijn afwezig in het sperma, maar onrijpe vormen van spermatogenese zijn aanwezig.
Vormen
Azoospermia is een soort onvruchtbaarheid bij mannen waarin spermatozoa niet wordt gedetecteerd in de ejaculaatanalyse. Andrologen en urologen wijzen op de aanwezigheid van verschillende vormen van abnormale spermatogenese: het is niet alleen azoospermie, maar ook oligozoospermie, asthenozoospermia, Teratozoospermia.
Bovendien is een combinatie van pathologieën mogelijk - bijvoorbeeld diagnoses zoals oligoasthenozoospermie, asthenoteratozoöspermie, oligoteratozoospermie, etc. worden vaak aangetroffen.
Asthenozoospermie |
De aanwezigheid van minder dan de helft van de spermatozoa met type I (progressieve lineaire) en type II (langzame lineaire of progressieve niet-lineaire) beweging, of de aanwezigheid van minder dan 25% van de cellen met type I-beweging. Het aantal en de vorm van mannelijke kiemcellen liggen binnen normale limieten. |
Oligozoospermie |
Een afname van het aantal levende mannelijke kiemcellen - minder dan 20 miljoen per 1 ml zaadvloeistof. |
Teratozoospermia |
Meer dan 50% van de mannelijke kiemcellen wordt gekenmerkt door afwijkingen in structuur (hoofd en staart). |
Azoospermia |
Geen sperma in de sperma-secretie. |
Volgens de etiologische (causale) factor verdelen specialisten dergelijke soorten overtreding:
- Niet-obstructieve azoospermie is een aandoening die niet wordt geassocieerd met belemmering van het zaadkanaal. De pathologie is meestal een secretoire type stoornis.
- Obstructieve azoospermie wordt geassocieerd met obstructie van de doorgang van de zaadkanalen. Dit leidt tot het feit dat mannelijke geslachtscellen niet van de testikels naar het seksuele orgaan kunnen komen. Deze variant van azoospermie treedt in 40% van de gevallen voor. Ductale obstructie kan worden verkregen of aangeboren.
- Obturator azoöspermie wordt veroorzaakt door obstructie van de spermatische kanalen. Deze pathologie kan het resultaat zijn van volledige of gedeeltelijke aplasie van de aanhangsels, kanalen of zaadblaasjes, verkregen obstructie van de kanalen als gevolg van post-inflammatoire obstructie, cystische en tumorprocessen die het kanaal van het aanhangsel comprimeren. Iatrogene obstructie als gevolg van chirurgische interventies in dit gebied is ook mogelijk.
- Secretoire azoöspermie gaat gepaard met een verminderde spermavorming als gevolg van bilateraal cryptorchidisme, epidparotitis, tumorprocessen, straling of toxische effecten.
- Tijdelijke azoospermie is een tijdelijke toestand waarin sperma niet altijd afwezig is in de baanbrekende secretie, maar alleen periodiek. De aandoening wordt bijvoorbeeld opgemerkt bij de verergering van bepaalde ziekten, na ernstige stress, tegen de achtergrond van de behandeling met bepaalde geneesmiddelen (hormonen, antibiotica, chemotherapie-medicijnen). Tijdelijke storing treedt vaak op als een man het bezoeken van baden en sauna's misbruikt, of te vaak geslachtsgemeenschap heeft.
- Genetische azoospermie wordt veroorzaakt door een erfelijke factor en is een aangeboren pathologie. De oorzaken zijn numerieke of structurele afwijkingen van geslachtschromosomen. Dragers van CFTR-genmutatie (cystische fibrose) hebben vaak obstructieve azoöspermie geassocieerd met de afwezigheid of obstructie van de zaadkanalen. [4]
- Conggenitale azoospermie, die zich ontwikkelt in de foetus tijdens de ontwikkeling van de foetus, kan worden veroorzaakt door hypopituïtarisme, Cullman of Prader-Willi-syndromen, andere aandoeningen die resulteren in gonadotropine of GNRH-deficiëntie en Klinefelter-syndroom. Meer dan 10% van de patiënten met gediagnosticeerde azoöspermie heeft abnormale spermatogenese vanwege een afwijking van het Y-chromosoom. Dergelijke afwijkingen strekken zich meestal uit tot de lange arm van het chromosoom: deze sectie wordt door specialisten aangeduid als AZF (azoospermia-factor).
Volgens de etiologische factor worden dergelijke vormen van azoöspermie onderscheiden:
- De pretesticulaire vorm wordt geassocieerd met hormonale storingen en vertegenwoordigt een secundair gebrek aan testiculaire functie.
- Testiculaire vorm is een primaire testiculaire disfunctie vanwege een afwijking van de testikels zelf.
- De post-testiculaire vorm is te wijten aan verminderde ejaculatie of blokkade van de ejaculatiekanalen.
De eerste en derde vormen van de ziekte zijn het gemakkelijkst te behandelen. Testiculaire variant is vaak onomkeerbaar (uitzondering - varicocele).
Complicaties en gevolgen
Azoospermia zelf wordt al beschouwd als een complicatie van infectieuze inflammatoire, endocriene aandoeningen die het urogenitale systeem beïnvloeden.
Wat kan echter azoospermie blijken, als u de pathologie niet behandelt?
Vaak heeft de samenleving een stereotiepe denken: als er geen kinderen in het gezin zijn, is het probleem bij de vrouw. Statistieken zeggen echter heel anders: de gezondheid van vrouwen staat niet toe dat zwanger wordt in slechts 1/3 van de gevallen. Nog eens 1/3 zijn schendingen van de kant van de mannelijke reproductieve gezondheid. De resterende 33% zijn problemen van beide partners tegelijk, of gevallen waarin de reden voor het gebrek aan zwangerschap niet kan worden bepaald. Dus als een vrouw geen zwanger wordt gedurende 1-2 jaar met regelmatige onbeschermde geslachtsgemeenschap, moeten beide partners worden gediagnosticeerd.
Bij sommige mannen wordt azoospermie geactiveerd door ernstige medische aandoeningen die in de loop van de tijd even ernstige complicaties kunnen veroorzaken:
- Ophoping;
- Inflammatoire pathologieën (prostatitis, orchitis, vesiculitis, epididymitis).
Bovendien wordt het onmiddellijke feit van onvermogen om te bedenken vaak de oorzaak van depressieve stoornissen bij mannen, stressvolle situaties, leidt tot familieconflicten en misverstanden.
Mannelijke onvruchtbaarheid met azoospermie
Als er tijdens de diagnose geen mannelijke geslachtscellen in de zaadvloeistof worden gedetecteerd, betekent dit niet dat het mannelijke lichaam helemaal geen dergelijke cellen produceert. Het gebeurt vaak dat de testikels volledig functioneren, maar er is een obstakel op weg naar de uitgang, waardoor het sperma wordt geblokkeerd om de zaadvloeistof in te voeren.
Er is een bepaald drempelaantal sperma dat in de testis moet worden geproduceerd om de cellen het sperma te bereiken. Als spermatozoa in lagere aantallen worden geproduceerd, bereiken ze mogelijk niet het ejaculaat, maar kunnen ze misschien rechtstreeks in de testis aanwezig zijn.
Om de oorzaak van azoöspermie te bepalen en de kans op hervatting van de vruchtbaarheid en verder gebruik van geassisteerde reproductieve methoden te beoordelen, beveelt de arts de patiënt aan om diagnostiek te ondergaan - met name een testiculaire biopsie. Deze procedure helpt vaak om volwassen spermatozoa in de weefsels te vinden en maakt het ook mogelijk om de behandelingstactieken te bepalen.
Diagnostics Azoöspermie
Om te slagen in de behandeling van azoospermie, is het noodzakelijk om de onderliggende oorzaak van de aandoening te identificeren. Het interviewen van de patiënt begint met de verzameling van anamnesis: de arts moet bijvoorbeeld weten over enkele kenmerken van het seksuele leven van de patiënt - de mate en kwaliteit van seksuele activiteit, de duur van de periode waarin het niet mogelijk is om een kind te bedenken. Bovendien worden punten zoals overgedragen of bestaande pathologieën, slechte gewoonten, beroepsmatige intoxicatie, enz. Belangrijke informatie. Vervolgens evalueert de specialist de externe gegevens van de man: de kenmerken van de lichaamsbouw, de toestand van de geslachtsdelen, de mate van secundaire seksuele kenmerken.
In veel diagnostische centra wordt een diagnose van azoöspermie pas gestuurd na ten minste twee microscopische onderzoeken van sperma die de afwezigheid van mannelijke sekscellen bevestigen. Indien nodig worden aanvullende diagnostiek voorgeschreven:
- Prostaat-echografie, zaadblaasjes, testikels, enz.;
- Testiculaire meting met een orchidometer en andere meetapparaten;
- Spermogram (minstens twee keer uitgevoerd met een tijdsinterval van 2-3 weken);
- Een bloedtest met niveaus van follikelstimulerend hormoon (fsh), testosteron, prolactin, remming B;
- Genetische studies (Karyotype, CFTR-gen, AZF-factor).
Bovendien worden tests uitgevoerd om seksueel overdraagbare aandoeningen te bepalen. Niet-obstructieve azoospermie wordt aangegeven als FSH-niveaus stijgen tot 7,6 mf/l of meer, met een algemene stoornis van testiculaire ontwikkeling.
Instrumentale diagnostiek kan worden uitgebreid. Transrectale echografie van de prostaatklier, echografie Doppler-echografie van scrotale vaten worden uitgevoerd.
Het spermogram wordt aangevuld met Mar-testen, die gepaard gaat met een beoordeling van het gehalte aan anti-sperm-antilichamen in het bloed.
Van bijzonder belang is de bepaling van de hormonale status, die helpt bij het beoordelen van de kwaliteit van hypofyse-hypothalamische regulatie van de functionaliteit van de seksklieren.
Zoals we weten, kunnen seksueel overdraagbare aandoeningen ook de kwaliteit van het sperma bij mannen negatief beïnvloeden. Om dergelijke pathologieën uit te sluiten, worden ELISA-, RIF- of polymerase-ketenreactie (PCR) -tests uitgevoerd.
Om de invoer van sperma-vloeistof niet in de urethra maar in de blaas (zogenaamde retrograde ejaculatie) uit te sluiten, wordt een post-ejaculatie urine-onderzoek uitgevoerd.
Testiculaire biopsie voor azoospermie.
Als er geen contra-indicaties zijn, biopsie wordt op de standaard manier uitgevoerd: een punctie van de testiculaire wand wordt gemaakt met een dunne naald, na voorlopige algemene of lokale anesthesie. De hele procedure duurt slechts enkele minuten. Als de anesthesie lokaal was, wordt de patiënt binnen een uur thuis vrijgelaten.
In sommige gevallen is het noodzakelijk om een zogenaamde "open" biopsie uit te voeren: deze methode wordt gebruikt als een grotere hoeveelheid weefsel moet worden genomen voor onderzoek. Tijdens de procedure wordt een huidincisie gemaakt in het scrotum (tot 10 mm) en neemt vervolgens de gewenste hoeveelheid weefsel. De manipulatie wordt voltooid door een of meer hechtingen toe te passen (meestal met behulp van absorbeerbare draden). De patiënt kan na 2-3 uur naar huis gaan of in het ziekenhuis blijven (als verder medisch toezicht vereist is).
De microchirurgische methode van testiculaire biopsie, waarbij een grotere huidincisie in het scrotum wordt aangebracht, wordt minder vaak beoefend. Deze techniek maakt een volledige revisie mogelijk met behulp van een chirurgische microscoop.
Al deze methoden vereisen eenvoudige maar speciale voorbereiding van de patiënt. De arts verzamelt vooraf de resultaten van pre-procedurele tests, bespreekt met de mogelijke methoden voor anesthesie met de anesthesioloog. Hij praat met de patiënt, legt de essentie van de procedure uit, ontdekt of hij implantaten, kunstmatige kleppen, pacemakers heeft, vraagt naar medicijnen, vooral die die het bloed verdunnen (acetylsalicylzuur, warfarine, enz.).
De onmiddellijke voorbereidende fase is als volgt:
- De avond vóór de procedure mag niet te veel eten, is het raadzaam om geen dineren te eten of iets licht te eten (cottage kaas, sommige groenten, enz.);
- Drink of eet niet op de dag van de biopsie;
- Was 's ochtends in de douche, scheer het haar af in het scrotum en de voorste dijbeen.
De tijdens de biopsie verkregen materialen gaan rechtstreeks naar de embryoloog. Hij beoordeelt de kansen van de man om met succes een kind te verwekken, voert aanvullende studies uit, overlegt met een reproductoloog, geneticus.
Cytogenetische studie van het karyotype van een man met azoospermie
Mannen die moeite hebben om zwanger te worden en een somatisch adequaat karyotype hebben, hebben een risico op het ontwikkelen van sperma-aneuploïdie, een verstoring van het chromosoomnummer in de diploïde set, met een frequentie van chromosoomdefecten in de kiemlijn variërend van 6 tot 18%.
Het is moeilijk om de rol van chromosoom Y bij de vorming van sperma te veel te benadrukken. Maar diagnostiek waarmee chromosomale veranderingen kunnen worden gedetecteerd en hun impact op de afname van het aantal mannelijke kiemcellen is momenteel moeilijk. Het is bekend dat de ontwikkeling van onvruchtbaarheid nauw verband houdt met de afwezigheid van chromosoom Y in het genmateriaal.
In azoospermie worden genetische defecten in het Y-chromosoom gevonden in ongeveer 35-50% van de gevallen.
De volgende chromosomale defecten kunnen leiden tot verminderde spermatogenese:
- Chromosoomnummerstoornis (xxy, jjj);
- Structurele chromosomale afwijkingen;
- Chromosomale translocaties.
Karyotype in azoöspermie en andere soortgelijke aandoeningen worden in dergelijke gevallen onderzocht:
- In secretoire azoospermie met verhoogde serum FSH-niveaus;
- In oligospermie met een snelheid van minder dan 5 miljoen sperma per 1 ml sperma;
- Teratozoospermia (aanwezigheid van een groot aantal dode sperma in de sperma-vloeistof).
In azoospermie, een 47, wordt xxy karyotype verandering vaak gedetecteerd: een extra X-chromosoom wordt waargenomen bij patiënten met cryptorchidisme en Klinefelter-syndroom. In alle metafasen wordt een Robertson-translocatie gedetecteerd (chromosoom 13, 14, evenals 47, XY, -13, Rob. T. (13,14).
Vermoedelijk wordt in dergelijke gevallen de translocatie gekenmerkt door late ontwikkeling, omdat er geen bewijs is van aangeboren en erfelijke aard van vruchtbaarheidsstoornissen en chromosomale afwijkingen.
De soorten chromosoomdefecten bij mannen met gediagnosticeerde azoöspermie worden in de tabel weergegeven: [5] ]
Karyotype |
% van de gevallen van patiënten met azoospermie |
46, xy. |
Meer dan 92% |
Chromosomale afwijkingen |
Minder dan 8% |
Classic 47, xxy |
Ongeveer 2% |
Volledige vorm 48, xxyy |
Minder dan 1% |
Mozaïekvariant 46, xy/47, xxy |
Minder dan 1% |
Klinische variant 47, xxy |
Minder dan 1% |
Differentiële diagnose
Karakteristieke kenmerken die worden geïdentificeerd tijdens het onderzoeken van een man met primaire testiculaire disfunctie:
- Onvoldoende uitdrukking van secundaire seksuele kenmerken;
- Gynecomastia;
- Ondermaatse testikel (minder dan 15 cm);
- De testikels zijn dicht of afwezig;
- FSH is verhoogd of binnen het normale bereik.
Obstructieve azoospermie is detecteerbaar:
- Testiculaire volumenorm;
- Vergroting, dichtheid van het aanhangsel, de aanwezigheid van knobbeltjes erin;
- Geschiedenis van chirurgie om neoplasmata in de aanhangsel of sterilisatie te verwijderen;
- Een foto van urethroprostatitis;
- Prostaatdefecten, vergrote zaadblaasjes;
- Endocrien systeem, hormonale balans liggen binnen normale limieten.
In het geval van cryptorchidisme daalt de testikel niet in het scrotum, de tekens kunnen bij de geboorte worden gedetecteerd. Eenzijdige of bilaterale pathologie is mogelijk. Microscopische verkalking van de testis kan zich ontwikkelen, wat een risicofactor wordt voor tumorontwikkeling. [6]
Voor varicocele:
- De groei en ontwikkeling van de testikel is aangetast;
- De veneuze vaten van het zaadkanaal worden hoofdzakelijk aan de linkerkant verwijd;
- Er is pijn en ongemak in de testikel.
Azoospermia |
Varicocele |
|
Externe inspectie |
De testikels zijn in grootte, inelastisch verminderd. |
Varicose verwijde veneuze vaten van het zaadkanaal zijn aanwezig. Positieve Valsalva-test. |
Ultrasond |
Veranderingen in de structuur van de testikels en aanhangsels worden opgemerkt. |
Variik verwijde veneuze vaten van de gebunde plexus worden gevisualiseerd. |
Spermogramresultaten |
Tekenen van azoospermie. |
Tekenen van asthenozoospermia. |
Met wie kun je contact opnemen?
Behandeling Azoöspermie
De hoofdrichting van de behandeling van azoospermie is het stimuleren van de natuurlijke ontwikkeling van mannelijke kiemcellen. Therapeutische manipulaties kunnen echter verschillen, wat afhangt van de grondoorzaken van de aandoening. [7] meestal beveelt de arts de patiënt aan dergelijke therapeutische technieken aan:
- Hormonale behandeling - omvat het nemen van oestrogeen en LH (luteïniserend hormoon) preparaten om spermatogenese te stimuleren. De duur van een dergelijke therapie wordt op individuele basis voorgeschreven en duurt meestal enkele maanden, tot zes maanden.
- Chirurgische behandeling wordt gebruikt voor obstructieve aandoeningen die azoöspermie uitlokken. Reproductieve functie wordt hersteld na de correctie van de doorgankelijkheid: de chirurg elimineert bijvoorbeeld aangeboren ontwikkelingsdefecten, varicocele enzovoort.
- Sperma-extractie door biopsie wordt uitgevoerd wanneer alle bovenstaande methoden het probleem niet hebben opgelost. Artsen halen actieve spermatozoa uit de zaadkanaalholte en gebruiken ze voor kunstmatige inseminatie.
Patiënten met azoospermie veroorzaakt door pathologieën zoals Varicocele, cryptorchidisme, prostaatcyste, vereisen een operatie.
Als het probleem een gevolg is van ontstekingsprocessen in het reproductieve systeem, wordt de behandeling met ontstekingsremmende geneesmiddelen uitgevoerd.
Verstoring van de hormonale balans wordt gestabiliseerd door geschikte hormoontherapie.
In alle gevallen wordt het behandelingsregime bepaald en afzonderlijk geselecteerd, omdat het belangrijk is om rekening te houden met veel kenmerken van zowel de patiënt als de toestand van zijn gezondheid in het algemeen. Als de behandeling niet het gewenste effect oplevert, is het mogelijk om het paar te helpen door microchirurgie uit te voeren, waardoor mannelijke geslachtscellen kunnen worden verkregen uit testiculair weefsel. Het verkregen biomateriaal wordt geleverd aan embryologen die spermatozoa selecteren voor latere kunstmatige inseminatie. [8]
Is azoospermie te behandelen of niet?
Azoospermie kan worden behandeld als de oorzaak van het probleem kan worden geëlimineerd. Als de pathologie bijvoorbeeld wordt uitgelokt door obstructie - blokkade van het zaadkanaal, wordt een reconstructieve bewerking uitgevoerd, waaronder urethrale plastic, anastomose, chirurgische verwijdering van varicocele, enz.
Behandelingssucces na chirurgische correctie van obstructie wordt in ongeveer 30-55% van de gevallen waargenomen.
Als azoospermie een gevolg was van endocriene, hormonale aandoeningen, wordt de therapie van hormoonvervanging of stimulerende natuur uitgevoerd. Er zijn veel gevallen van volwaardige mannelijke kiemcellen die in het sperma verschijnen na een cursus hormonale therapie.
Als zwangerschap in azoöspermie niet plaatsvindt ondanks alle genomen maatregelen, wordt de patiënt aanbevolen om een reproductoloog te raadplegen voor een kunstmatige inseminatieprocedure - bijvoorbeeld ICSI (sperma-injectie in het cytoplasma). De techniek omvat het verkrijgen van sperma van de testis of aanhangsel door open of aspiratie-biopsie.
In gecompliceerde gevallen, wanneer het als onmogelijk wordt beschouwd om de oorzaak van azoospermie te detecteren en te elimineren, is de enige optie om donorsperma te gebruiken voor conceptie. [9]
Medicijn
In secundair hypogonadisme voor behandeling Gebruik de voorbereidingen van chorion gonadotropin: HCG, Choragon, Pregnyl, Profazi, enz., In een dosering van 2duizend IE drie keer per week. Menotropine wordt ook toegediend in de hoeveelheid van 0,5-1 ampul in de vorm van intramusculaire injecties drie keer per week.
Aanvullende medicijnen:
- Cephalosporine-antibiotica (cefazolin, cefotaxime 1.0 tweemaal per dag;
- Uroseptische middelen van fluorochinolonengroep (ciprofloxacine 250 mg tweemaal per dag);
- Lokale ontstekingsremmende geneesmiddelen (Vitaprost-zetpillen 1 pc. In het rectum in de avond voor het slapengaan);
- Analgetica (ketonaal 2,0 intramusculair, analgin 1.0, nospazine 2.0 intramusculair);
- Geneesmiddelen om microcirculatie te optimaliseren (pentoxifylline 5.0 als een intraveneuze druppel);
- Antimycotische middelen (fluconazol 150 mg eenmaal per dag, intraconazoloplossing);
- Ascorbinezuur 2,0 dagelijks gedurende vier dagen.
De indicator van de positieve dynamiek van de behandeling is het verdwijnen van het trekken van pijnen in het liesgebied, de aanwezigheid van enkele spermatozoa tijdens spermogram, de afwezigheid van ontstekingsprocessen. Spermogram en hormonale tests worden herhaald met een interval van 4 weken.
Tribestan
De behandeling van endocriene vormen van azoospermie wordt vaak uitgevoerd met behulp van de voorbereidingen van de oorsprong van planten. Momenteel is er een bijzondere interesse in fytomedicines, die zowel effectief als veilig zijn. Plantenpreparaten combineren meestal een mild complex effect en de afwezigheid van uitgesproken bijwerkingen, evenals de mogelijkheid van gebruik in combinatie met traditionele geneesmiddelen.
Er zijn een aantal kruidenpreparaten die saponinen bevatten, of zogenaamde steroïde glycosiden, die in staat zijn om de hormonale balans in het mannelijke lichaam zachtjes te reguleren. Het is opmerkelijk dat dergelijke remedies het verstoorde werk van endocriene klieren corrigeren, zonder het normaal functionerende kliersysteem te beïnvloeden.
Een van de middelen in de compositie waarvan saponinen aanwezig zijn, is Tribestan. Het medicijn wordt actief gebruikt om libido- en vruchtbaarheidsstoornissen bij mannen te corrigeren.
De rijke complexe samenstelling van Tribestan biedt meertrapsactie van het medicijn, dat wordt weerspiegeld op het niveau van de hypofyse, seksklieren, bijniercortex. Met behulp van saponinen en sapogeninen wordt de functie van endocriene klieren gestabiliseerd en helpen alkaloïden om bloedvaten te verwijden, de bloedcirculatie in het seksuele systeem te versnellen.
Tribestan beïnvloedt de hormonale balans, heeft een indirect oestrogene effect zonder interfereren met regulatiemechanismen.
Bovendien heeft het medicijn een positief effect op het psycho-emotionele evenwicht, verbetert de toestand van het autonome zenuwstelsel, optimaliseert het welzijn, vermindert vermoeidheid, verhoogt de fysieke en mentale prestaties. Het is belangrijk dat Tribestan veilig, niet-toxisch is, geen functionele en morfologische veranderingen veroorzaakt. Het kan worden gebruikt als monotherapie of in combinatie met hormonale medicijnen.
Mannen met azoospermie worden aanbevolen om drie keer per dag tribestan 1-2 tabletten te nemen, gedurende ten minste drie opeenvolgende maanden. Het therapeutische cursus kan worden herhaald totdat het vereiste positieve effect is bereikt.
In de regel is de behandeling goed verdragen, er zijn geen gevallen van overdosis en uitgesproken bijwerkingen opgemerkt. Allergische reacties werden zelden gedetecteerd.
Spermactine
Wetenschappers hebben ontdekt dat het nemen van medicijnen die antioxidanten en sporenelementen bevatten in veel gevallen helpt om de kansen op bemesting te vergroten en het risico op reproductieve stoornissen vermindert. De meest voorkomende en interesse van de kant van specialisten ontvingen medicatiecomplexen die verschillende soorten stoornissen van spermatogenese (inclusief azoospermie) beïnvloeden. Artsen hebben het effect opgemerkt van spermactine, acetyl-L-carnitine, L-carnitine fumaraat en alfa-lipoïnezuurcomplex op oxidatieve stresswaarden en de mate van DNA-fragmentatie van mannelijke kiemcellen.
Talrijke studies hebben een positieve statistisch significante dynamiek aangetoond van basisspermogramwaarden, in het bijzonder motiliteit en morfologie. Stabiele verbetering werd waargenomen al dichter bij de derde maand van de therapeutische koers. Tegelijkertijd nam het aantal vrije radicalen af. De belangrijkste conclusie werd getroffen: stimulatie van spermatogenese met de complexe voorbereiding spermactine is een effectieve en veilige manier om mannelijke reproductieve functie te corrigeren.
Het medicijn wordt 's ochtends meteen na het ontbijt één zakje (10 g) genomen. Het poeder moet worden verdund in 150-200 ml water of sap (melk, hete thee en alcoholbevattende drankjes zijn niet geschikt).
In zeldzame gevallen kan spermactine een individuele overgevoeligheidsreactie veroorzaken. Als dit gebeurt, wordt de complexe remedie geannuleerd en vervangen door andere, meer geschikte medicijnen.
Selzinc
Voor voldoende functioneren van het mannelijke reproductieve systeem is het belangrijk om een fysiologisch niveau van concentratie van vitamines en sporenelementen te handhaven die deelnemen aan biochemische reacties en hun katalysatoren zijn. Sommige essentiële micronutriënten worden geproduceerd door de mannelijke reproductieve organen. De belangrijkste elementen voor normale vruchtbaarheid worden beschouwd als zink- en seleniumionen.
Tegenwoordig hebben veel patiënten vitamine- en micro-element-tekort in het lichaam. In het bijzonder wordt dit geassocieerd met voedingsstoornissen, met veel slechte gewoonten en ongunstige omgevingscondities. Uniforme en beperkte voeding brengt vrij snel een afname van de inname van nuttige stoffen en, bijgevolg, de ontwikkeling van verschillende pathologische aandoeningen.
Zink regelt genexpressie tijdens celproliferatie en differentiatie en is betrokken bij sensibilisatie voor hormonen en groeifactoren. Zinktekort wordt vooral beïnvloed in de vroege fasen van de celcyclus. Het is het tekort dat vertraagde seksuele ontwikkeling veroorzaakt bij adolescenten en verminderde mannelijke vruchtbaarheid. Interessant is dat zink de neiging heeft zich op te hopen in de prostaatklier en dient als een van de ingrediënten van de afgescheiden vloeistof. Het helpt de activiteit van spermoplasmatische enzymen te reguleren, neemt deel aan de processen van coagulatie en liquefactie van zaadvloeistof. De aanwezigheid van zink in mannelijke kiemcellen is de hoogste in het hele organisme en komt neer op 1900 µg/kg.
Een ander sporenelement, Selenium, heeft een beschermend effect tegen biochemisch agressieve vrije radicalen. Selenium is noodzakelijk als een antioxiderende verdediger van celmembranen, stimuleert het werk van andere antioxidanten. In het geval van een tekort aan dit sporenelement ontwikkelt zich mannelijke onvruchtbaarheid, omdat het niet alleen bescherming biedt van mannelijke kiemcellen, maar ook verantwoordelijk is voor hun motiliteit.
Veel studies hebben de effectiviteit van Selzinc bevestigd met betrekking tot spermaconcentratie, motiliteit en morfologie bij mannen die lijden aan vruchtbaarheidsstoornissen. Dit medicijn blijft absoluut veilig, zelfs bij het nemen van twee dagelijkse doses, en er worden geen bijwerkingen en symptomen opgemerkt. Selzinc wordt dagelijks een tablet genomen, gedurende enkele maanden (naar goeddunken van de arts).
Prostagut Forte
Polycomponent kruidenremedie prostagut forte wordt gebruikt voor azoospermie geassocieerd met goedaardige prostaathyperplasie en prostatitis. Het medicijn wordt als absoluut veilig beschouwd en is tegelijkertijd niet inferieur in effectiviteit voor bekende synthetische geneesmiddelen.
De samenstelling van het product wordt weergegeven door een extract van Serenoa kruipende bessen en Sabal Palm, evenals een droog extract van de wortelstok van brandnetel kruipen.
Prostagut Forte wordt gekenmerkt door een uitgesproken ontstekingsremmend, anti-edemateus effect, het vermogen om cellulaire ontwikkeling te remmen door de RNA-productie te onderdrukken. Aanvullende eigenschappen van het medicijn: stimulatie van het zenuwstelsel, remming van testosteronconsumptie door prostaatcellen. De actieve samenstelling van het medicijn helpt bij het verminderen van pijnlijke en brandende sensaties van patiënten tijdens urine-uitscheiding bij goedaardige prostaathyperplasie.
Het medicijn heeft geen rechtstreeks invloed op de genezing van azoospermie.
Capsules van het medicijn worden oraal, in hele vorm, met water genomen. Behandelingsduur - Minstens één maand, één capsule in de ochtend en 's avonds. Prostagut wordt goed verdragen, bijwerkingen in de vorm van onaangename sensaties in het buikgebied treden zelden op. Sommige patiënten kunnen allergie voor het medicijn ontwikkelen.
Wat kan worden geconcludeerd? De Frostagut Forte van het medicijn heeft alleen een effect op de externe manifestaties van aandoeningen, maar direct azoöspermie, evenals de groei van prostaat neoplasmata, deze medicatie kan niet genezen. Als onderdeel van een uitgebreide behandeling kan het medicijn echter worden gebruikt.
Fysiotherapiebehandeling
Medische en chirurgische methoden zijn niet de enige manier om van azoospermie af te komen. Artsen gebruiken huidige, laser, magnetotherapie als een toevoeging aan de belangrijkste therapeutische methoden, waardoor een beter herstel van mannelijke vruchtbaarheid mogelijk is.
Ondertussen wordt de effectiviteit van fysieke procedures niet altijd opgemerkt: ze helpen als het nodig is om chronische urogenitale pathologieën te genezen, of om het herstel van het lichaam na de operatie te versnellen. Het belangrijkste effect van dergelijke procedures is het verhogen of verminderen van de spieren toon, het verwijden van vaten, het verbeteren van microcirculatie, het blokkeren van trage ontstekingsprocessen.
Fysiotherapie wordt niet voorgeschreven voor acute ontstekingsreacties, infectieuze processen, vermoedelijke kwaadaardige tumoren, evenals in perioden van koorts, met een ernstig verloop van systemische pathologieën.
- Vacuümmassage is de meest populaire procedure voor de behandeling van azoospermie en is een lokale negatieve druktechniek genaamd LOD-therapie. De procedure omvat het plaatsen van de penis in een speciale baro-kamer waaruit lucht langzaam wordt uitgepompt. Dientengevolge is het penisgebied actief vloeiend bloed, er komt een staat van erectie. Na het herstellen van de druk wordt de procedure herhaald. Een dergelijke specifieke massage wordt voorgeschreven als azoospermie bij een man wordt gecombineerd met erectiestoornissen. Wat geeft zo'n behandeling? Voorkomt bloedstasis, verbetert de microcirculatie, verrijkt de organen met zuurstof, wat een positief effect heeft op het werk van de prostaat en testikels. De methode is gecontra-indiceerd bij patiënten met een uitgesproken varicocele, inguinale hernia, evenals met een verhoogd risico op bloedstolsels.
- Lasertherapie omvat het gebruik van een laser met lage intensiteit die geen weefsel vernietigt: het rode stralingsbereik bereikt een diepte van twee millimeter en infrarood tot acht millimeter. De belangrijkste eigenschap van lasertherapie is immuunstimulatie, optimalisatie van metabole processen, het blokkeren van de ontstekingsreactie, activering van testosteronproductie, die direct de motorische activiteit van spermatozoa beïnvloedt.
- Magnetische therapie normaliseert het vasculaire netwerk, stabiliseert de hormoonproductie, heeft hypotensieve en antitumoreffecten.
- Elektrostimulatie omvat de toepassing van gepulseerde stromen die ervoor zorgen dat de spieren contracteren. Met behulp van elektroforese worden geneesmiddelen geleverd aan het vereiste gebied - met name enzym- en anti-edema-geneesmiddelen. Deze methode van medicijnafgifte aan de weefsels helpt de concentratie van het geneesmiddel in het noodzakelijke gebied van het lichaam te verhogen, om de ernst van de bijwerkingen te verminderen. Elektrostimulatie wordt niet voorgeschreven aan patiënten met tumorprocessen, complexe ontstekingsziekten, evenals in de aanwezigheid van huidlaesies in het gebied van de procedure.
Andere fysiotherapietechnieken voor azoospermie kunnen zijn:
- Ozon-therapie;
- Modderbehandeling;
- Transurethrale microgolftherapie.
De methoden kunnen alleen of in combinatie met elkaar worden gebruikt.
Kruidenbehandeling
Folk remedies voor azoospermie zijn meestal niet effectief. In sommige gevallen helpen medicinale planten in combinatie met levensstijl en dieetveranderingen echter om de kwaliteit van zaadvloeistof enigszins te verbeteren.
Als er problemen zijn met spermatogenese, wordt het aanbevolen om elke ochtend, middag en avond een infusie van meidoornfruit te brouwen en te drinken in plaats van thee. Daarnaast helpen kruidenhee van vlierbessen en hollyflower goed.
Knijp 100 ml sap om de kwaliteit van sperma-roosters te herstellen en meng het met twee tabletten mumie. Het medicijn wordt dagelijks geconsumeerd voor het ontbijt. Bovendien moet je gedurende de dag een infusie van de kruiden ergot drinken. Het verloop van een dergelijke behandeling gaat een maand door.
Kook 2 eetlepels van Adam's wortelplant met kokend water. Na het afkoelen wordt de remedie gefilterd en 1 el gebruikt. Dagelijks.
Bereid een kruidencollectie voor op basis van walnootbladeren, dennenscheuten, IJslandse mos en witte moerbei. Ingrediënten worden in gelijke hoeveelheden genomen. Dan 2 eetlepels. L. van het mengsel wordt gekookt water (450 ml) gegoten en dringt aan in een thermosmos gedurende een half uur. Zeef dan en neem drie keer per dag 150 ml in plaats van thee. Je kunt honing en citroensap toevoegen.
Een goed effect wordt gekenmerkt door een tinctuur van Lapchatka. Om het voor te bereiden, neemt u de wortelstok van de plant (100 g), giet 0,5 liter wodka, sta op twee weken. Dan wordt de tinctuur gefilterd en drie keer per dag een theelepel genomen tussen maaltijden, een kleine hoeveelheid water drinken.
Folk-genezers adviseren om azoospermia-seizoen eten te elimineren met gedroogde en verse basilicum, of een infusie van bladeren te drinken. Om een infusie van 20 g verse basilicumbladeren te bereiden die 250 ml kokend water zijn gegoten, sta je een half uur aan. De remedie is een half uur driemaal per dag gedronken voor het ontbijt, lunch en diner.
De producten van imkers - in het bijzonder Royal Jelly in combinatie met honing - doen ook goed werk. Zo'n mengsel wordt onmiddellijk na een maaltijd één lepel gegeten en houdt het in de mond totdat het volledig oplost. Het is niet nodig om water of andere vloeistoffen te drinken.
Chirurgische behandeling
In het geval van azoospermie, een pathologie waarin het ejaculaat spermatozoa mist, worden chirurgische methoden gebruikt om mannelijke geslachtscellen te verkrijgen. Deze methoden omvatten PESA, TESA en TESE.
De eerste twee methoden, PESA of TESA, worden meestal beoefend door specialisten. De TESE-techniek van bilaterale testiculaire biopsie met behulp van microchirurgische technologie wordt gebruikt om niet-obstructieve azoospermie te behandelen. [10] ]
- PESA is een naaldbiopsie uitgevoerd in verschillende gebieden van de testiculaire aanhangsels. PESA is een naaldbiopsie die wordt uitgevoerd in verschillende gebieden van de testiculaire aanhangsels en wordt als 100% effectief beschouwd in de aanwezigheid van VAS-experentobstructie, maar de procedure zelf kan de mate van VAS-experentieblokkering verder verergeren.
- De TESA-techniek omvat het uitvoeren van een naaldbiopsie in verschillende delen van de testikels. Het is een minimaal invasieve procedure die met succes het vereiste aantal spermatozoa verkrijgt. De methode heeft echter zijn nadelen: het is alleen effectief als er foci van spermatogenese zijn, maar zelfs bestaande foci kunnen niet altijd worden gedetecteerd vanwege het ontbreken van visuele controle over de weefselstructuur. Als de arts maximaal zes lekke banden op elke zaadbal uitvoert en er geen mannelijke kiemcellen worden gevonden, wordt een TESE-microchirurgische punctie aanbevolen.
- TESE is het ambitie van testiculair weefsel voor verdere sperma-extractie. Deze techniek wordt als het meest effectief beschouwd. Eerst wordt een biopsie uitgevoerd en worden spermatozoa gescheiden van het geëxtraheerde biomateriaal. Oefen gesloten punctie, waarvoor een speciaal pistool wordt gebruikt: deze procedure wordt gekenmerkt door frequente complicaties en relatief lage efficiëntie. De meest voorkomende is bilaterale microchirurgische multifocale testiculaire biopsie, die vaak wordt gebruikt bij patiënten met niet-obstructieve azoospermie.
Zwangerschap met azoospermie
Voordat voorspellingen worden gedaan over de mogelijkheid van bemesting van een vrouw met azoospermie bij een man, moet de arts de resultaten van de diagnose analyseren, het type bepalen en de oorzaak van de aandoening vinden. Pas daarna worden de optimale tactieken van latere maatregelen ontwikkeld om zwangerschap en de geboorte van een gezond kind voor het paar te bereiken.
Als een patiënt wordt gediagnosticeerd met obstructieve azoöspermie, is het mogelijk om de vruchtbaarheid te herstellen met behulp van een chirurg. Microchirurgische reconstructie wordt uitgevoerd om de VAS-aflagen te openen, waarvan de subtiliteiten afhankelijk zijn van de locatie en de omvang van het belemmerde gebied.
De zaak met secretoire azoöspermie is enigszins erger, omdat met zo'n diagnose de kansen op een succesvolle behandeling, hoewel dat er zijn, maar ze niet zo groot zijn. Desalniettemin kunnen sommige hormonale storingen worden geëlimineerd met conservatieve behandeling gericht op het stabiliseren van het endocriene systeem en het corrigeren van spermatogenese. Als de oorzaak van azoöspermie de uitbreiding van de scrotale vaten was, kan onvruchtbaarheid vaak worden genezen door een operatie.
Voor veel patiënten zijn de kansen op remedie nog steeds slank. In een dergelijke situatie, als de arts ziet dat er geen vooruitzicht is op lopende therapie, kan het gebruik van geassisteerde reproductieve methoden - met name IVF - worden aanbevolen. Deze technologie wordt al meer dan vier decennia met succes gebruikt door reproductologen en in de loop der jaren is de effectiviteit van de methode toegenomen.
IVF voor azoospermie
Tegenwoordig gebruiken specialisten met succes de techniek om mannelijke kiemcellen rechtstreeks uit de testikel te extraheren voor hun verdere gebruik in in vitro meststoffen (ICSI) -programma's. De techniek van sperma-extractie is biopsie. Deze procedure resulteert in een langverwachte zwangerschap in ongeveer 30-60% van de gevallen.
De effectiviteit van de biopsie kan variëren, afhankelijk van de ernst van de azoospermie. Om een duidelijkere geïndividualiseerde behandelingsprognose te bieden, wordt een grondig onderzoek van de patiënt uitgevoerd. De arts ontvangt voorlopige informatie over het type pathologie, waarmee hij de kansen op het succes van het bemesting beoordeelt.
Er zijn verschillende biopsietechnieken: de arts selecteert de meest geschikte die in een bepaalde situatie uiterst effectief zal zijn.
Het voorkomen
Het voorkomen van de ontwikkeling van azoöspermie en het voorkomen van reproductieve gezondheidsstoornissen bij mannen is in de eerste plaats over het leiden van een gezonde levensstijl. Artsen moeten hun patiënten motiveren en hen de noodzaak uitleggen om slechte gewoonten te vermijden.
Artsen bevelen aan:
- Weigeren om promiscue seksuele activiteiten te doen, heb geen onbeschermde geslachtsgemeenschap met een twijfelachtige partner;
- Weigeren alcoholische dranken te drinken, drugs of rook te gebruiken;
- Praktijk redelijke matige fysieke activiteit, vermijd zowel hypodynamie als overmatige fysieke activiteit;
- Bezoek periodiek een arts voor preventieve onderzoeken, behandel tijdig eventuele besmettelijke en inflammatoire processen in het lichaam;
- Niet te vergeten voldoende rust en slaap te krijgen;
- Vermijd conflicten en stressvolle situaties.
Bovendien is het belangrijk om te onthouden dat om de mannelijke vruchtbaarheid te behouden, het ongewenst is om zich van seks te onthouden en te vaak geslachtsgemeenschap te hebben. Het is optimaal om eenmaal per 3-4 dagen geslachtsgemeenschap te hebben.
Prognose
Het succes van de behandeling voor azoospermie hangt af van vele factoren. Dit zijn allereerst de leeftijd en de algemene gezondheidstoestand van de patiënt, zijn levensstijl. Als een chromosomaal defect wordt gedetecteerd, kan de specialist aandringen op extra genetische diagnose, wat nodig is om de mate van risico op embryo's te beoordelen. Bovendien vereist het recept van hormonale middelen een duidelijke controle van de behandeling: als u zich niet houdt aan het schema om dergelijke geneesmiddelen te gebruiken, kan dit de effectiviteit van de therapie aanzienlijk en negatief beïnvloeden.
De algehele prognose is als volgt: Patiënten met obstructieve azoöspermie hebben een betere kans om na de behandeling te bedenken, zowel natuurlijk als het gebruik van ondersteunde reproductieve technologieën. Secretoire azoospermie is moeilijker te behandelen, maar zelfs hier zijn er enkele kansen op succes van de therapie. Het belangrijkste is het vervullen van alle aanbevelingen en voorschriften van de arts, de exacte naleving van het behandelingschema. Alleen in dit geval is het mogelijk om het uiterlijk en de aanhoudende aanwezigheid van mannelijke geslachtscellen in het spermatvloeistof te bereiken, en verder - en een succesvolle conceptie.
Het meest hopeloze type aandoening wordt beschouwd als azoöspermie, ontwikkeld als gevolg van epidparotitis of bof. De ergste prognose wordt opgemerkt in de genetische of idiopathische vorm van pathologie.

