Medisch expert van het artikel
Nieuwe publicaties
Niet-tuberculose mycobacteriën
Last reviewed: 04.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
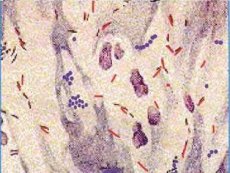
Niet-tuberculeuze mycobacteriën zijn onafhankelijke soorten die wijdverspreid in het milieu voorkomen als saprofyten en die in sommige gevallen ernstige ziekten kunnen veroorzaken - mycobacteriose. Ze worden ook wel milieumycobacteriën, verwekkers van mycobacteriose, opportunistische en atypische mycobacteriën genoemd. Een belangrijk verschil tussen niet-tuberculeuze mycobacteriën en Mycobacterium tuberculosis complex is dat ze vrijwel niet van mens op mens worden overgedragen.
Niet-tuberculeuze mycobacteriën worden op basis van een beperkt aantal kenmerken ingedeeld in 4 groepen: groeisnelheid, pigmentvorming, koloniemorfologie en biochemische eigenschappen.
1e groep - langzaam groeiende fotochromogene soorten (M. kansasii, enz.). Het belangrijkste kenmerk van vertegenwoordigers van deze groep is de aanwezigheid van pigment in het licht. Ze vormen kolonies van S- tot RS-vormen en bevatten caroteenkristallen, waardoor ze geel kleuren. De groeisnelheid varieert van 7 tot 20 dagen bij 25, 37 en 40 °C, catadase-positief.
M. kansasii zijn gele bacteriën die in water en aarde leven en meestal de longen aantasten. Deze bacteriën zijn te herkennen aan hun grote formaat en kruisvormige rangschikking. Een belangrijk symptoom van infecties veroorzaakt door M. kansasii is de ontwikkeling van een gedissemineerde ziekte. Huid- en weke delenlaesies, de ontwikkeling van peesschedeontsteking, osteomyelitis, lymfadenitis, pericarditis en infecties van het urogenitale stelsel zijn ook mogelijk.
2e groep - langzaam groeiende scotochromogene bacteriën (M. scrofulaceum, M. matmoense, M. gordonae, enz.). Micro-organismen vormen gele kolonies in het donker en oranje of roodachtige kolonies in het licht, meestal S-vormige kolonies, die groeien bij 37 °C. Dit is de meest voorkomende groep niet-tuberculeuze mycobacteriën. Ze worden geïsoleerd uit verontreinigde wateren en bodems en hebben een lage pathogeniciteit voor mens en dier.
M. scrofulaceum (van het Engelse scrofula - scrofula) is een van de belangrijkste veroorzakers van cervicale lymfadenitis bij kinderen jonger dan 5 jaar. Bij ernstige bijkomende ziekten kunnen ze schade veroorzaken aan de longen, botten en weke delen. Naast water en aarde zijn er ook microben geïsoleerd uit rauwe melk en andere zuivelproducten.
M. maimoense zijn microaerofielen die grijswitte, gladde, glanzende, ondoorzichtige, koepelvormige, ronde kolonies vormen.
Primaire isolaten groeien zeer langzaam bij 22-37 °C. Blootstelling aan licht veroorzaakt geen pigmentproductie. Indien nodig kan de blootstelling tot 12 weken worden voortgezet. Bij mensen veroorzaken ze chronische longziekte.
M. gordonae is de meest voorkomende erkende saprofyt, scotochromogeen in kraanwater, en veroorzaakt zeer zelden mycobacteriose. Naast water (bekend als M. aquae) worden ze vaak geïsoleerd uit de bodem, maagspoeling, bronchiale afscheidingen of ander materiaal van patiënten, maar in de meeste gevallen zijn ze niet pathogeen voor de mens. Tegelijkertijd zijn er meldingen van gevallen van meningitis, peritonitis en huidletsels veroorzaakt door dit type mycobacteriën.
Groep 3 - langzaam groeiende, niet-chromogene mycobacteriën (M. avium-complex, M. gaslri M. terrae-complex, enz.). Ze vormen kleurloze S- of SR- en R-kolonies, die lichtgeel en crèmekleurig kunnen zijn. Ze worden geïsoleerd uit zieke dieren, water en grond.
M. avium en M. inlracellulare worden gecombineerd tot één M. avium-complex, omdat hun interspeciesdifferentiatie bepaalde moeilijkheden oplevert. Micro-organismen groeien bij 25-45 °C, zijn pathogeen voor vogels, minder pathogeen voor runderen, varkens, schapen en honden, en zijn niet pathogeen voor cavia's. Meestal veroorzaken deze micro-organismen longletsels bij mensen. Letsels van de huid, het spierweefsel en het skelet, evenals verspreide vormen van ziekten, zijn beschreven. Ze behoren tot de verwekkers van opportunistische infecties die het verworven immunodeficiëntiesyndroom (aids) compliceren. M. avium subspecies paratuberculosis is de verwekker van de ziekte van Jones bij runderen en mogelijk de ziekte van Crohn (een chronische ontstekingsziekte van het maag-darmkanaal) bij mensen. De microbe is aanwezig in vlees, melk en ontlasting van geïnfecteerde koeien, en wordt ook aangetroffen in water en bodem. Standaard waterzuiveringsmethoden inactiveren deze microbe niet.
M. xenopi veroorzaakt longletsels bij mensen en verspreide vormen van ziekten die verband houden met aids. Ze worden geïsoleerd uit kikkers van het geslacht Xenopus. De bacteriën vormen kleine, gladde, glanzende, ongepigmenteerde kolonies die vervolgens felgeel kleuren. Thermofielen groeien niet bij 22 °C en groeien goed bij 37 en 45 °C. Bij bacterioscopie zien ze eruit als zeer dunne staafjes, die aan één kant taps toelopen en parallel aan elkaar liggen (zoals een schutting). Ze worden vaak geïsoleerd uit koud en warm kraanwater, inclusief drinkwater dat is opgeslagen in ziekenhuisreservoirs (nosocomiale uitbraken). In tegenstelling tot andere opportunistische mycobacteriën zijn ze gevoelig voor de meeste middelen tegen tuberculose.
M. ukerans is de verwekker van mycobacteriële cutane N (Buruli-ulcus). De ziekte groeit alleen bij 30-33 °C en koloniegroei wordt pas na 7 weken waargenomen. De ziekteverwekker komt ook vrij wanneer muizen geïnfecteerd raken in de pulpa van de pootzool. Deze ziekte komt veel voor in Australië en Afrika. De bron van infectie is de tropische omgeving en BCG-vaccinatie tegen deze mycobacteriose.
Groep 4 - snelgroeiende mycobacteriën (M. fortuitum-complex, M. phlei, M. xmegmatis, enz.). Hun groei wordt waargenomen in de vorm van R- of S-vormige kolonies gedurende 1-2 tot 7 dagen. Ze komen voor in water, grond en rioolwater en zijn representatief voor de normale microflora van het menselijk lichaam. Bacteriën uit deze groep worden zelden geïsoleerd uit pathologisch materiaal van patiënten, maar sommige ervan hebben klinische betekenis.
Het M. fortuitum-complex omvat M. fortuitum en M. chcionae, die uit twee ondersoorten bestaan. Ze veroorzaken gedissemineerde processen, huid- en postoperatieve infecties en longziekten. De microben van dit complex zijn zeer resistent tegen tuberculosemedicijnen.
M. smegmatis is een vertegenwoordiger van de normale microflora, geïsoleerd uit smegma bij mannen. De bacterie groeit goed bij 45 °C. Als verwekker van menselijke ziekten staat hij op de tweede plaats onder de snelgroeiende mycobacteriën, na het M. fortuitum-complex. Hij tast de huid en weke delen aan. Tuberculoseverwekkers moeten van M. smegmatis worden onderscheiden bij urineonderzoek.
Meestal worden mycobacteriose veroorzaakt door vertegenwoordigers van groep 3 en 1.
Epidemiologie van mycobacteriose
De verwekkers van mycobacteriose komen wijdverbreid voor in de natuur. Ze zijn te vinden in aarde, stof, veen, modder, rivierwater, vijvers en zwembaden. Ze worden aangetroffen in teken en vissen, veroorzaken ziekten bij vogels, wilde dieren en huisdieren en zijn vertegenwoordigers van de normale microflora van de slijmvliezen van de bovenste luchtwegen en het urogenitale stelsel bij mensen. Infectie met niet-tuberculeuze mycobacteriën vindt plaats vanuit de omgeving via overdracht via de lucht, contact met huidbeschadigingen, en via voedsel en water. Overdracht van micro-organismen van persoon op persoon komt zelden voor. Het zijn opportunistische bacteriën, dus een afname van de weerstand van het macro-organisme en zijn genetische aanleg zijn van groot belang voor de ontwikkeling van de ziekte. Granulomen vormen zich in de aangetaste gebieden. In ernstige gevallen is de fagocytose onvolledig, is er sprake van uitgesproken bacteriëmie en worden in de organen macrofagen aangetroffen die gevuld zijn met niet-tuberculeuze mycobacteriën en lijken op lepracellen.
Symptomen van mycobacteriose
De symptomen van mycobacteriose zijn divers. Het ademhalingsstelsel wordt het vaakst aangetast. De symptomen van longpathologie zijn vergelijkbaar met die van tuberculose. Er zijn echter vaak gevallen van extrapulmonale lokalisatie van het proces, waarbij de huid en het onderhuidse weefsel, wondoppervlakken, lymfeklieren, urogenitale organen, botten en gewrichten, evenals de hersenvliezen betrokken zijn. Orgaanlaesies kunnen zowel acuut als latent beginnen, maar verlopen bijna altijd ernstig.
Het is ook mogelijk dat er een gemengde infectie ontstaat. In sommige gevallen kunnen ze de oorzaak zijn van het ontstaan van een secundaire endogene infectie.
Microbiologische diagnostiek van mycobacteriose
De belangrijkste methode voor het diagnosticeren van mycobacteriose is bacteriologisch. Het materiaal voor het onderzoek wordt verzameld op basis van de pathogenese en klinische manifestaties van de ziekte. Eerst wordt bepaald of de geïsoleerde reincultuur behoort tot de verwekkers van tuberculose of tot niet-tuberculeuze mycobacteriën. Vervolgens wordt een reeks studies gebruikt om het type mycobacteriën, de mate van virulentie en de Runyon-groep vast te stellen. De primaire identificatie is gebaseerd op kenmerken zoals groeisnelheid, vermogen om pigment te vormen, koloniemorfologie en vermogen om bij verschillende temperaturen te groeien. Om deze kenmerken te identificeren, zijn geen extra apparatuur of reagentia nodig, waardoor ze kunnen worden gebruikt in basislaboratoria van tuberculoseklinieken. De definitieve identificatie (referentie-identificatie) met behulp van complexe biochemische studies wordt uitgevoerd in gespecialiseerde laboratoria van wetenschappelijke instellingen. In de meeste gevallen wordt de voorkeur gegeven aan identificatie op basis van biochemische feiten, zoals moderne moleculair genetische methoden die arbeidsintensief zijn, veel voorbereidende fasen hebben, speciale apparatuur vereisen en duur zijn. Het bepalen van de gevoeligheid voor antibiotica is van groot belang voor de behandeling. De gelijktijdige aanwezigheid van klinische, radiologische en laboratoriumgegevens en de isolatie van een zuivere kweek van niet-tuberculeuze mycobacteriën, en het uitvoeren van meerdere dynamische studies, zijn van doorslaggevend belang voor de diagnose van mycobacteriose.
Van hulpbelang bij de diagnostiek zijn de bepaling van antithesen met behulp van RNGA, RP, immuno-elektroforese, RNIF en ELISA, alsmede het uitvoeren van huidallergietesten met sensitines.
Behandeling en specifieke preventie van mycobacteriose
Alle soorten niet-tuberculeuze mycobacteriën, met uitzondering van M. xenopi, zijn resistent tegen isoniazide, streptomycine en thiosemicarbazonen. Behandeling van mycobacteriose met antituberculose- en antibacteriële middelen dient langdurig (12-13 maanden) en gecombineerd te zijn. Het is meestal niet effectief bij MAC-infecties en ziekten veroorzaakt door snelgroeiende mycobacteriën. In sommige gevallen wordt chirurgische behandeling toegepast. Er zijn geen geneesmiddelen ontwikkeld voor specifieke preventie van mycobacteriose.


 [
[