Medisch expert van het artikel
Nieuwe publicaties
Diagnose van de stadia van prostaatkanker
Laatst beoordeeld: 04.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Klinisch wordt onderscheid gemaakt tussen gelokaliseerde (T 1-2, N 0, M 0 ), lokaal gevorderde (T 3-4, N 0-1, M 0 ) en gegeneraliseerde kanker (T 1-4, N 0-1, M 1 ).
Patiënten met klinisch gelokaliseerde en lokaal gevorderde stadia worden geclassificeerd volgens de mate van risico (D'Amico A V. et al., 2003):
- laag: stadium T 1a-c; PSA-niveau minder dan 10 µg/ml: Gleason-classificatie - 2-5; in biopsie - unilaterale laesie minder dan 50%:
- matig: stadium T 2a; PSA-niveau minder dan 10 ng/ml; Gleason-score - 3 + 4 = 7; in biopsie - bilaterale laesie minder dan 50%;
- hoog stadium T 2b, T 3a-b; PSA-niveau - 10-20 ng/ml; Gleason-classificatie - meer dan 4 + 3 - 7; in biopsie - schade meer dan 50%, perineurale invasie;
- Zeer hoog: stadium T 4; PSA-niveau boven 20 ng/ml; Gleason-score boven 8; biopsie toont lymfovasculaire invasie.
Nadat de diagnose is gesteld en de omvang van het proces is vastgesteld (gelokaliseerd, lokaal gevorderd of gegeneraliseerd), staan de arts en de patiënt voor de keuze van een behandelmethode. In de moderne samenleving wordt veel belang gehecht aan de kwaliteit van leven van patiënten na aanvang van de behandeling. De kwaliteit van leven zonder behandeling hangt af van het beloop van de onderliggende ziekte en de progressie van het oncologische proces. Veranderingen in de kwaliteit van leven treden vooral op na aanvang van de behandeling en het gebruik van een van de therapeutische of chirurgische methoden. Door het stadium van het proces duidelijk vast te stellen, kan niet alleen de optimale behandelmethode worden gekozen, maar ook het verdere verloop van de ziekte worden voorspeld.
Bepaling van de PSA-waarde in combinatie met het klinische beeld van prostaatkanker en de gradatie van de tumor volgens de Gleason-schaal verhoogt de informatie-inhoud van elk van de genoemde indicatoren aanzienlijk bij het vaststellen van het pathologische stadium van kanker. AV Partin et al. (1997) hebben prognosetabellen voorgesteld die het mogelijk maken de verdere verspreiding van de tumor, de keuze van de behandelmethode, de mate van radicaliteit en de prognose van de effectiviteit van de behandeling te voorspellen.
Om de uitzaaiing van de tumor te beoordelen, zijn DRE, TRUS, bepaling van de PSA-waarde en botscintigrafie de meest gebruikte methoden. Indien nodig worden computertomografie (CT) of magnetische resonantiebeeldvorming (MRI) en een röntgenfoto van de borstkas voorgeschreven.
Elke beeldvormende methode is ontworpen om het stadium te bepalen en de effectiviteit van de behandeling te beoordelen. Na het verifiëren van de diagnose moet de uroloog de omvang van de primaire tumor, de grenzen ervan en het invasieve of metastatische potentieel van de tumor vaststellen. Al deze indicatoren zijn van groot belang voor de prognose van de ziekte en de keuze van de behandelmethode.
Primaire tumor (T)
Allereerst is het noodzakelijk om te bepalen of de tumor beperkt is tot de prostaatklier (T 1-2 ) of zich uitstrekt tot buiten het kapsel (T 3-4 ). Digitaal onderzoek laat vaak niet toe om de verspreiding van de tumor te beoordelen. Volgens sommige gegevens komen de resultaten van DRE bij minder dan 50% van de patiënten overeen met die van histologisch onderzoek. Een uitgebreider onderzoek is echter alleen geïndiceerd bij het bepalen van een radicale behandeling.
De PSA-waarde kan de omvang van de tumor weerspiegelen, maar biedt geen nauwkeurige bepaling van het morfologische stadium. De combinatie van de PSA-waarde, de Gleason-index en palpatiegegevens maakt een betere voorspelling van het morfologische stadium mogelijk dan elk van deze parameters afzonderlijk. De waarde van vrij PSA is controversieel: in één onderzoek hielp het bepalen van het vrije PSA-gehalte om het stadium in gelokaliseerde tumoren te verduidelijken, maar andere onderzoeken konden dit niet bevestigen. Alleen diepgaande studies kunnen dit probleem oplossen.
Transrectale echografie wordt het vaakst gebruikt om de toestand van de prostaatklier te onderzoeken. Deze methode kan slechts 60% van de tumoren detecteren en toont niet altijd kapselinvasie. Bijna 60% van de patiënten met stadium T3 . Echografie toont een minder vaak voorkomend proces. Echografische tekenen van kapselinvasie zijn uitstulping, oneffenheid en ruptuur van de kliercontour. Invasie van tumorcellen in de zaadblaasjes is een slecht prognostisch teken, maar informatie hierover is uiterst belangrijk voor het kiezen van een behandelmethode. Bij het uitvoeren van TRUS moet aandacht worden besteed aan de echostructuur van de blaasjes (hyperechogeniciteit), hun asymmetrie, vervorming en expansie. Schade aan de zaadblaasjes wordt ook aangegeven door verlies van rondheid en verdichting aan de basis van de klier. Deze tekenen zijn vrij subjectief, dus het is niet juist om volledig op echografische gegevens te vertrouwen. Invasie van de zaadblaasjes wijst op een hoog risico op lokale recidieven en metastasen, en een biopsie ervan is geïndiceerd ter opheldering (vóór de operatie). Het onderzoek dient niet met deze procedure te worden gestart, maar als het risico op invasie hoog is en de keuze van de behandeling afhangt van de biopsie-uitslag, is de implementatie ervan gerechtvaardigd. Een negatief resultaat sluit microscopische invasie niet uit. In de regel wordt een biopsie van de zaadblaasjes uitgevoerd bij klinisch stadium T2b en hoger en het PSA-gehalte meer dan 10 ng/ml bedraagt. Het resultaat wordt als positief beschouwd als ten minste één biopsie van de prostaatklierbasis tumorcellen bevat. Niet alleen aanvullend onderzoek, maar ook een grondige analyse van de resultaten van de primaire biopsie maken het mogelijk de nauwkeurigheid van de klinische bepaling van het stadium te vergroten (het aantal en de omvang van tumorhaarden, kapselinvasie spelen een rol). De mate van differentiatie is ook belangrijk: bij een Gleason-index van minder dan 6 is de tumor in 70% van de gevallen gelokaliseerd.
De bloedstroom in de prostaatklier bij kanker is hoger dan in een normale prostaatklier of bij hyperplasie. Na castratie is de intensiteit van de bloedstroom in de prostaatklier verminderd. De ontwikkeling van echodopplerografie voor de diagnose en monitoring van prostaatkanker is veelbelovend, maar er zijn momenteel geen betrouwbare gegevens over het gebruik van echodopplerografie bij het bepalen van het stadium van het lokale proces. Het is mogelijk om deze methode te gebruiken om extra materiaal te verkrijgen tijdens een gerichte biopsie uit foci van pathologische vascularisatie.
De resultaten van prostaatkankervisualisatie zijn direct afhankelijk van de technische uitrusting van de kliniek en de ervaring van de specialist. Daarom spelen alle moderne visualisatiemethoden geen bepalende, maar een verhelderende rol, en is de keuze van de behandelmethode gebaseerd op een combinatie van klinische onderzoeksgegevens en instrumentele studies.
MRI biedt de beste mogelijkheden voor visualisatie van de structuur van de prostaatklier. De moderne standaard voor onderzoek van de bekkenorganen met behulp van de MRI-methode is het gebruik van een endorectale sensor, waarmee een beeld met de hoogst mogelijke ruimtelijke resolutie van 0,5-1 mm kan worden verkregen. Door lucht in de endorectale sensor te persen, worden het prostaatkapsel, de rectoprostatische hoeken en de rectoprostatische fascia van Denonvilliers duidelijk zichtbaar. Het gebruik van een endorectale sensor bij MRI beperkt de visualisatie van regionale lymfeklieren (tot aan de bifurcatie van de aorta abdominalis) niet. Prostaatkanker wordt gekenmerkt door een lage signaalintensiteit op T-gewogen beelden tegen de achtergrond van een hoog-intensief signaal van een onveranderde perifere zone van de klier. Onregelmatige vorm, diffuse verspreiding met massa-effect, vage en ongelijkmatige contouren zijn morfologische kenmerken van foci met lage signaalintensiteit in de perifere zone van de prostaatklier, wat wijst op een neoplastische aard van de laesie. Bij dynamische contrastmeting accumuleren kankerhaarden snel het contrastmiddel in de arteriële fase en verwijderen het snel, wat de mate van angiogenese en daarmee de mate van maligniteit van de tumor weerspiegelt. Een lage signaalintensiteit is ook kenmerkend voor haarden van post-biopsiebloedingen, prostatitis, goedaardige stromahyperplasie van de neutrale zone van de klier, fibreuze en littekenvorming, fibromusculaire hyperplasie en de gevolgen van hormonale of radiotherapie. MRI zonder dynamische contrastmeting maakt geen betrouwbare differentiatie van de meeste van de genoemde veranderingen en aandoeningen mogelijk.
Zoals hierboven vermeld, is een van de belangrijkste taken van elke beeldvormingsmethode voor prostaatkanker het bepalen van het volume van de klierlaesie en de verspreiding van de tumor buiten het kapsel. Het bepalen van het tumorvolume is belangrijk voor de prognose. Een tumorvolume van minder dan 4 cm³ wijst op uitzaaiingen op afstand, en 12 cm³ wijst op een extreem hoge kans op uitzaaiingen. Volgens onderzoek varieert de nauwkeurigheid van MRI bij het detecteren van foci van neoplastische laesies in de prostaatklier van 50 tot 90%. De gevoeligheid van MRI bij het bepalen van de lokalisatie van prostaatkanker is ongeveer 70-80%, terwijl microscopische foci van kanker (foci) niet met MRI kunnen worden gedetecteerd.
Het belangrijkste voordeel van endorectale MRI is de mogelijkheid om neoplastische laesies te lokaliseren in gebieden die ontoegankelijk zijn voor andere diagnostische methoden en om de aard en richting van de tumorgroei te verduidelijken. MRI maakt bijvoorbeeld het detecteren van neoplastische laesies mogelijk in de voorste delen van de perifere zone van de prostaat, die ontoegankelijk zijn met transrectale biopsie. Over het algemeen vormt MRI een aanzienlijke aanvulling op de gegevens van DRE en TRUS over tumorlokalisatie.
Endorectale MRI maakt visualisatie van het kapsel van de klier, de vaat-zenuwbundels, de zaadblaasjes, de kliertop, de periprostatische veneuze plexus en bepaling van de lokale prevalentie van de kliertumor mogelijk. Het is belangrijk te benadrukken dat kapselpenetratie als een microscopisch teken wordt beschouwd en dat zelfs moderne MRI-apparatuur (endorectale coils) dergelijke informatie niet kan verschaffen. Het is alleen mogelijk om gegevens te verkrijgen over groei voorbij het kapsel van de klier.
Diagnostische criteria voor extracapsulaire extensie met behulp van MRI:
- de aanwezigheid van een extracapsulaire tumor;
- ongelijkmatige contour van de klier (vervorming, hoekigheid);
- asymmetrie van neurovasculaire bundels;
- obliteratie van de rectoprostatische hoeken;
- breed contact van de tumor met het kapsel.
De hoogste specificiteit (tot 95-98%) en nauwkeurigheid van MRI-resultaten worden bereikt bij het onderzoeken van patiënten met een gemiddeld of hoog risico op extracapsulaire invasie. Er wordt aangenomen dat extracapsulaire invasie (volgens MRI-gegevens) wijst op de ongeschiktheid van chirurgische behandeling en een ongunstige prognose voor de ziekte. Hormonale of radiotherapie heeft geen invloed op de nauwkeurigheid van het detecteren van extracapsulaire verspreiding van prostaattumoren. De grootste moeilijkheid bij het detecteren van kankerhaarden en extracapsulaire verspreiding van tumoren is de grote variabiliteit in de interpretatie van tomogrammen door verschillende specialisten. De primaire taak van een specialist in radiodiagnostiek is het bereiken van een hoge diagnostische specificiteit (zelfs ten koste van de sensitiviteit) om operabele patiënten niet de kans op radicale behandeling te ontnemen.
De vergelijkbare dichtheid van kankerachtig, hyperplastisch en normaal prostaatweefsel op CT maakt deze methode weinig bruikbaar voor het beoordelen van de lokale verspreiding van de tumor. Invasie in de zaadblaasjes is belangrijker dan invasie in de kapsels, maar zelfs in dit geval levert CT alleen informatie op bij gevorderde gevallen. Deze methode wordt echter actief gebruikt om het getroffen gebied te markeren vóór radiotherapie.
De trage ontwikkeling van radiodiagnostiek in ons land heeft geleid tot late diagnose van prostaatkanker en daarmee tot een onvoldoende prevalentie van radicale behandelmethoden voor prostaatkanker (bijvoorbeeld prostatectomie), een beperkte beschikbaarheid van moderne tomografen en het ontbreken van geschikte opleidingen voor specialisten in radiodiagnostiek en urologen. Ondanks de wijdverspreide aanwezigheid van CT en MRI, is de uitrusting van de spreekkamers en de opleiding van specialisten in radiodiagnostiek onvoldoende om de verkregen informatie doorslaggevend te maken bij de keuze van een behandelmethode voor patiënten met prostaatkanker.
Regionale lymfeklieren (N)
Regionale lymfeklieren dienen alleen te worden beoordeeld wanneer dit direct van invloed is op de behandelstrategie (meestal bij het plannen van een radicale behandeling). Hoge PSA-waarden, T2c -T3a- tumoren, slechte differentiatie en perineurale invasie gaan gepaard met een hoog risico op lymfekliermetastasen. Beoordeling van de lymfeklierstatus op basis van PSA-waarden wordt als onvoldoende beschouwd.
Alleen lymfeklierdissectie (open of laparoscopisch) levert de benodigde informatie op. Recente studies naar uitgebreide lymfeklierdissectie hebben aangetoond dat prostaatkanker niet altijd de obturatorlymfeklieren aantast. Bij asymptomatische tumoren en PSA-waarden lager dan 20 kg/ml bevestigt CT slechts in 1% van de gevallen vergrote lymfeklieren. Het gebruik van MRI of CT is gerechtvaardigd bij een hoog risico op metastasering, aangezien de specificiteit van deze methoden 93-96% bedraagt. Zelfs een positief resultaat kan echter vals zijn, en alleen een punctie van een verdachte lymfeklier volstaat om lymfeklierdissectie te weigeren. Retrospectieve analyse toont aan dat de grootte van de lymfeklier niet altijd de aanwezigheid van metastasen aangeeft; asymmetrie van de aangetaste lymfeklieren wordt als een meer informatief teken beschouwd. Momenteel wordt bij slechts 2-3% van de patiënten die een radicale prostatectomie hebben ondergaan vanwege gelokaliseerde prostaatkanker, op basis van postoperatief histologisch onderzoek de diagnose gesteld van uitzaaiingen naar de lymfeklieren.
Positronemissietomografie (PET) en scintigrafie met gelabelde antilichamen worden aanbevolen als methoden voor het detecteren van metastasen in lymfeklieren, maar het gebruik ervan is nog steeds beperkt vanwege de onvoldoende gevoeligheid.
De nomogrammen van Partin (2001) kunnen worden gebruikt om het risico op regionale lymfeklierbetrokkenheid te beoordelen. Nomogrammen zijn wiskundige algoritmen die worden gebruikt voor een specifieke patiënt of een groep patiënten. Deze tabellen maken het mogelijk om de kans op lokale tumoruitzaaiing (naar het kapsel, zaadblaasjes) en lymfeklierbetrokkenheid te bepalen op basis van het klinische stadium, PSA-niveau en Gleason-index. Ze maken het met name mogelijk om een groep patiënten te identificeren met een lage (minder dan 10%) kans op lymfekliermetastasen (met een PSA-niveau boven 20 ng/maand, stadium T 1-2a en Gleason-index 2-6); in deze groep kan de conditie van de lymfeklieren mogelijk niet worden gespecificeerd vóór radicale behandeling. Het risico op lymfekliermetastasen kan ook worden ingeschat door tumorgebieden met uitgesproken anaplasie (4-5 punten) op te sporen: als dergelijke gebieden in vier of meer biopten worden gevonden of in ten minste één biopt overheersen, bedraagt het risico 20-45%. Bij andere patiënten bedraagt het risico niet meer dan 2,5%. Aanvullend onderzoek is in deze gevallen niet nodig.
Uitzaaiingen op afstand (M)
Bij 85% van de patiënten die aan prostaatkanker overlijden, worden laesies van het axiale skelet vastgesteld. Botmetastasen ontstaan doordat kankercellen met de bloedbaan het beenmerg binnendringen, wat leidt tot tumorgroei en lysis van botstructuren. De prevalentie van botmetastasen beïnvloedt de prognose en vroege detectie waarschuwt de arts voor mogelijke complicaties. In 70% van de gevallen gaat de metastasering gepaard met een verhoogde activiteit van het iso-enzym alkalische fosfatase (ALP) in het bot. Bepaling van de activiteit van ALP en de PSA-waarde stelt ons in de overgrote meerderheid van de gevallen in staat om botmetastasen te detecteren. Volgens multivariate analyse worden deze indicatoren alleen beïnvloed door het aantal botmetastasen. Het is belangrijk dat de activiteit van het iso-enzym ALP de mate van botschade nauwkeuriger weergeeft dan de PSA-waarde.
Scintigrafie wordt beschouwd als de meest gevoelige methode voor het detecteren van botmetastasen (het is beter dan radiografie en het bepalen van de activiteit van alkalische en zure fosfatase). Technetiumdifosfonaten zijn beter bruikbaar als radiofarmaceutisch middel, omdat hun accumulatie in botten veel actiever is dan in weke delen. Er is een correlatie aangetoond tussen een semi-kwantitatieve beoordeling van botschade en overleving. Detectie van metastasen op afstand is mogelijk in elk orgaan. Ze komen het vaakst voor in niet-regionale lymfeklieren, longen, lever, hersenen en huid. Bij overeenkomstige klachten en symptomen worden thoraxfoto, echografie, CT en MRI gebruikt om ze op te sporen. De tactieken voor verdenking op botmetastasen worden weergegeven in het diagram.
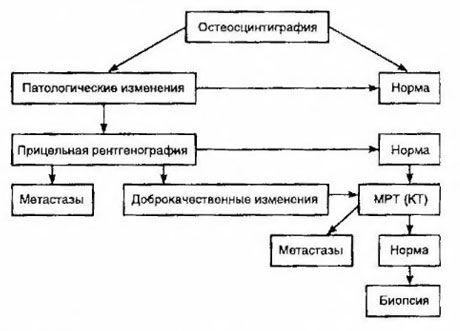
De meest betrouwbare laboratoriumindicator die helpt bij het bepalen van de mate van metastasering is de PSA-waarde. Het is aangetoond dat een stijging van meer dan 100 ng/ml de enige parameter is die betrouwbaar wijst op metastasen op afstand. Het bepalen van de PSA-waarde vermindert het aantal patiënten dat botscintigrafie nodig heeft. De kans op het detecteren van botmetastasen met een daling van de PSA-waarde is zeer laag. Bij afwezigheid van klachten en een initiële PSA-waarde van minder dan 20 ng/ml kan scintigrafie worden vermeden bij de detectie van sterk en matig gedifferentieerde tumoren. Tegelijkertijd is scintigrafie geïndiceerd bij slecht gedifferentieerde tumoren en kapselinvasie (ongeacht de PSA-waarde).


 [
[