Medisch expert van het artikel
Nieuwe publicaties
Norovirus: genotypen, tests, verloop en complicaties
Laatst bijgewerkt: 03.07.2025

We hanteren strikte richtlijnen voor bronnen en linken alleen naar gerenommeerde medische websites, academische onderzoeksinstellingen en, waar mogelijk, medisch peer-reviewed onderzoek. De nummers tussen haakjes ([1], [2], enz.) zijn klikbare links naar deze onderzoeken.
Als u van mening bent dat onze content onjuist, verouderd of anderszins twijfelachtig is, selecteer deze dan en druk op Ctrl + Enter.
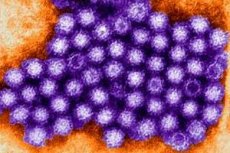
Norovirus is de belangrijkste oorzaak van acute gastro-enteritis bij mensen van alle leeftijden. Het is een zeer besmettelijke ziekteverwekker die wordt overgedragen via contact met een besmet persoon, voedsel, water en besmette oppervlakken. Internationale volksgezondheidsinstanties schatten dat norovirus verantwoordelijk is voor ongeveer 18% van alle gevallen van diarree en braken wereldwijd, waarbij het jaarlijkse aantal gevallen wordt geschat op honderden miljoenen. [1]
De druk op de gezondheidszorg en de economie is hoog. Volgens schattingen van gespecialiseerde centra alleen al worden jaarlijks honderden miljoenen gevallen van gastro-enteritis en tienduizenden sterfgevallen onder jonge kinderen geregistreerd, voornamelijk in landen met weinig middelen. Dit maakt het norovirus tot een prioriteitsdoel voor de preventie en bestrijding van uitbraken. [2]
Besmetting is mogelijk met kleine doses van het virus, maar de verspreiding ervan in het milieu kan enorme hoeveelheden bereiken. Dit verklaart de gemakkelijke verspreiding in gesloten gemeenschappen: verpleeghuizen, ziekenhuizen, kinderopvang, schepen en restaurants. [3]
In gematigde klimaten komen uitbraken het vaakst voor tijdens het koude seizoen, maar infectie is het hele jaar door mogelijk. De immuniteit na de ziekte is onvolledig en van korte duur, wat leidt tot terugkerende episodes, vooral wanneer er nieuwe varianten van de ziekteverwekker opduiken. [4]
Bij de meeste patiënten is de therapie ondersteunend en gericht op rehydratatie, correctie van elektrolytenonevenwichtigheden en veilige symptoomverlichting. Specifieke antivirale middelen zijn nog niet goedgekeurd voor routinematig gebruik; vaccinatie is in ontwikkeling en ondergaat een belangrijke herevaluatie na de mislukte proef met een belangrijke kandidaat. [5]
Tabel: Belangrijkste feiten over norovirus
| Parameter | Intelligentie |
|---|---|
| De belangrijkste klinische vorm | Acute gastro-enteritis met diarree en braken |
| Infectieuze dosis | Vanaf 18 deeltjes en hoger |
| Piekseizoensinvloeden | Meestal in de winter, maar er zijn het hele jaar door gevallen |
| Belangrijkste transmissieroutes | Contact - huishouden, voedsel, water, aerosol-druppelafzetting tijdens braken |
| Basistherapie | Orale rehydratatie, indien nodig intraveneuze oplossingen |
Epidemiologie
De wereldwijde ziektelast blijft aanhoudend hoog. Naar schatting doen zich jaarlijks 685 miljoen gevallen voor, waarvan ongeveer 200 miljoen bij kinderen jonger dan 5 jaar; in deze groep worden tienduizenden sterfgevallen gemeld. In totaal is norovirus verantwoordelijk voor ongeveer 18% van de gevallen van acute gastro-enteritis. [6]
Na de dalingen als gevolg van de pandemiegerelateerde beperkingen, rapporteerden veel landen in Europa in 2023-2024 een toename van het aantal gevallen en uitbraakniveaus boven de seizoenen van vóór de pandemie. Er werd een toegenomen circulatie van genotypes waargenomen, waaronder uitbraken van GII.17 in verschillende landen. [7]
De overdracht is het meest intens in gesloten omgevingen, waar nauw contact en oppervlaktebesmetting de omstandigheden voor herinfectie creëren. In dergelijke omgevingen draagt het norovirus aanzienlijk bij aan de 'winterlast' van de gezondheidszorg. [8]
De lage infectieuze dosis en de persistentie van het virus in de omgeving leiden tot voedselgerelateerde uitbraken en contacttransmissieketens. Zelfs geïsoleerde braakaanvallen kunnen ervoor zorgen dat aerosolen zich op omringende oppervlakken nestelen, wat de verspreiding van het virus in gemeenschappen bevordert. [9]
Langdurige virale uitscheiding na klinisch herstel houdt occulte transmissie in stand. Bij immuungecompromitteerde patiënten is chronische virale uitscheiding met maandenlange uitscheiding en intra-host evolutie van varianten mogelijk. [10]
Tabel. Epidemiologische richtlijnen
| Indicator | Typische waarde |
|---|---|
| Aandeel van alle acute gastro-enteritis | Ongeveer 18% |
| Wereldwijde gevallen per jaar | Ongeveer 685 miljoen |
| Kwetsbare groepen | Kinderen jonger dan 5 jaar, ouderen, immuungecompromitteerd |
| Seizoensinvloeden | Meestal koude maanden |
| Recente trends in Europa | De activiteit zal in 2023-2024 toenemen, waarbij het GII-aandeel groeit.17 |
Structuur van de ziekteverwekker
Norovirus behoort tot de familie Caliciviridae en is een ongeënvelopt deeltje met icosahedrale symmetrie en een diameter van ongeveer 35-50 nanometer. De capside bestaat uit het VP1-eiwit, georganiseerd in 90 dimeren, en een kleine hoeveelheid VP2-eiwit. Deze architectuur vormt het "enveloppe"-domein en het uitstekende P-domein, dat cruciaal is voor de receptorherkenning op menselijke cellen. [11]
Het virale genoom is een enkelstrengs, positief-sense ribonucleïnezuur van ongeveer 7,5 kilonucleotiden lang met een covalent gebonden VPg-eiwit aan het uiteinde van vijf basen. Het genoom codeert voor drie open leeskaders: een groot polyproteïne van niet-structurele eiwitten en twee structurele eiwitten van de capside. [12]
Kritieke regio's van het P2-subdomein van VP1 interacteren met zogenaamde bloedhistogroepantigenen op het oppervlak van menselijke cellen. De diversiteit van deze koolhydraatstructuren bij mensen bepaalt gedeeltelijk de vatbaarheid voor verschillende genotypes en vergroot de wendbaarheid van het virus wanneer nieuwe varianten ontstaan. [13]
Niet-structurele eiwitten die uit het polyproteïne worden gevormd omvatten protease en RNA-afhankelijke RNA-polymerase, evenals eiwitten die intracellulaire membranen herstructureren en 'replicatiefabrieken' creëren. Het NS4-eiwit is bijvoorbeeld betrokken bij het organiseren van membraanstructuren die nodig zijn voor de synthese van genomisch en subgenomisch ribonucleïnezuur. [14]
De capsidestructuur en het vermogen om virusachtige deeltjes te assembleren op basis van VP1 worden actief gebruikt voor de ontwikkeling van vaccins en de evaluatie van neutraliserende antilichamen. Deze deeltjes bootsen morfologisch en antigeen inheemse virionen na en maken een veilige studie van immuunreacties mogelijk. [15]
Tabel. Genoom en eiwitten van norovirus
| Onderdeel | Functie |
|---|---|
| Genomisch ribonucleïnezuur | Matrix voor de synthese van polyproteïne- en capside-eiwitten |
| VPg | Primer en regulator van genomische ribonucleïnezuurtranslatie |
| VP1 | Het belangrijkste capside-eiwit vormt de S- en P-domeinen |
| VP2 | Klein capside-eiwit, stabilisatie van genomische verpakking |
| Protease en polymerase | Polyproteïnerijping en genoomreplicatie |
Levenscyclus
De infectie begint met hechting aan koolhydraat-"doelen" op het oppervlak van enterocyten in de dunne darm. Interactie van het VP1 P-domein met bloedhistogroepantigenen zorgt voor herkenning en binnendringing in de cel. Sommige genotypes vertonen verschillende bindingsspectra, wat van invloed is op tropisme en epidemisch potentieel. [16]
Na penetratie wordt het genomische ribonucleïnezuur onmiddellijk vertaald, waardoor een polyproteïne ontstaat. Het virale protease vormt op vooraf bepaalde "snijpunten" een reeks niet-structurele eiwitten die de endomembraancompartimenten herstructureren. RNA-afhankelijke RNA-polymerase opereert op deze "platformen". [17]
Replicatie omvat de synthese van een negatieve kopie van volledige lengte, vervolgens nieuwe positieve genomen en subgenomisch ribonucleïnezuur voor de synthese van VP1 en VP2. De assemblage van de capside en de verpakking van het genoom leiden tot de rijping van virionen, die vrijkomen en naburige cellen infecteren.[18]
Moderne modellen gebaseerd op menselijke darmenteroïden hebben de reproduceerbare kweek van bepaalde norovirusgenotypen mogelijk gemaakt. Dit was een doorbraak in het bestuderen van de levenscyclus en het screenen van antivirale kandidaten, hoewel de gevoeligheid en reproduceerbaarheid afhankelijk zijn van de stam en de donorkenmerken. [19]
Nieuwe gegevens over de structuur van polymerase, protease en belangrijke niet-structurele eiwitten verduidelijken replicatieknelpunten die mogelijk geschikt zijn voor medicijntargeting. Dit gebied is actief in ontwikkeling en verbindt fundamentele ontdekkingen met de zoektocht naar therapeutische doelen. [20]
Tabel. Levenscyclusfasen
| Fase | Korte beschrijving | Potentiële therapeutische doelen |
|---|---|---|
| Bijlage | Binding aan bloedhistogroepantigenen | Blokkering van de capside-interactie met receptoren |
| Penetratie en demontage | Aflevering van het genoom in het cytoplasma | Toegangsremmers |
| Polyproteïne vertaling | Vorming van niet-structurele eiwitten | Proteaseremmers |
| Genoomreplicatie | Synthese van nieuwe kopieën van ribonucleïnezuur | Polymerase-remmers |
| Opbouw en uitgang | Vorming van virionen | Capside-assemblagefout |
Pathogenese
Het primaire doelwit zijn volwassen enterocyten in de dunne darm. Beschadiging en functionele dysregulatie van de villi leiden tot verminderde water- en elektrolytenabsorptie en secretoire diarree. De snelle ontwikkeling van symptomen gaat gepaard met een massale afgifte van ontstekingsmediatoren en intestinale en gastrische motorische reflexen. [21]
Het virus is extreem stabiel in de omgeving: het kan wekenlang overleven op droge oppervlakken bij kamertemperatuur. Bij uitbraken kan de aerosol zich over een groot gebied verspreiden en voorwerpen en vloeren besmetten. Deze eigenschappen vormen de "perfecte" combinatie voor uitbraken. [22]
Immuunbescherming ontwikkelt zich, maar is vaak van korte duur en typespecifiek. Snelle antigene veranderingen in het capside-eiwit stellen het virus in staat om eerder gevormde neutraliserende antilichamen te ontwijken, wat de periodieke opkomst van "succesvolle" varianten ondersteunt, zoals de golven van GII.4-genotypes en de recente opkomst van GII.17. [23]
Zelfs na klinisch herstel kan iemand het virus nog wekenlang uitscheiden. Bij immuungecompromitteerde patiënten duurt de uitscheiding maanden en jaren, gaat gepaard met intrapopulatie-evolutie en kan leiden tot een recidiverend verloop. [24]
De ernst van de ziekte wordt bepaald door leeftijd, comorbiditeiten en de hoeveelheid vochtverlies. Uitdroging en elektrolytenonevenwichtigheden dragen het meest bij aan ongunstige uitkomsten, wat leidt tot acute nierfunctiestoornissen en andere complicaties als er niet snel wordt gerehydrateerd. [25]
Tabel. Belangrijkste mechanismen van pathogenese
| Mechanisme | Betekenis voor de kliniek |
|---|---|
| Schade en disfunctie van enterocyten | Verminderde opname van water en elektrolyten |
| Ontstekingsmediatoren | Misselijkheid, braken, buikpijn |
| Stabiliteit in de externe omgeving | Langdurige vervuiling van gebouwen |
| Antigene variabiliteit | Terugkerende infecties en uitbraken |
| Langetermijntoewijzing | Langdurig risico op overdracht na herstel |
Symptomen
De incubatietijd bedraagt gewoonlijk 12 tot 48 uur. De ziekte begint acuut, met misselijkheid, herhaaldelijk braken, waterige diarree, buikkrampen, zwakte en vaak lichte koorts. Bij jonge kinderen kan braken de overhand hebben op diarree. [26]
Symptomen duren doorgaans niet langer dan 1 tot 3 dagen, maar zwakte, verminderde eetlust en onstabiele stoelgang kunnen langer aanhouden. Het vochtverlies is afhankelijk van de frequentie van de stoelgang en het braken en bepaalt de noodzaak van medische hulp. [27]
Tekenen van uitdroging zijn onder meer dorst, droge slijmvliezen, verminderde urineproductie, duizeligheid en, bij kinderen, een ingevallen fontanel, lethargie en een gebrek aan tranen bij het huilen. Deze symptomen vereisen onmiddellijke beoordeling van de mate van uitdroging en rehydratie. [28]
Bij ouderen en mensen met chronische ziekten kan het verloop ernstiger zijn, met aanzienlijke verstoringen van de elektrolytenbalans. Immuungecompromitteerde patiënten zijn vatbaar voor langdurige diarree en gewichtsverlies. [29]
Zelfs zonder ernstige uitdroging ontwikkelen sommige mensen die van de ziekte zijn hersteld een postinfectieus syndroom met een verminderde darmmotiliteit en -gevoeligheid, wat zich uit in buikpijn, een opgeblazen gevoel en onstabiele ontlasting. [30]
Tabel: Symptomen per leeftijdsgroep
| Groep | Meest voorkomende manifestaties |
|---|---|
| Kinderen jonger dan 5 jaar | Herhaaldelijk braken, waterige diarree, koorts, risico op uitdroging |
| Tieners en volwassenen | Diarree en braken, krampende pijn, zwakte |
| Ouderen | Ernstige uitdroging, elektrolytstoornissen, bloeddrukdaling |
| Immuungecompromitteerd | Langdurige diarree, gewichtsverlies, langdurige virale uitscheiding |
Stadia
Het verloop van de ziekte kan worden onderverdeeld in een incubatie-, acute en herstelfase. De incubatiefase duurt 0,5 tot 2 dagen en is klinisch asymptomatisch, maar de primaire replicatie in enterocyten is al gaande. [31]
De acute fase duurt doorgaans 1 tot 3 dagen en wordt gekenmerkt door een piek in braken en een hoge stoelgangfrequentie. Tijdens deze periode is het risico op overdracht het hoogst, aangezien de virale uitscheiding zeer hoog is. [32]
De herstelfase vindt plaats gedurende de volgende dagen. De symptomen nemen af, de eetlust en de voedseltolerantie worden hersteld, maar zwakte en onstabiele ontlasting kunnen aanhouden. [33]
De uitscheiding van het virus via de ontlasting gaat door nadat de symptomen zijn verdwenen. Bij immuungecompromitteerde personen wordt de uitscheidingsfase chronisch en vereist speciale controlemethoden. [34]
Bij sommige patiënten ontwikkelen zich postinfectieuze functionele symptomen na de acute fase. Deze zijn niet geassocieerd met aanhoudende actieve ontsteking, maar kunnen de kwaliteit van leven aanzienlijk aantasten. [35]
Tabel. Indeling van de cursus
| Fase | Duur | Belangrijkste kenmerken |
|---|---|---|
| Incubatie | 0,5-2 dagen | Asymptomatische replicatie |
| Acuut | 1-3 dagen | Maximaal braken, diarree en besmettelijkheid |
| Herstellend | Een paar dagen | Vermindering van symptomen, behoud van zwakte |
| Langetermijntoewijzing | Weken en langer | Vooral bij immuungecompromitteerde personen |
Formulieren
De typische vorm is acute waterige gastro-enteritis. Een vorm met voornamelijk braken is mogelijk, vooral bij jonge kinderen, en een vorm met voornamelijk diarree bij volwassenen. Deze fenotypes bepalen de klinische tactiek van rehydratatie. [36]
Een ernstige vorm wordt waargenomen bij ouderen, bij mensen met comorbiditeiten en wanneer de rehydratatie laat wordt ingezet. Deze gaat gepaard met ernstige dehydratie, hypovolemie en elektrolytenonevenwichtigheden. [37]
De langdurige en chronische vorm is typisch voor patiënten met immunodeficiëntie: zij die een transplantatie hebben ondergaan, zij die immunosuppressiva krijgen, of zij met aangeboren immuundefecten. Maanden en jaren van virale uitscheiding en aanzienlijk gewichtsverlies zijn mogelijk. [38]
Voedselgerelateerde uitbraken komen vaak in clusters voor, waarbij de symptomen gelijktijdig optreden bij groepen mensen die een gemeenschappelijk voedsel delen. In dergelijke situaties zijn snel onderzoek, isolatie van patiënten en desinfectie cruciaal. [39]
Bij degenen die hersteld zijn, is een postinfectieuze functionele vorm met symptomen van het prikkelbare darmsyndroom mogelijk, waarvoor een gedifferentieerde aanpak nodig is en een uitleg aan de patiënt over de goedaardige aard van de aandoening. [40]
Tabel. Klinische vormen en behandelrichtlijnen
| Formulier | Voor wie is het kenmerkend? | Leidende tactieken |
|---|---|---|
| Typische acute | De meeste patiënten | Orale rehydratie, dieet indien verdragen |
| Variant met overheersend braken | Vaak kinderen | Lokale toepassing van anti-emetica, fractionele rehydratatie |
| Zwaar | Ouderen, comorbiditeit | Intraveneuze oplossingen, elektrolytbewaking |
| Chronisch bij immuungecompromitteerde patiënten | Getransplanteerde en andere immuundeficiënties | Langetermijnobservatie, correctie van immunosuppressie, experimentele benaderingen |
| Post-infectieuze functionele | Sommigen van degenen die herstelden | Educatie, dieettherapie, symptomatische ondersteuning |
Complicaties en gevolgen
De belangrijkste acute complicaties houden verband met uitdroging en elektrolytenonevenwichtigheden: hyponatriëmie, hypokaliëmie en metabolische veranderingen. Zonder tijdige rehydratie zijn acute nierfunctiestoornissen, collaps en toevallen bij kinderen mogelijk. [41]
Bij ouderen kan norovirus decompensatie van chronische aandoeningen veroorzaken. In langdurige zorginstellingen leiden uitbraken tot een toename van ziekenhuisopnames en sterfte als gevolg van onderliggende ziekten. [42]
Bij immuungecompromitteerde individuen ontwikkelt zich vaak langdurige diarree met gewichtsverlies, hypoproteïnemie en maandenlange virale uitscheiding, waarvoor multidisciplinaire monitoring nodig is. [43]
Onder de gevolgen op de lange termijn wordt een verhoogd risico op postinfectieuze functionele gastro-intestinale aandoeningen, waaronder het prikkelbaredarmsyndroom en dyspepsie, besproken. Het risico neemt toe in de eerste maanden na gastro-enteritis. [44]
Tenslotte kan langdurige verontreiniging van het milieu tijdens uitbraken secundaire gevallen in de hand werken, tenzij er strikte reinigings- en ontsmettingsvoorschriften op de locatie worden nageleefd. [45]
Tabel. Belangrijkste complicaties en risicofactoren
| Complicatie | Risicofactoren | Preventie |
|---|---|---|
| Ernstige uitdroging | Kinderen en ouderen, frequent braken | Vroege rehydratatie |
| Elektrolytstoornissen | Herhaalde dunne ontlasting en braken | Elektrolytenbewaking bij matige tot ernstige gevallen |
| Acute nierfunctiestoornis | Hypovolemie | Intraveneuze rehydratie indien geïndiceerd |
| Langdurige diarree | Immunodeficiëntie | Correctie van immunosuppressie, observatie |
| Postinfectieuze functionele klachten | Elke leeftijd na een ernstige episode | Training, dieettherapie, medicijnen indien geïndiceerd |
Diagnostiek
De "gouden standaard" voor laboratoriumbevestiging is de detectie van viraal ribonucleïnezuur door middel van kwantitatieve reverse transcriptie-polymerasekettingreactie (RPR) in feces. Moderne panels maken het mogelijk om belangrijke genotypes te typeren en de virale lading te beoordelen. [46]
In de routinematige praktijk is bij een typisch klinisch beeld en de aanwezigheid van een uitbraak niet altijd laboratoriumbevestiging nodig, maar in ernstige gevallen, bij ziekenhuisopname, uitbraken in instellingen en bij immuungecompromitteerde patiënten is testen wenselijk voor epidemiologische controle en uitsluiting van andere oorzaken. [47]
Snelle immunochromatografische antigeentesten zijn minder gevoelig dan op nucleïnezuur gebaseerde methoden en zijn geschikter voor indicatieve beoordelingen wanneer de middelen beperkt zijn. Geautomatiseerde moleculaire platforms versnellen de diagnose en verbeteren de detectiepercentages. [48]
Genotypering is nuttig voor epidemiologen. Dubbele typering van polymerase en capside helpt bij het volgen van de circulatie van recombinanten en de verandering in dominante afstammingslijnen, wat belangrijk is voor het beoordelen van seizoensdynamiek. [49]
Instrumentele diagnostiek is doorgaans niet nodig. Bloedonderzoek is gericht op het vaststellen van de mate van dehydratie en elektrolytenonevenwichtigheden. Beeldvormende methoden zijn alleen geïndiceerd bij een atypische klinische presentatie en bij verdenking op chirurgische pathologie. [50]
Tabel. Laboratoriumbevestigingsmethoden
| Methode | Voordelen | Nadelen | Wanneer kiezen |
|---|---|---|---|
| Omgekeerde transcriptie polymerasekettingreactie | Hoge gevoeligheid en specificiteit, typering | Vereist een laboratorium | Ziekenhuisopname, uitbraak, immunodeficiëntie |
| Antigeen-sneltest | Snel en gemakkelijk | Lagere gevoeligheid | Beperkte middelen |
| Sequentiebepaling van de polymerase- en capsideregio's | Surveillance, detectie van recombinanten | Er zijn middelen nodig | Openbare gezondheidscentra |
Differentiële diagnose
Het is belangrijk om norovirus-gastro-enteritis te onderscheiden van rotavirus- en sapovirusinfecties, bacteriële diarree, parasitaire infecties en niet-infectieuze oorzaken. Aanwijzingen voor norovirus zijn onder andere een fulminante aanvang, een combinatie van braken en waterige diarree, 'familiaire' en collectieve clusters, en winterse seizoensgebondenheid. Polymerasekettingreactie (PCR) kan helpen de diagnose te bevestigen. [51]
Bacteriële infecties gaan vaak gepaard met koorts, bloed en slijm, hevige pijn en vaak een langduriger verloop. Laboratoriumtests op basis van nucleïnezuur kunnen de oorzaak snel achterhalen en onnodige antibiotica vermijden. [52]
Bij kinderen moeten chirurgische oorzaken van braken en buikpijn worden uitgesloten op basis van klinische criteria en, indien nodig, worden doorverwezen voor beeldvorming. Bij vermoeden van een voedselgerelateerde ziekte is het epidemiologische verband met een specifiek product doorslaggevend. [53]
Bij immuungecompromitteerde personen is het belangrijk om op de hoogte te zijn van de mogelijkheid van gemengde infecties en langdurige virale uitscheiding. Een grondiger onderzoek naar de oorzaken is noodzakelijk in gevallen van langdurige ziekte en gewichtsverlies. [54]
Tabel: Verschillen tussen norovirus gastro-enteritis en andere oorzaken
| Teken | Norovirus | Bacteriële diarree | Parasitaire besmettingen |
|---|---|---|---|
| Begin | Scherp, uren | Vaker geleidelijk | Geleidelijk |
| Bloed in de ontlasting | Zelden | Vaak | Zelden |
| Braaksel | Heel vaak | Minder vaak | Soms |
| Duur | Meestal 1-3 dagen | Langer | Vaak wekenlang |
| Laboratoriumbevestiging | Polymerase-kettingreactie | Cultuur- of moleculaire panelen | Microscopie en moleculaire panelen |
Behandeling
De basis van de therapie is rehydratatie. Bij lichte tot matige dehydratatie heeft een orale rehydratatieoplossing met een lage osmolariteit de voorkeur. Het aanbevolen volume voor de eerste 2-4 uur is 50-100 milliliter per kilogram lichaamsgewicht, gevolgd door een dosis van 10 milliliter per kilogram na elke episode van losse ontlasting en 2 milliliter per kilogram na een episode van braken. Vroeg voeden in kleine porties versnelt het herstel. [55]
Bij ernstige dehydratie is intraveneuze rehydratie geïndiceerd volgens standaardregimes met monitoring van natrium, kalium, ureum en creatinine. De keuze van de oplossingen en de infusiesnelheid worden bepaald door de ernst en de bijbehorende aandoeningen, vooral bij ouderen. [56]
Om braken bij kinderen ouder dan 6 maanden in noodsituaties te verminderen, is een enkele dosis ondansetron acceptabel. Dit vergemakkelijkt orale rehydratatie en vermindert de noodzaak voor intraveneuze infusen. Regelmatig gebruik buiten een ziekenhuisomgeving wordt niet aanbevolen. Bij volwassenen is kortdurend symptomatisch gebruik onder medisch toezicht mogelijk, indien geïndiceerd. [57]
Zink in een dosis van 10-20 milligram per dag gedurende 10-14 dagen wordt aanbevolen voor kinderen jonger dan 5 jaar om de duur en ernst van diarree te verminderen, vooral in gebieden met beperkte middelen. Antibacteriële geneesmiddelen zijn niet geïndiceerd voor norovirus. Probiotica hebben een tegenstrijdige bewijsbasis en zijn geen verplicht onderdeel van de therapie. [58]
Specifieke antivirale therapie is nog in de onderzoeksfase. Nitazoxanide is onderzocht bij immuungecompromitteerde patiënten, maar heeft nog geen overtuigend voordeel aangetoond in systematische modellen en individuele onderzoeken. Favipiravir heeft antivirale activiteit aangetoond door mutagenese-inductie in beperkte onderzoeken, maar is niet goedgekeurd voor de behandeling van norovirus. Kandidaten, zoals virale proteaseremmers, bevinden zich in de preklinische en vroege klinische fase. Hun gebruik is alleen mogelijk binnen de context van onderzoeken en op individuele basis. [59]
Tabel. Managementtactieken naar ernst
| Rang | Tekenen | Tactiek |
|---|---|---|
| Licht | Dorst, matige zwakte, behouden diurese | Orale rehydratie, fractioneel drinken, voeding zoals verdragen |
| Gemiddeld | Droge slijmvliezen, verminderde diurese, tachycardie | Verbeterde orale rehydratatie, elektrolytenbeoordeling, ondansetron indien geïndiceerd |
| Zwaar | Ernstige zwakte, ernstige oligurie, orthostatische verschijnselen | Intraveneuze vloeistoffen, elektrolytenbewaking, ziekenhuisopname |
Preventie
Handen wassen met zeep blijft een belangrijke maatregel. Antiseptica op alcoholbasis zijn minder effectief tegen norovirus, vooral in gevallen van zichtbaar besmette oppervlakken. Reiniging en desinfectie van de uitbraak vereist bleekoplossingen met een concentratie van 1000-5000 ppm actief chloor, die minstens 5 minuten moeten inwerken en vervolgens moeten worden afgespoeld. [60]
Personeel van de voedselvoorziening en alle werknemers die in contact komen met voedsel, moeten na het verdwijnen van de symptomen ten minste 48 uur vrij blijven van het werk. In gebieden met een uitbraak wordt aanbevolen om gemeenschappelijke eetruimtes te sluiten, de bewegingsvrijheid van patiënten en personeel te beperken en de schoonmaak te intensiveren. [61]
Voedselveiligheid vereist het wassen van fruit en groenten, het koken van schaaldieren, het voorkomen van kruisbesmetting en een strikte persoonlijke hygiëne. In geval van geïsoleerd braken is uitgebreide desinfectie van de omgeving van de episode noodzakelijk. [62]
Vaccinprofylaxe is in ontwikkeling. De meest geavanceerde kandidaat, gebaseerd op virusachtige deeltjes, HIL-214, voldeed niet aan de primaire en secundaire werkzaamheidseindpunten in een grootschalig onderzoek onder zuigelingen, wat leidde tot de stopzetting van het programma. Er wordt nog steeds gewerkt aan andere platforms, waaronder die gebaseerd op immunologische correlaties van bescherming en gegevens uit onderzoeken met jonge kinderen. [63]
Uitbraakmanagement in instellingen omvat snelle bewaking, isolatie van gevallen, verbeterde schoonmaak en training van personeel. Deze maatregelen zijn effectief gebleken in het verminderen van secundaire gevallen en de duur van de uitbraak. [64]
Tabel. Praktische preventieve maatregelen
| Meeteenheid | Concrete acties |
|---|---|
| Handhygiëne | Was u na toiletgebruik en voor het eten minstens 20 seconden met zeep |
| Desinfectie | Chlooroplossing 1000-5000 ppm, 5 minuten vasthouden |
| Voedselveiligheid | Warmtebehandeling van schaaldieren, snijplanken, koeling van afgewerkte gerechten |
| Schorsing van het werk | Ten minste 48 uur nadat de symptomen zijn verdwenen |
| Flitsbesturing | Isolatie, verbeterde reiniging, informatie en training van personeel |
Voorspelling
Bij de meeste patiënten is de ziekte zelflimiterend en resulteert deze binnen enkele dagen in volledig herstel met snelle rehydratie. De prognose wordt bepaald door leeftijd, comorbiditeiten en toegang tot medische zorg. [65]
De slechtste uitkomsten houden verband met vertraagde rehydratatie bij kinderen en ouderen. Tijdige correctie van vocht- en elektrolytenverlies voorkomt vrijwel volledig levensbedreigende complicaties. [66]
Er bestaat een risico op postinfectieuze functionele stoornissen, maar de absolute waarden zijn matig. De meeste symptomen verdwijnen na verloop van tijd met de juiste patiëntenvoorlichting en ondersteunende therapie. [67]
Bij immuungecompromitteerde patiënten hangt de prognose af van de beheersing van de onderliggende aandoening, mogelijke correctie van de immunosuppressie en toegang tot ondersteunende zorg. Voor deze groep is een multidisciplinaire aanpak vereist. [68]
Vanuit het perspectief van de volksgezondheid kunnen betrouwbare hygiënische en organisatorische maatregelen uitbraken aanzienlijk beperken en de belasting van ziekenhuizen tijdens het seizoen verminderen. [69]
Tabel. Prognosefactoren
| Factor | Invloed |
|---|---|
| Leeftijd tot 5 jaar en ouder dan 65 jaar | Verhoogd risico op uitdroging en ziekenhuisopname |
| Geassocieerde ziekten | Verhoogd risico op complicaties |
| Tijd om te beginnen met rehydratatie | Hoe eerder, hoe beter het resultaat. |
| Immuunstatus | Bij immuundeficiëntie is een langdurig beloop mogelijk |
| Niveau van zorgorganisatie | Het verminderen van secundaire gevallen en de duur van uitbraken |
Veelgestelde vragen
Hoe lang duurt de besmettelijkheid na herstel?
Het virus kan nog wekenlang worden verspreid nadat de symptomen zijn verdwenen, dus het handhaven van een goede hygiëne en het vermijden van voedselcontact gedurende ten minste 48 uur blijft cruciaal. [70]
Kan norovirus met antibiotica worden behandeld?
Nee. Het is een virale infectie, dus antibiotica zijn niet effectief en niet geïndiceerd. De belangrijkste behandeling is rehydratatie en symptomatische ondersteuning. [71]
Zijn er effectieve antivirale middelen?
Specifieke middelen voor routinematig gebruik zijn nog niet goedgekeurd. Nitazoxanide en andere kandidaten zijn onderzocht, maar er zijn geen overtuigende gegevens voor wijdverbreid gebruik; gerichte oplossingen via onderzoek zijn mogelijk. [72]
Bestaat er een vaccin?
Er worden verschillende platformen ontwikkeld, maar de meest geavanceerde kandidaat, HIL-214, bleek niet effectief in een grootschalig onderzoek onder zuigelingen. De ontwikkeling is gaande, rekening houdend met nieuwe immunologische criteria. [73]
Hoe maak je schoon na een braakaanval?
Gebruik een chlooroplossing met 1000-5000 ppm, laat deze minstens 5 minuten intrekken en verwijder zichtbaar vuil. Behandel vervolgens de omliggende huid. Was je handen met zeep. [74]

