Medisch expert van het artikel
Nieuwe publicaties
T-cel lymfomen van de huid
Laatst beoordeeld: 04.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
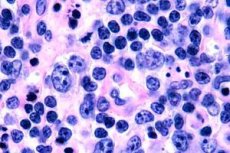
T-cellymfomen worden meestal vastgesteld bij ouderen, hoewel er ook bij kinderen geïsoleerde gevallen van de ziekte voorkomen. Mannen zijn twee keer zo vaak ziek als vrouwen. T-cellymfomen zijn epidermotroop van aard.
Oorzaken T-cel lymfomen van de huid
De oorzaken en pathogenese van cutane T-cellymfomen zijn nog niet volledig bekend. Momenteel beschouwen de meeste onderzoekers het humaan T-celleukemievirus type 1 (HTLV-1) I als de belangrijkste etiologische factor die de ontwikkeling van maligne T-cellymfomen van de huid initieert. Daarnaast wordt de rol van andere virussen bij de ontwikkeling van T-cellymfoom besproken: het Epstein-Barr-virus en herpes simplex type 6. Bij patiënten met T-cellymfoom worden virussen aangetroffen in de huid, het perifere bloed en Langerhanscellen. Bij veel patiënten met mycosis fungoides worden antilichamen tegen HTLV-I aangetroffen.
Een belangrijke rol in de pathogenese van T-cellymfomen wordt gespeeld door immunopathologische processen in de huid, waarvan de belangrijkste de ongecontroleerde proliferatie van klonale lymfocyten is.
Cytokinen geproduceerd door lymfocyten, epitheelcellen en cellen van het macrofaagsysteem hebben pro-inflammatoire en proliferatieve effecten (IL-1, verantwoordelijk voor de differentiatie van lymfocyten; IL-2 - T-celgroeifactor; IL-4 en IL-5, die de instroom van eosinofielen in de laesie en hun activering verhogen, enz.). Als gevolg van de instroom van T-lymfocyten in de laesie ontstaan Pautrier-microabcessen. Gelijktijdig met de toename van de lymfocytenproliferatie wordt de activiteit van antitumorcellen onderdrukt: natural killers, lymfocytotoxische lymfocyten, dendritische cellen, met name Langerhanscellen, evenals cytokinen (IL-7, IL-15, enz.) - tumorgroeiremmers. De rol van erfelijke factoren kan niet worden uitgesloten. De aanwezigheid van familiale gevallen en de frequente detectie van bepaalde histocompatibiliteitsantigenen (HLA B-5 en HLA B-35 bij zeer kwaadaardige huidlymfomen, HLA A-10 bij minder agressieve lymfomen, HLA B-8 bij de erythrodermische vorm van mycosis fungoides) bevestigen het erfelijke karakter van de dermatose.
Klinische observaties wijzen op een mogelijke transformatie van chronische dermatosen (neurodermitis, atopische dermatitis, psoriasis, enz.) naar mycosis fungoides. De sleutelfactor is de langdurige persistentie van lymfocyten in de ontstekingshaard, die de immuunbewaking verstoort en de vorming van een kloon van kwaadaardige lymfocyten en daarmee de ontwikkeling van een kwaadaardig proliferatief proces bevordert.
De invloed van fysieke factoren op het lichaam, zoals zonlicht, ioniserende straling en chemische stoffen, kan leiden tot het ontstaan van een kloon van ‘genotraumatische’ lymfocyten die een mutageen effect hebben op lymfoïde cellen en tot de ontwikkeling van kwaadaardige lymfocyten.
T-cellymfomen kunnen daarom worden beschouwd als een multifactoriële ziekte die begint met de activering van lymfocyten onder invloed van verschillende carcinogene, "genotraumatiserende" factoren en het ontstaan van een dominante T-celkloon. De ernst van de immuunsurveillancestoornis, de kloon van kwaadaardige lymfocyten, bepaalt de klinische manifestaties (gevlekte lymfocyten, plaque of tumorelementen) van T-cellymfomen.
Pathogenese
In het vroege stadium van mycosis fungoides worden acanthose met brede uitlopers, hyperplasie en verdichting van basale keratinocyten, vacuolaire degeneratie van enkele basale cellen, atypische mitosen in verschillende lagen van de opperhuid en epidermotropie van het infiltraat met penetratie van lymfocyten in de opperhuid waargenomen. In de opperhuid worden kleine infiltraten rond de bloedvaten waargenomen, bestaande uit mononucleaire cellen met hyperchrome kernen – "mycotische" cellen. In het tweede stadium wordt een toename van de ernst van het dermale infiltraat en epidermotropie van de infiltraatcellen waargenomen, waardoor kwaadaardige lymfocyten de opperhuid binnendringen en clusters vormen in de vorm van microabcessen van Potrier. In het derde stadium, het tumorstadium, worden massieve acanthose en lichte atrofie van de opperhuid waargenomen, evenals een verhoogde infiltratie van de opperhuid door tumorlymfocyten, die meerdere Potrier-microabcessen vormen. Het massieve infiltraat bevindt zich over de gehele dikte van de dermis en bedekt een deel van de hypodermis. Er worden blastvormen van lymfocyten waargenomen.
Cutaan groot anaplastisch T-cellymfoom
Het wordt vertegenwoordigd door een groep lymfoproliferatieve processen die worden gekenmerkt door de aanwezigheid van proliferaties van atypische klonale grote anaplastische CD30+ T-cellen. Het ontwikkelt zich doorgaans secundair in het tumorstadium van mycosis fungoides of bij het syndroom van Sézary, maar kan zich onafhankelijk ontwikkelen of met verspreiding van systemische lymfomen van dit type. Klinisch gezien komen dergelijke lymfomen overeen met de zogenaamde gedecapiteerde vorm van mycosis fungoides in de vorm van enkele of meerdere lymfeklieren, meestal gegroepeerd.
Histologisch gezien beslaat de proliferatie bijna de gehele dermis, met of zonder epidermotropie in het geval van epidermale atrofie.
Cytologisch gezien kunnen tumorcellen variëren in grootte en vorm. Op basis van deze eigenschappen wordt onderscheid gemaakt tussen middel- en grootcellig pleomorf T-cellymfoom met kernen van verschillende onregelmatige configuraties - gekronkeld, meerlobbig, met dicht chromatine, een goed gedefinieerde nucleolus en vrij overvloedig cytoplasma; immunoblastisch - met grote ronde of ovale kernen met helder karyoplasma en één centraal gelegen nucleolus; anaplastisch - met lelijke, zeer grote cellen met kernen van onregelmatige configuratie en overvloedig cytoplasma. Fenotypisch behoort deze hele groep tot T-helperlymfomen en kan CD30+ of CD30- zijn.
R. Willemze et al. (1994) toonden aan dat het beloop van CD30+-lymfoom gunstiger is. Genotypisch wordt een klonale herschikking van de T-lymfocytreceptor gedetecteerd.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
Symptomen T-cel lymfomen van de huid
De meest voorkomende aandoening in de groep T-cellymfomen van de huid is mycosis fungoides, goed voor ongeveer 70% van de gevallen. Er zijn drie klinische vormen van de ziekte: klassiek, erythrodermisch en onthoofd. T-cellymfomen worden gekenmerkt door een polymorfisme van huiduitslag in de vorm van vlekken, plaques en tumoren.
De erythrodermische vorm van mycosis fungoides begint meestal met oncontroleerbare jeuk, zwelling, algehele hyperemie, het verschijnen van erythemateuze-plaveiselcellaesies op de huid van de romp en ledematen, die de neiging hebben om binnen 1-2 maanden samen te smelten en erytrodermie te ontwikkelen. Bijna alle patiënten hebben palmoplantaire hyperkeratose en diffuse haaruitval over de gehele huid. Alle groepen lymfeklieren zijn sterk vergroot. Vergrote inguinale, femorale, axillaire en cubitale lymfeklieren worden gepalpeerd als "pakketjes" van dichte elastische consistentie, niet vergroeid met omliggend weefsel, pijnloos. De algemene toestand verslechtert sterk: koorts met een lichaamstemperatuur tot 38-39 °C, nachtelijk zweten, zwakte en gewichtsverlies treden op. Momenteel wordt het Sézary-syndroom door veel dermatologen beschouwd als de zeldzaamste leukemische variant van de erythrodermische vorm van mycosis fungoides.
Op lymfocytogrammen wordt een uitgesproken leukocytose vastgesteld - Sezary-cellen. Sezary-cellen zijn kwaadaardige T-helpercellen, waarvan de kernen een geplooid cerebriform oppervlak hebben met diepe instulpingen van het kernmembraan. Na 2-5 jaar treedt een fatale afloop op, vaak veroorzaakt door cardiovasculaire pathologie en intoxicatie.
De gedecapiteerde vorm van mycosis fungoides wordt gekenmerkt door de snelle ontwikkeling van tumorachtige laesies op een ogenschijnlijk gezonde huid zonder voorafgaande langdurige plaquevorming. Deze vorm wordt gekenmerkt door een hoge maligniteitsgraad, wat wordt beschouwd als een manifestatie van lymfosarcoom. Een fatale afloop wordt binnen een jaar waargenomen.
Stages
De klassieke vorm van mycosis fungoides wordt gekenmerkt door drie ontwikkelingsstadia: erythemateus-plaveiselcelcarcinoom, plaque en tumor.
Het eerste stadium lijkt op het klinische beeld van sommige goedaardige inflammatoire dermatosen - eczeem, seborroïsch eczeem, plaque parapsoriasis. In dit stadium van de ziekte worden vlekken van verschillende grootte waargenomen, intens roze, rozerood met een paarse tint, ronde of ovale contouren, met relatief duidelijke grenzen, oppervlakkige zemelachtige of dunne schilfering. De elementen bevinden zich vaak op verschillende huidgebieden, meestal op de romp en het gezicht. Geleidelijk neemt hun aantal toe. Na verloop van tijd kan het proces het karakter van erytrodermie aannemen (erytrodermische fase). De huiduitslag kan jarenlang aanhouden of spontaan verdwijnen. In tegenstelling tot goedaardige inflammatoire dermatosen zijn de elementen van de huiduitslag en jeuk in dit stadium resistent tegen de behandeling.
Het infiltratieve plaquestadium ontwikkelt zich over meerdere jaren. In plaats van de eerder bestaande gevlekte huiduitslag verschijnen plaques met ronde of onregelmatige contouren, intens paars van kleur, duidelijk afgebakend van de gezonde huid, dicht en met een schilferig oppervlak. Hun consistentie lijkt op "dik karton". Sommige plaques verdwijnen spontaan, waardoor er donkerbruine hyperpigmentatie en/of atrofie (poikiloderma) achterblijft. Jeuk is in dit stadium nog intenser en pijnlijker, koorts en gewichtsverlies worden waargenomen. Lymfadenopathie kan in dit stadium worden waargenomen.
In het derde, tumorstadium, verschijnen pijnloze tumoren met een dichte, elastische consistentie, geelrood van kleur, die zich ontwikkelen vanuit plaques of ontstaan op een ogenschijnlijk gezonde huid. De vorm van de tumoren is bolvormig of afgeplat, vaak lijkend op een paddenstoelhoed. Tumoren kunnen overal voorkomen. Hun aantal varieert sterk van enkel tot tientallen, met een diameter van 1 tot 20 cm. Wanneer lang bestaande tumoren uiteenvallen, vormen zich zweren met onregelmatige randen en een diepe bodem, die de fascia of het bot bereiken. De lymfeklieren, milt, lever en longen worden het vaakst aangetast. De algemene toestand verslechtert, intoxicatiesymptomen verschijnen en nemen toe, en er ontwikkelt zich zwakte. De gemiddelde levensverwachting van patiënten met de klassieke vorm van mycosis fungoides vanaf het moment van diagnose is 5 tot 10 jaar. Sterfte wordt meestal waargenomen als gevolg van bijkomende ziekten: longontsteking, cardiovasculair falen, amyloïdose. Subjectief wordt jeuk gevoeld, en wanneer tumoren uiteenvallen, pijn in de getroffen gebieden.
Wat moeten we onderzoeken?
Hoe te onderzoeken?
Behandeling T-cel lymfomen van de huid
In het erythemateuze-plaveiselcelstadium hebben patiënten geen antitumortherapie nodig; ze krijgen topische corticosteroïden voorgeschreven (prednisolon, betamethason, dexamethasonderivaten), interferon alfa (3 miljoen IE per dag, daarna 3 keer per week gedurende 3-6 maanden, afhankelijk van de klinische manifestaties of de effectiviteit van de behandeling), interferon gamma (100.000 IE per dag gedurende 10 dagen, de cyclus wordt 12-3 keer herhaald met een pauze van 10 dagen), PUVA-therapie of Re-PUVA-therapie. De effectiviteit van PUVA-therapie is gebaseerd op de selectieve vorming van covalente crosslinks van psoralenen met DNA in prolifererende T-helpercellen, wat hun deling remt. In de tweede fase worden, naast de bovengenoemde middelen, systemische corticosteroïden (30-40 mg prednisolon per dag gedurende 1,5-2 maanden) en cytostatica (prospedine 100 mg per dag, in totaal 4-5 injecties) gebruikt. De combinatie van interferonen met andere therapiemethoden heeft een sterker therapeutisch effect (interferonen + PUVA, interferonen + cytostatica, interferonen + aromatische retinoïden).
In het tumorstadium is polychemotherapie de belangrijkste behandeling. Een combinatie van vincristine (0,5-1 mg intraveneus eenmaal daags, in totaal 4-5 injecties) met prednisolon (40-60 mg per dag oraal tijdens chemotherapie), prospidine (100 mg per dag, in totaal 3 g) en interferonen wordt gebruikt. Fotodynamische therapie, elektronenbundeltherapie en fotoferese (extracorporale fotochemotherapie) worden aanbevolen.

