Medisch expert van het artikel
Nieuwe publicaties
De rol van veranderingen in het subchondrale bot in de pathogenese van osteoartritis
Laatst beoordeeld: 19.10.2021

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
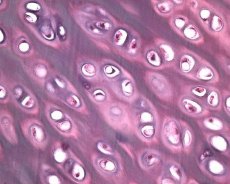
Samen met de degeneratie van gewrichtskraakbeen, omvat het pathologische proces bij osteoartritis het onderliggende botweefsel. Er wordt gesuggereerd dat de verdikking van de subchondrale plaat de progressie van osteoartritis bevordert. Naarmate er meer osteoartritis vordert, wordt gewrichtskraakbeen, dat een object is voor mechanische en chemische stress, langzaam aangetast als gevolg van een onevenwichtigheid in de processen van katabolisme en kraakbeenherstel. In het bijzonder draagt mechanische spanning met betrekking tot de "gewichtdragende" lichaamsmassa van de gewrichten bij aan de vorming van een groot aantal micro-fracturen in de subchondrale plaat en het kraakbeen. Naarmate het gewrichtskraakbeen erodeert, neemt de sclerose van het subchondrale bot toe, neemt de stijfheid van het botweefsel toe, wat op zijn beurt bijdraagt aan een verdere verstoring van de gewrichtskraakbeenstructuur. De vraag naar de primaire of secundaire aard van veranderingen in het subchondrale bot bij osteoartrose blijft echter onopgelost.
Tot voor kort werd aangenomen dat de radiografisch bepaalde veranderingen in de sponsachtige substantie van het subchondrale bot, zoals sclerose of cystevorming, bij patiënten met artrose secundair zijn. De resultaten van klinische en experimentele onderzoeken wijzen echter op een mogelijke initiërende rol van subchondraal bot in de pathogenese van osteoartritis. Eén mogelijk mechanisme is een sterke toename in de stijfheidsgradiënt van het subchondrale bot vanwege het feit dat de integriteit van het juiste kraakbeenweefsel afhankelijk is van de mechanische eigenschappen van het "bed" van het bot. Studies bij primaten hebben aangetoond dat veranderingen in het subchondrale bot vooraf kunnen gaan aan veranderingen in gewrichtskraakbeen. Het bewijs in de modellen van osteoartrose bij dieren en klinische studies van bewijs ter ondersteuning van deze hypothese en daar tegen, heeft de discussie alleen maar verergerd. Het verdikken van trabeculae in het subchondrale bot gaat niet altijd gepaard met een toename in mineralisatie van botweefsel, of beter gezegd, een toename van het volume van de osteoïde. Dit teken van abnormale mineralisatie geeft aan dat een verstoring in de regulatie van botremodellering een integraal onderdeel is van osteoartrose, en ondersteunt ook het concept van botweefseldefect bij osteoartritis. De J. Dequeker-groep (1989) beschouwt de laatste als een "gegeneraliseerde metabole botziekte".
Botweefsel wordt voortdurend bijgewerkt. Dit dynamische proces, genaamd botremodellering, is een complexe opeenvolging van processen van resorptie en mineralisatie. Osteoclasten resorberen botweefsel en osteoblasten scheiden eiwitten af die de belangrijkste organische component vormen voor mineralisatie. Onderwijs en botafbraak bij toeval tegenkomen het skelet, het is - een geprogrammeerde proces dat plaatsvindt in verschillende delen van het skelet, die bekend staat als botremodellering units. Aan het begin van de cyclus verschijnen osteoclasten op het inactieve oppervlak; Binnen 2 weken vormen ze een tunnel in de corticale botlaag of lacune op het oppervlak van het trabeculaire bot. De frequentie van activering van nieuwe botremodellerende eenheden bepaalt de mate van botweefselvernieuwing. Bij een gezonde jongere zijn de processen van vorming en resorptie van botweefsel in evenwicht, de normale massa botweefsel wordt gehandhaafd. Hormonale regulatie van botresorptie tenminste PTH en PGE 2, aanwezig niet alleen door osteoclasten en osteoblasten, maar de werking van deze hormonen vrijkomen factoren die botresorptie door osteoclasten stimuleert. Momenteel zijn er meer dan 12 lokale en systemische regulator van botgroei invloed zijn remodelleren, met name PTH, 1,25 (OH) 2 D 3, calcitonine, groeihormoon, glucocorticoïden, schildklierhormonen, insuline, IGF (1 en 2), oestrogenen, PGE 2, androgenen.
Botcellen geven een aantal eiwitten en cytokinen af, die endocriene regulatie en signaaloverdracht uitvoeren. Eiwitten geproduceerd door osteoblasten omvatten botmatrixeiwitten zoals collageen, osteopontine, osteocalcine, bot-sialoproteïnen. Bovendien geven deze cellen proteasen af, zowel in actieve als latente vorm, die deelnemen aan het proces van botremodellering - MMP, componenten van het plasminogeenactivator (AP) / plasmine-activatorsysteem. De cytokinen die vrijkomen door osteoblasten kunnen zowel werken door autocriene mechanismen als door paracrine tot lokale cellen (andere osteoblasten, osteoclasten).
Het is nog niet bekend op welke manier deze signalen worden gereguleerd - door mechanische stress of andere chemische signalen die worden veroorzaakt door mechanische stress. Het is echter bekend dat herhaalde mechanische stress lokale proliferatie van botcellen en / of eiwitten veroorzaakt. In vivo kan mechanische stress osteoblasten activeren, cyclische nucleotideniveaus verhogen, prostaglandinen produceren en ook morfologische veranderingen veroorzaken die zijn geassocieerd met botremodellering. Onder omstandigheden in vitro spanning induceert proliferatie van osteoblasten cultuur mRNA expressie van botproteïnen betrokken bij de vorming van osteoïd mineralisatie en in het proces, de afgifte van lokale groeifactoren zoals IGF-1 en IGF-2 en adhesiemoleculen. De transmissie van een signaal van mechanische spanning kan worden bewerkstelligd door mechanisch gevoelige ionkanalen.
Er zijn indirecte aanwijzingen voor een gestoorde osteoblastfunctie bij osteoartritis. G. Gevers en J. Dequeker (1987) laten een toename in serum osteocalcine bij vrouwen met artrose van de gewrichten van de handen, en explantaten corticaal botoppervlak, wat suggereert dat de pathologie van het botweefsel deel van osteoartritis kan worden. Bij autopsie werd niet alleen de verdikking van het subchondrale bot gedetecteerd, maar ook de abnormaal lage mineralisatie van de heupkop. Bij cavia's met chirurgisch geïnduceerde osteoartritis werd een significante verdikking van de botfractie in de subchondrale zone gedetecteerd met behulp van computertomografie. Een onbalans tussen collageen en niet-collagene (osteocalcine etc.) Eiwitten kunnen botvolume verhogen, maar heeft geen invloed op de dichtheid van mineralen. Volgens M. Shimizu et al (1993), de progressie van de degeneratieve veranderingen in het kraakbeen geassocieerd met intensere remodellering van het subchondrale bot en verhoging van de stijfheid, waarop ook een defect in botcellen artrose. Volgens de voorgestelde V. Lee en M. Aspden (1997) hypothese van gebrekkige proliferatie van botcellen leidt tot een toename van de hardheid van het bot, maar geen verhoging van de minerale dichtheid veroorzaken.
CI Westacott en co-auteurs (1997) veronderstelden dat abnormale osteoblasten direct het metabolisme van kraakbeenweefsel beïnvloeden. Het kweken van osteoblasten bij patiënten met artrose chondrocyten met mensen die geen ziekten van de gewrichten hadden, de auteurs waargenomen een significante verandering in de release van glycosaminoglycanen normaal kraakbeenweefsel in vitro, maar het niveau van cytokinevrijstelling bleef ongewijzigd. G. Hilal et al (1998) toonden aan dat kweken van osteoblasten subchondrale bot van patiënten met artrose in vitro heeft een veranderd metabolisme - Systeemactiviteit AP / plasmine en IGF-1 in deze cellen wordt verhoogd. De waarneming van CI Westacott et al. (1997) kan worden verklaard door een toename in protease-activiteit in subchondrale botcellen.
Het blijft onbekend of osteoartrose veranderingen in het subchondrale bot initieert of bijdraagt aan de progressie ervan. DK Dedrick et al (1993) hebben aangetoond dat bij honden met chirurgisch geïnduceerde osteoarthritis subchondrale bot verdikking is geen vereiste voor het ontwikkelen van osteoartrozpodobnyh veranderingen in gewrichtskraakbeen, maar draagt bij aan de progressie van degeneratieve processen in het kraakbeen. De resultaten van de studie van A. Sa'ied en co-auteurs (1997) zijn in tegenspraak met de gegevens van de vorige studie. Middels echografie 50 MHz voor de evaluatie van de initiële morfologische veranderingen en de voortgang volgens het articulair kraakbeen en bot in experimentele osteoartritis geïnduceerde monoyoduksusnoy zuur injecties in het kniegewricht van de rat, hebben we gelijktijdig procesveranderingen in bot en kraakbeen gedurende de eerste drie dagen na injectie aangetoond.
Osteoblasten groeifactoren en cytokinen die deelnemen aan de plaatselijke hermodellering van botweefsel, wat kan bijdragen tot remodelleren van kraakbeenweefsel op passende "dragergewicht" gewrichten na de penetratie door microscheurtjes in de verkalkte laag van kraakbeen. Bovendien worden de producten van de uitscheiding van botcellen gevonden in de synoviale vloeistof. De meest waarschijnlijke producten uitgescheiden abnormale osteoblasten kunnen lokaal proces remodeling kraakbeen werking TGF-b en bot morfometrische proteïnen (ILC). Beide vertegenwoordigers van de TGF-familie onderscheiden zich door chondrocyten en osteoblasten en beide zijn in staat om de hermodellering van zowel bot- als kraakbeenweefsel te modificeren. Martel J. Pelletier et al (1997) een toename waar TGF-P niveaus in het subchondrale bot explantaten artrose patiënten vergeleken met gezonde individuen, wat wijst op een mogelijke rol van deze groeifactor in de pathogenese van osteoartritis. IGF wordt ook geproduceerd door osteoblasten. In de cultuur van osteoblast-achtige cellen verkregen van patiënten met osteoartritis, is een toename in het niveau van IGF dat het metabolisme van kraakbeen verandert gevonden.
TGF-b, IGF, de Commissie en de cytokinen geproduceerd door osteoblasten in het subchondrale bot kunnen de productie van collagenase en andere proteolytische enzymen beïnvloeden het kraakbeen, die op zijn beurt kan bijdragen tot verbouwing / afbraak van de kraakbeenmatrix. Het blijft onduidelijk of de osteoblasten produceren OA minder macrofaag koloniestimulerende factor (M-CSF - een stimulator van botresorptie) dan normale cellen. Onderzoeksresultaten AG Uitterlinden en medewerkers (1997) liet zien dat een rol in de vorming van osteofyten receptoren een vitamine D, die door osteoblasten tot expressie kunnen spelen en de expressie van verschillende factoren gesynthetiseerd door deze cellen, die deels verklaart de rol van osteoblasten in de pathogenese van deze ziekte.
Gegeven de resultaten van de bovengenoemde studies, G. Hilal et al (1998), J. Martel-Pelletier et al (1997) hebben de volgende werkhypothese relatie remodeling subchondrale bot en kraakbeen bij artrose juiste voorgesteld. In een vroege of verlengde fase van OA-pathogenese wordt het proces van remodelering van botweefsel in het subchondrale bot geïntensiveerd. Tegelijkertijd repetitieve belasting leidt tot lokale microfracturen en / of het uiterlijk van het systeemonbalans IGF / IGF-svyazyvayushy eiwit (IGFBP) door een abnormale reactie van osteoblasten subchondrale bot, die zijn sclerosis bevordert. De laatste kan op zijn beurt bijdragen aan het verschijnen van micro-fracturen van het juiste kraakbeen en schade aan zijn matrix.
Onder normale omstandigheden wordt deze schade geëlimineerd door lokale synthese en afgifte van IGF-1 en IGF-bindend eiwit, dat de vorming van ECM van gewrichtskraakbeen stimuleert. Tegelijkertijd bevordert het PD-systeem de groei van subchondrale botcellen en de vorming van botmatrix. Anabole activiteit van IGF-systeem toegenomen subchondrale bot bij patiënten met artrose, terwijl lokale activatie systeem SA / plasmine (lokale regulator van IGF-systeem) in het gewrichtskraakbeen veroorzaakt de lokale wijzigingen. In osteoblasten bij artrose IGF-1 beschrijft de regulering van AP plasmine soort positieve feedback, dus kan remodelleren van botweefsel, die uiteindelijk leidt tot de subchondrale sclerose remmen. Dus in het bot en kraakbeen lokale inductie van IGF-1 iproteaz leidt, enerzijds, de schade aan het kraakbeen, de andere - een verdikking van het subchondrale bot, de laatstgenoemde op zijn beurt stimuleert verdere kraakbeenschade. De onbalans tussen de kraakbeenschade geassocieerd met subchondrale sclerose en de herstelcapaciteit, leidt tot progressieve veranderingen in het kraakbeen ECM en de ontwikkeling van osteoartritis. Volgens de auteurs verklaart deze hypothese ook de trage progressie van de ziekte.

