Medisch expert van het artikel
Nieuwe publicaties
Medicijnen
Neuroleptica of antipsychotica
Last reviewed: 04.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Antipsychotica (neuroleptica) zijn een klasse psychotrope geneesmiddelen die voornamelijk worden gebruikt voor de behandeling van schizofrenie. Tegenwoordig worden er twee groepen (of categorieën) geneesmiddelen onderscheiden: klassieke en atypische antipsychotica. Hieronder vindt u informatie over de farmacologische eigenschappen, indicaties en bijwerkingen van elk van deze groepen geneesmiddelen.
Indicaties voor het gebruik van klassieke antipsychotica
Volgens de aanbevelingen van gezaghebbende onderzoekers op het gebied van psychofarmacotherapie zijn de belangrijkste indicaties voor het voorschrijven van traditionele neuroleptica momenteel als volgt.
- Verlichting van psychomotorische agitatie en gedragsstoornissen veroorzaakt door ernstige psychotische symptomen. In deze gevallen is het gebruik van orale of parenterale vormen van geneesmiddelen met antipsychotische werking geïndiceerd, zowel globaal (clopromazine, levomepromazine, thioproperazine, zuclopenthixol) als selectief – in de vorm van een effect op hallucinogeen-paranoïde stoornissen (haloperidol, trifluoperazine).
- Anti-recidief (preventieve) therapie. Hiervoor worden depotmedicijnen voorgeschreven, vooral bij patiënten met een slechte therapietrouw (haloperidoldecanoaat, verlengde vorm van flupentixol), of lage of gemiddelde doses medicijnen om een desinhiberend (anti-negatief) effect te bereiken. Hoge doses worden gebruikt voor de verlichting van acute psychotische stoornissen (flupentixol, zuclopenthixol). Bij dit type therapie wordt ook het voorschrijven van zogenaamde kleine neuroleptica (thioridazine, chloorprothixeen, sulpiride) aanbevolen, waarvan de psychotrope werking bestaat uit een effect op de manifestaties van de depressieve pool en slapeloosheid.
- Het overwinnen van therapeutische resistentie tegen atypische antipsychotica bij de behandeling van acute psychotische toestanden. Hiervoor worden meestal parenterale vormen van klassieke antipsychotica met globale (chloorpromazine, levomepromazine, enz.) en selectieve (haloperidol) antipsychotische werking gebruikt.
Deze geneesmiddelen veroorzaken verschillende bijwerkingen, waarvan de aard afhangt van de farmacologische eigenschappen van elk geneesmiddel. Antipsychotica met een meer uitgesproken cholinolytisch effect veroorzaken vaker accommodatiestoornissen, constipatie, een droge mond en urineretentie. Een sedatief effect is kenmerkender voor antipsychotica met een uitgesproken antihistaminicumeffect, en orthostatische hypotensie is kenmerkender voor geneesmiddelen die a1-adrenerge receptoren blokkeren. Blokkering van de cholinerge, nordrenerge en dopaminerge transmissie door typische neuroleptica kan leiden tot een aantal stoornissen in de seksuele sfeer, zoals amenorroe of dysmenorroe, anorgasmie, galactorroe, zwelling en pijn van de borstklieren en verminderde potentie. Bijwerkingen in de seksuele sfeer worden voornamelijk geassocieerd met de cholinolytische en adrenoblokkerende eigenschappen van deze geneesmiddelen, en ook met een toename van de prolactinesecretie als gevolg van de blokkade van het dopaminemetabolisme. De ernstigste bijwerkingen van klassieke neuroleptica zijn motorische disfunctie. Dit is de meest voorkomende reden waarom patiënten stoppen met het innemen van hun medicatie. De drie belangrijkste bijwerkingen van de therapie die verband houden met de invloed op de motorische sfeer zijn vroege extrapiramidale syndromen, tardieve dyskinesie en NMS.
Er wordt aangenomen dat extrapiramidale syndromen verband houden met blokkade van D2-receptoren in de basale ganglia. Deze omvatten dystonie, neuroleptisch parkinsonisme en acathisie. Manifestaties van acute dystonische reactie (vroege dyskinesie) omvatten plotseling optredende hyperkinesie, oculogyrische crises, contracties van de spieren van het gezicht en de romp, en opisthotonus. Deze aandoeningen zijn dosisafhankelijk en treden vaak op na 2-5 dagen behandeling met zeer krachtige neuroleptica zoals haloperidol en flufenazine. Om vroege dyskinesie te verlichten, wordt de dosis neuroleptica verlaagd en worden anticholinergica (biperideen, trihexyfenidyl) voorgeschreven. Tardieve dyskinesie betreft meestal de nekspieren en is, in tegenstelling tot acute dystonische reactie, minder gevoelig voor behandeling met anticholinergica. Neuroleptisch parkinsonisme wordt gekenmerkt door verminderde spontane motoriek, hypo- en amimie, rusttremor en rigiditeit. Het is belangrijk om deze symptomen te onderscheiden van de uiterlijk gelijkende negatieve stoornissen bij schizofrenie, die zich uiten in emotionele vervreemding, afstomping van emoties en anergie. Om deze bijwerkingen te corrigeren, zijn anticholinergica, een verlaging van de dosis van het neurolepticum of vervanging ervan door een atypisch antipsychoticum geïndiceerd. Acathisie manifesteert zich door innerlijke angst, het onvermogen om langdurig op één plaats te blijven en de behoefte om voortdurend armen of benen te bewegen. Ter verlichting hiervan worden anticholinergica en centrale bètablokkers (propranolol) gebruikt.
Late dyskinesie manifesteert zich door onwillekeurige bewegingen van een spiergroep, meestal de spieren van de tong en de mond. Klinisch worden verschillende vormen onderscheiden: dyskinesie van de spieren van de wangen, tong en mond (periodieke samentrekkingen van de kauwspieren, waardoor de indruk ontstaat van een grimas, waarbij de tong onwillekeurig uit de mond van de patiënt kan steken); tardieve dystonie en tardieve acathisie (de patiënt maakt choreoathetoïde bewegingen van het hoofd, de romp, de bovenste en onderste ledematen). Deze vorm van dyskinesie wordt voornamelijk waargenomen tijdens langdurige behandeling met klassieke neuroleptica en wordt vastgesteld bij ongeveer 15-20% van de patiënten die deze als onderhoudstherapie gebruiken. Waarschijnlijk is bij sommige patiënten het risico op het ontwikkelen van dyskinesiesymptomen verhoogd, aangezien sommige van deze symptomen al vóór het "neurolepticatijdperk" in de kliniek voor schizofrenie werden waargenomen. Daarnaast is tardieve dyskinesie beschreven bij oudere vrouwen en patiënten met stemmingsstoornissen. Tardieve dyskinesie wordt in verband gebracht met een toename van het aantal dopaminereceptoren in het striatum, hoewel GABA-erge en andere neurotransmittersystemen waarschijnlijk ook betrokken zijn bij de pathogenese ervan. Er bestaat geen effectieve universele behandeling voor dergelijke bijwerkingen. Er wordt gesuggereerd dat lage doses hoog-potente neuroleptica met dopamine-blokkerende werking of vitamine E een matig gunstig effect kunnen hebben bij deze aandoeningen. De meest effectieve maatregel voor tardieve dyskinesie is een verlaging van de dosis van een typisch neurolepticum of vervanging ervan door een atypisch antipsychoticum.
Volgens de huidige gegevens komt het maligne neurolepticasyndroom voor bij ongeveer 0,5% van de gevallen van psychofarmacotherapie. Het zeldzame voorkomen van een dergelijke levensbedreigende complicatie kan waarschijnlijk worden verklaard door de wijdverbreide invoering van atypische antipsychotica in de praktijk, aangezien het risico op het ontwikkelen van NMS tijdens behandeling met deze geneesmiddelen onbeduidend is. Algemeen wordt aangenomen dat de belangrijkste oorzaak van het ontstaan van NMS een overmatige blokkade van het dopaminerge systeem is tijdens behandeling met neuroleptica, vooral na verhoging van de dosis van een zeer krachtig antipsychoticum. De belangrijkste symptomen van NMS zijn hyperthermie, verhoogde tonus van skeletspieren en peesreflexen, verminderd bewustzijn met overgang naar coma. Bloedonderzoek toont leukocytose, verhoogde bezinkingssnelheid van erytrocyten en levertransaminaseactiviteit aan; urineonderzoek toont de aanwezigheid van albuminurie aan. Verstoringen van de water- en elektrolytenbalans treden snel op, wat de voorwaarden schept voor de vorming van hersenoedeem. NMS is een acute aandoening die een spoedopname van de patiënt vereist voor intensieve infusietherapie. Bij de behandeling van NMS zijn hydratie en symptomatische therapie het belangrijkst. In deze situatie moeten alle voorgeschreven neuroleptica onmiddellijk worden stopgezet. In sommige gevallen hebben dopaminereceptoragonisten (bijvoorbeeld bromocriptine) of spierverslappers een positief effect, hoewel de effectiviteit ervan niet is onderzocht. Na het elimineren van NMS mag het neurolepticum gedurende ten minste twee weken niet worden hervat. Vervolgens kan een laag-potent antipsychoticum worden voorgeschreven, bij voorkeur een geneesmiddel van de nieuwe generatie. De dosis van het nieuw voorgeschreven geneesmiddel moet uiterst zorgvuldig worden verhoogd, waarbij de vitale functies en laboratoriumgegevens (bloed- en urineonderzoek) in de gaten worden gehouden.
Typische neuroleptica veroorzaken zelden gevaarlijke, fatale complicaties. Overdosering hangt voornamelijk af van het individuele profiel van de anti-adrenerge en anticholinerge werking van het geneesmiddel. Omdat deze geneesmiddelen een sterk anti-emetisch effect hebben, is maagspoeling geïndiceerd voor de eliminatie ervan uit het lichaam, in plaats van toediening van emetica. Arteriële hypotensie is doorgaans een gevolg van adrenerge receptorblokkade en dient te worden gecorrigeerd door toediening van dopamine en noradrenaline. Bij hartritmestoornissen is het gebruik van lidocaïne geïndiceerd.
Werkingsmechanisme en farmacologische effecten van typische antipsychotica
Naarmate de psychofarmacologie zich ontwikkelde, werden verschillende opties voorgesteld voor het effect van antipsychotica op neuroreceptoren. De belangrijkste hypothese blijft dat ze dopamine-neurostructuren (voornamelijk D2-receptoren) beïnvloeden, gebaseerd op gegevens over de verstoring van het normale dopaminemetabolisme in hersenstructuren bij psychoses. Dopamine D2-receptoren bevinden zich in de basale ganglia, de nucleus accumbens en de frontale cortex; ze spelen een hoofdrol bij het reguleren van de informatiestroom tussen de hersenschors en de thalamus.
De afbeelding geeft een gedetailleerder beeld van de verstoringen in de dopamine-overdracht in de corticale en subcorticale gebieden van de hersenen en de rol die deze verstoringen spelen bij de ontwikkeling van schizofreniesymptomen (bewerkt naar de monografie van Jones RB, Buckley PF, 2006).
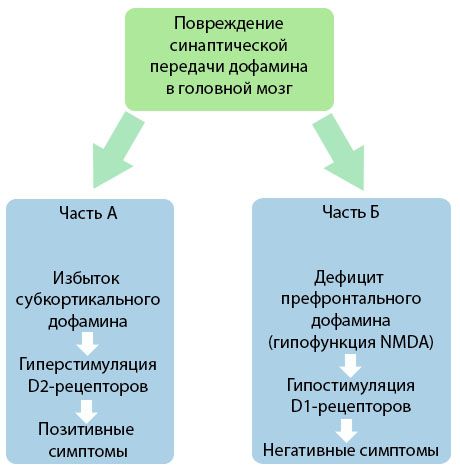
Deel A weerspiegelt de klassieke, vroege dopaminetheorie, die een teveel aan dopamine in subcorticale gebieden en hyperstimulatie van D2-receptoren postuleert, wat leidt tot het ontstaan van productieve symptomen. Deel B demonstreert de daaropvolgende modernisering van de theorie begin jaren negentig. De gegevens die toen werden verkregen, onthulden dat een tekort aan dopamine in D-receptoren, samen met onvoldoende stimulatie van deze receptoren in de prefrontale cortex, leidt tot het ontstaan van negatieve symptomen en cognitieve tekorten. Volgens de moderne kennis zijn beide soorten dopaminerge transmissiestoornissen - een teveel aan subcorticale dopamine en een tekort aan dopamine in de prefrontale cortex - daarom het gecombineerde resultaat van een verstoring van de synaptische transmissie in het prefrontale gebied en worden ze geassocieerd met een hypofunctie van N-methyl-N-aspartaat. Naast de aanvankelijk geïsoleerde dopamine werden later andere neurotransmitters geïdentificeerd die betrokken zijn bij de pathogenese van schizofrenie, zoals serotonine, gamma-aminoboterzuur, glutamaat, noradrenaline, acetylcholine en verschillende neuropeptiden. Hoewel de rol van deze mediatoren nog niet volledig is onderzocht, wordt het naarmate de kennis groeit duidelijk dat er talrijke neurochemische verschuivingen in het lichaam optreden. Het klinische effect van een antipsychoticum is dan ook een optelsom van de effecten op verschillende receptorformaties en leidt tot de eliminatie van homeostasestoornissen.
De afgelopen jaren is er, dankzij de opkomst van nieuwe onderzoeksmethoden zoals radio-isotopenligandbinding en PET-scans, aanzienlijke vooruitgang geboekt in het ontrafelen van het precieze biochemische werkingsmechanisme van neuroleptica. Met name de relatieve sterkte en tropisme van geneesmiddelen om zich te binden aan individuele neuroreceptoren in verschillende hersengebieden en -structuren zijn vastgesteld. Er is aangetoond dat de ernst van het antipsychotische effect van een geneesmiddel direct afhankelijk is van de sterkte van het blokkerende effect op verschillende dopaminerge receptoren. Recent zijn vier typen van dergelijke receptoren geïdentificeerd:
- D1 bevinden zich voornamelijk in het gebied van de substantia nigra en het striatum (de zogenaamde nigrostriatale regio), evenals in de prefrontale regio;
- D2 - in de nigrostriatale en mesolimbische regio's en de hypofysevoorkwab (afscheiding van prolactine);
- D3 (presynaptisch) - in verschillende hersenstructuren controleren ze de dopaminerge activiteit volgens de wet van negatieve feedback;
- D4 (presynaptisch) - voornamelijk in de nigrostriatale en mesolimbische gebieden.
Tegelijkertijd kan nu als bewezen worden beschouwd dat de blokkade van D2-receptoren de ontwikkeling van antipsychotische, secundair sedatieve effecten en extrapiramidale bijwerkingen veroorzaakt. Andere klinische verschijnselen van de blokkade van dit type receptoren zijn het pijnstillende en anti-emetische effect van neuroleptica (vermindering van misselijkheid en braken door onderdrukking van het braakcentrum), evenals een afname van het groeihormoongehalte en een toename van de prolactineproductie (neuro-endocriene bijwerkingen, waaronder galactorroe en menstruatieonregelmatigheden). Langdurige blokkade van nigrostriatale D2-receptoren leidt tot het optreden van overgevoeligheid, wat verantwoordelijk is voor de ontwikkeling van tardieve dyskinesieën en "overgevoeligheidspsychosen". Waarschijnlijke klinische verschijnselen van de blokkade van presynaptische D3- en D4-receptoren worden voornamelijk geassocieerd met het stimulerende effect van neuroleptica. Door de gedeeltelijke blokkade van deze receptoren in de nigrostriatale en mesolimbocorticale gebieden kunnen activerende en indringende (krachtige, zeer werkzame) neuroleptica in kleine doses de dopaminerge transmissie stimuleren en in hoge doses onderdrukken.
De laatste jaren is de belangstelling voor de werking van de serotonerge systemen in de hersenen, waaronder serotoninereceptoren, sterk toegenomen. Feit is dat het serotonerge systeem in verschillende delen van de hersenen een modulerende werking heeft op dopaminerge structuren. Met name in de mesocorticale regio remt serotonine de afgifte van dopamine, waardoor de blokkade van postsynaptische 5-HT-receptoren leidt tot een toename van het dopaminegehalte. Zoals bekend, gaat de ontwikkeling van negatieve symptomen bij schizofrenie gepaard met een hypofunctie van dopamineneuronen in de prefrontale structuren van de hersenschors. Momenteel zijn er ongeveer 15 typen centrale 5-HT-receptoren bekend. Experimenteel is ontdekt dat neuroleptica zich voornamelijk binden aan 5-HT-receptoren van de eerste drie typen.
Deze geneesmiddelen hebben voornamelijk een stimulerend (agonistisch) effect op 5-HT1a-receptoren. Waarschijnlijke klinische gevolgen: verhoogde antipsychotische activiteit, verminderde ernst van cognitieve stoornissen, correctie van negatieve symptomen, antidepressieve werking en verminderde incidentie van extrapiramidale bijwerkingen.
Het effect van neuroleptica op 5-HT2-receptoren, met name op 5-HT2a-subtypen, is van groot belang. Deze receptoren bevinden zich voornamelijk in de hersenschors en hun gevoeligheid is verhoogd bij patiënten met schizofrenie. Het vermogen van nieuwe generatie neuroleptica om de ernst van negatieve symptomen te verminderen, cognitieve functies te verbeteren, de slaap te reguleren door de totale duur van de slow-wave (D-wave) slaapfasen te verlengen, agressie te verminderen en depressieve symptomen en migraineachtige hoofdpijn (als gevolg van cerebrovasculaire aandoeningen) te verlichten, wordt geassocieerd met de blokkade van 5-HT2a-receptoren. Aan de andere kant zijn bij mannen hypotensieve effecten en ejaculatiestoornissen mogelijk bij de blokkade van 5-HT2a-receptoren.
Er wordt aangenomen dat de werking van neuroleptica op 5-HT2c-receptoren een sedatief (anxiolytisch) effect heeft, een verhoogde eetlust (gepaard gaande met een toename van het lichaamsgewicht) en een afname van de prolactineproductie.
5-HT3-receptoren bevinden zich voornamelijk in de limbische regio. Wanneer deze worden geblokkeerd, ontwikkelt zich eerst het anti-emetische effect. Ook de antipsychotische en angstremmende effecten worden versterkt.
Het optreden van parkinsonachtige symptomen hangt ook af van de blokkerende werking van het geneesmiddel op muscarine-cholinerge receptoren. Cholinolytische en dopamine-blokkerende effecten zijn tot op zekere hoogte in wederkerige relaties. Het is bijvoorbeeld bekend dat D2-receptoren in de nigrostriatale regio de afgifte van acetylcholine remmen. Wanneer meer dan 75% van de D2-receptoren in de nigrostriatale regio geblokkeerd is, wordt de balans verstoord ten gunste van het cholinerge systeem. Dit is de reden voor het corrigerende effect van anticholinergica (correctoren) op neuroleptische extrapiramidale bijwerkingen. Chloorprothixeen, clozapine en olanzapine hebben een hoge affiniteit voor muscarinereceptoren en veroorzaken praktisch geen extrapiramidale bijwerkingen, omdat ze cholinerge en dopaminerge receptoren gelijktijdig blokkeren. Haloperidol en piperazinefenothiazinederivaten hebben een uitgesproken effect op dopaminereceptoren, maar een zeer zwak effect op cholinereceptoren. Dit komt doordat ze sterke extrapiramidale bijwerkingen kunnen veroorzaken, die afnemen bij gebruik van zeer hoge doses, wanneer het cholinolytische effect merkbaar wordt. Naast het verminderen van het dopamineblokkerende effect op D2-receptoren in de nigrostriatale regio en het nivelleren van extrapiramidale bijwerkingen, kan een sterk cholinerge werking leiden tot een verslechtering van cognitieve functies, waaronder geheugenstoornissen, evenals perifere bijwerkingen (droge slijmvliezen, verminderde visuele accommodatie, constipatie, urineretentie, verwardheid, enz.). Neuroleptica hebben een vrij sterk blokkerend effect op histaminereceptoren type I, wat allereerst gepaard gaat met de ernst van het sedatieve effect, evenals een toename van het lichaamsgewicht door een toegenomen eetlust. De antiallergische en jeukwerende effecten van neuroleptica gaan ook gepaard met hun antihistaminische eigenschappen.
Naast dopamineblokkerende, antiserotonerge, cholinolytische en antihistaminische effecten hebben de meeste neuroleptica adrenolytische eigenschappen, d.w.z. ze blokkeren zowel centrale als perifere a1-adrenoreceptoren. Adrenoblokkers zoals chloorpromazine en chloorprothixeen hebben een uitgesproken sedatieve werking. Bovendien kan de blokkerende werking van deze geneesmiddelen neurovegetatieve bijwerkingen veroorzaken (arteriële hypotensie, tachycardie, enz.), evenals een versterking van het hypotensieve effect van adrenoblokkers.
Uit de werken van een groot aantal auteurs zijn gegevens naar voren gekomen over de bindingssterkte (affiniteit) van individuele neuroleptica met verschillende typen neuroreceptoren.
Op basis van hun neurochemische werkingsprofiel kunnen de typische en atypische antipsychotica, die het meest in de klinische praktijk worden gebruikt, voorwaardelijk worden onderverdeeld in zes groepen.
De eerste groep bestaat uit selectieve blokkers van D2- en D4-receptoren (sulpiride, amisudpride, haloperidol, enz.) uit de groep van benzamide- en butyrofenonderivaten. In lage doses activeren ze, voornamelijk door blokkade van presynaptische D4-receptoren, de dopaminerge transmissie van zenuwimpulsen en hebben ze een stimulerend (ontremmend) effect. In hoge doses blokkeren ze D2-receptoren in alle hersengebieden, wat zich klinisch manifesteert door een uitgesproken antipsychotisch effect, evenals extrapiramidale en endocriene (als gevolg van prolactinemie) bijwerkingen.
De tweede groep omvat zeer actieve D2-receptorblokkers, evenals geneesmiddelen die 5-HT2a- en 5-HT1a-receptoren zwak of matig blokkeren (flupentixol, flufenazine, zuclopenthixol, enz.), d.w.z. voornamelijk piperazinederivaten van fenothiazine of thioxanthenen die qua stereochemische structuur daaraan verwant zijn. Net als de geneesmiddelen uit de eerste groep hebben deze neuroleptica allereerst een uitgesproken antipsychotisch (incisief) effect en veroorzaken ze ook extrapiramidale pye-effecten en prolactinemie. In lage doses hebben ze een matig activerend (psychostimulerend) effect.
De derde groep bestaat uit polyvalente sedatieve neuroleptica die de meeste neuroreceptoren op ongedifferentieerde wijze blokkeren. Deze geneesmiddelen hebben een duidelijk blokkerend effect op dopaminereceptoren en veroorzaken ook sterke adrenolytische en cholinolytische effecten. Dit omvat de meeste sedatieve neuroleptica, voornamelijk alifatische en piperidinederivaten van fenothiazine, evenals thioxanthenen die qua stereochemische structuur nauw verwant zijn (chloorpromazine, levomepromazine, chloorprothixeen, enz.). Het psychotrope werkingsspectrum van deze geneesmiddelen wordt in de eerste plaats gedomineerd door een uitgesproken primair sedatief effect, dat zich ongeacht de gebruikte dosis ontwikkelt, en een matig antipsychotisch effect. Bovendien veroorzaken geneesmiddelen uit deze groep, vanwege hun uitgesproken anticholinerge werking, zwakke of matige extrapiramidale en neuro-endocriene bijwerkingen, maar leiden ze vaak tot de ontwikkeling van orthostatische hypotensie en andere autonome reacties als gevolg van een uitgesproken blokkade van a1-adrenerge receptoren.
De vierde groep omvat neuroleptica die D2- en 5-HT2a-receptoren op evenwichtige wijze blokkeren, d.w.z. in dezelfde mate (de laatste in iets sterkere mate) en a1-adrenoreceptoren in matige mate. Deze groep omvat vertegenwoordigers van de nieuwe generatie atypische antipsychotica (risperidon, ziprasidon, sertindol), die verschillende chemische structuren hebben. Het neurochemische werkingsmechanisme bepaalt hun selectieve invloed voornamelijk op de mesolimbische en mesocorticale hersengebieden. Naast een uitgesproken antipsychotisch effect, de afwezigheid of zwakke expressie van extrapiramidale bijwerkingen (bij gebruik van therapeutische doses), een zwakke of matige prolactinemie en matige adrenolytische eigenschappen (hypotensieve reacties), is deze groep neuroleptica in staat negatieve symptomen te corrigeren door indirecte stimulatie van de dopaminerge transmissie in de hersenschors.
De vijfde groep bestaat uit polyvalente atypische antipsychotica met tricyclische dibenzodiazepine of een vergelijkbare structuur (clozapine, olanzapine en quetiapine). Net als de geneesmiddelen uit de derde groep blokkeren ze de meeste neuroreceptoren op ongedifferentieerde wijze. 5-HT2a-receptoren worden echter sterker geblokkeerd dan D2- en D4-receptoren, met name die in de nigrostriatale regio. Dit bepaalt de daadwerkelijke afwezigheid of het zwakke extrapiramidale effect en de afwezigheid van neuro-endocriene bijwerkingen die gepaard gaan met een verhoogde prolactineproductie met een uitgesproken antipsychotisch effect, en het vermogen om de ernst van negatieve symptomen te verminderen. Bovendien hebben alle geneesmiddelen uit deze groep uitgesproken adrenolytische en antihistaminische eigenschappen, wat de sedatieve en hypotensieve effecten bepaalt. Clozapine en olanzapine hebben ook een vrij uitgesproken blokkerende werking op muscarinereceptoren en leiden tot de ontwikkeling van cholinolytische bijwerkingen.
Het vermogen om postsynaptische dopaminerge receptoren te blokkeren met een compenserende toename in de synthese en het metabolisme van dopamine is dus de enige gemeenschappelijke biochemische eigenschap van alle neuroleptica die in deze groepen worden beschouwd.
De zesde groep omvat het enige atypische antipsychoticum, aripiprazol, dat relatief recent op de binnenlandse markt voor psychofarmaceutica is verschenen. Dit geneesmiddel is een partiële agonist van D2-dopaminereceptoren en werkt als een functionele antagonist in een hyperdopaminerge toestand en als een functionele agonist in een hypodopaminerge toestand. Een dergelijk uniek receptorprofiel van aripiprazol maakt het mogelijk om het risico op extrapiramidale stoornissen en hyperprolactinemie te verminderen tijdens het gebruik ervan. Bovendien werkt aripiprazol als een partiële agonist van 5-HT1a-receptoren en tegelijkertijd als een antagonist van 5-HT2a-receptoren. Aangenomen wordt dat een dergelijke interactie met receptoren leidt tot een over het algemeen evenwichtige werking van de serotonine- en dopaminesystemen, waardoor het werkingsmechanisme van aripiprazol kan worden aangemerkt als stabiliserend voor het dopamine-serotoninesysteem.
De huidige kennis over de neurochemische werkingsmechanismen van neuroleptica stelt ons in staat een nieuwe, pathogenetisch beter onderbouwde farmacodynamische classificatie van deze groep psychotrope geneesmiddelen voor te stellen. Het gebruik van deze classificatie stelt ons in staat om in hoge mate het spectrum van psychotrope activiteit, tolerantie en waarschijnlijke geneesmiddelinteracties van een bepaald geneesmiddel te voorspellen. Met andere woorden, de kenmerken van de neurochemische activiteit van een geneesmiddel bepalen grotendeels de kenmerken van de klinische activiteit, die van belang zijn bij de keuze van een bepaald antipsychoticum voor een specifieke patiënt.
De effectiviteit van het globale antipsychotische effect van een neurolepticum wordt geschat met behulp van het zogenaamde chloorpromazine-equivalent, dat als 1 wordt genomen. Bijvoorbeeld, het chloorpromazine-equivalent van haloperidol = 50. Dit betekent dat de antipsychotische effectiviteit van 1 mg haloperidol vergelijkbaar is met die van 50 mg chloorpromazine. Op basis van deze indicator is een classificatie ontwikkeld die voorziet in de indeling van neuroleptica met een hoge (chloorpromazine-equivalent > 10,0), gemiddelde (chloorpromazine-equivalent = 1,0-10,0) en lage (chloorpromazine-equivalent = 1,0) antipsychotische activiteit, ook wel patentiteit genoemd. Typische neuroleptica (antipsychotica van de eerste generatie) worden al bijna een halve eeuw veelvuldig gebruikt in de klinische psychofarmacotherapie. Het spectrum van hun therapeutische activiteit omvat:
- globale antipsychotische werking in de vorm van het vermogen om verschillende verschijnselen van psychose gelijkmatig en gedifferentieerd te verminderen:
- primair sedatief (remmend) effect - het vermogen van geneesmiddelen om psychomotorische agitatie snel te verlichten;
- selectieve, selectieve antipsychotische werking, die zich uit in het vermogen om individuele symptomen te beïnvloeden: delirium, hallucinaties, ontremming van driften, enz.;
- activerende (ontremmende, ontremmende, anti-autistische) neurotrope werking, gemanifesteerd door de ontwikkeling van extrapiramidale symptomen;
- somatotrope werking in de vorm van ontwikkeling van neuro-endocriene en vegetatieve bijwerkingen;
- Verdovende werking, uitgedrukt in het vermogen van sommige antipsychotica om depressieve symptomen te veroorzaken.
De effectiviteit van antipsychotica van de eerste generatie bij de behandeling van niet alleen psychotische stoornissen, maar ook bij stoornissen binnen de borderlinepsychiatrie, is veelvuldig bewezen en staat buiten kijf. Ondanks de hoge frequentie van bijwerkingen bij het voorschrijven ervan, worden ze nog steeds in de medische praktijk gebruikt.
Atypische antipsychotica
Moderne richtlijnen bevatten gegevens over de voordelen van het gebruik van tweedegeneratie-antipsychotica in de farmacotherapie. De term "atypisch" (synoniem - tweedegeneratie-antipsychotica) is voorwaardelijk en wordt voornamelijk gebruikt om de nieuwe generatie aan te duiden. Vergeleken met traditionele neuroleptica zijn geneesmiddelen uit deze groep effectiever in het corrigeren van negatieve, affectieve en cognitieve stoornissen, wat gepaard gaat met een betere verdraagbaarheid en een lager risico op extrapiramidale symptomen. Verschillen in de aard van het therapeutische effect van het ene of het andere geneesmiddel uit een reeks atypische antipsychotica worden, net als bij de groep typische neuroleptica, verklaard door het individuele farmacologische werkingsprofiel.
Om de mogelijkheden van psychofarmacotherapie met atypische antipsychotica te verduidelijken, is het raadzaam om ons te richten op de geneesmiddelen van deze groep die in Rusland zijn geregistreerd.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Clozapine (dibenzodiazepine)
De grondlegger van de groep atypische antipsychotica. Het werkingsmechanisme van clozapine wordt gekenmerkt door een lichte blokkade van D2-receptoren met gelijktijdige sterke antagonisme tegen 5-HT2a-receptoren, a1-, a2-adrenerge en H1-histaminereceptoren. Het heeft zich bewezen als een effectief antipsychoticum bij resistentie tegen andere antipsychotica (een middel uit de reservegroep) en is ook geïndiceerd voor de behandeling van chronische manie, psychotische agitatie en agressie. In de thuispraktijk wordt clozapine vaak voorgeschreven om sedatie te bereiken en als hypnoticum bij psychotische patiënten. Erkend moet worden dat een dergelijk gebruik van clozapine niet overeenkomt met het hoofdprofiel van de indicaties voor gebruik in therapie. Waarschijnlijk moet de houding ten opzichte van dit antipsychoticum als secundair geneesmiddel worden herzien, aangezien het vandaag de dag het enige geneesmiddel is met bewezen effectiviteit bij resistente patiënten.
Clozapine veroorzaakt, in tegenstelling tot klassieke neuroleptica, geen ernstige extrapiramidale stoornissen vanwege de eerder genoemde lage affiniteit voor O2-receptoren. Het is ook gebleken dat het gebruikt kan worden voor de behandeling van late dystonie en ernstige acathisie. Vanwege het lage risico op het ontwikkelen van NMS kan clozapine worden beschouwd als een middel van eerste keuze bij patiënten die eerder aan deze complicatie hebben geleden.
Er kunnen echter een aantal ernstige bijwerkingen optreden tijdens de behandeling met clozapine. De gevaarlijkste daarvan (zelfs bij het voorschrijven van kleine doses) is agranulocytose, die voorkomt bij 0,5-1,0% van de patiënten. Andere belangrijke bijwerkingen die kunnen optreden bij het gebruik van het geneesmiddel zijn slaperigheid, hypersalivatie en gewichtstoename, die vaak al verhoogd zijn tegen de tijd dat clozapine wordt voorgeschreven onder invloed van eerdere antipsychotische therapie. Er moet ook rekening worden gehouden met de mogelijkheid van het ontwikkelen van tachycardie, arteriële hypotensie en epileptische aanvallen tijdens het gebruik ervan. De kans op aanvallen is afhankelijk van de dosis. Het risico hierop neemt aanzienlijk toe als de dosis clozapine hoger is dan 600 mg/dag. Het ontwikkelen van aanvallen is geen contra-indicatie voor verder gebruik van het geneesmiddel, maar vereist een halvering van de dosis en het voorschrijven van anti-epileptica, zoals valproïnezuur. Preventie van bijwerkingen van clozapinebehandeling omvat zorgvuldige monitoring van het aantal witte bloedcellen, evenals ECG en endocriene parameters.
Overdosering met clozapine kan leiden tot bewustzijnsverlies en zelfs coma, evenals symptomen die verband houden met het cholinolytische effect (tachycardie, delirium), epileptische aanvallen, ademhalingsdepressie en extrapiramidale syndromen. Een fatale afloop kan optreden bij inname van meer dan 2500 mg van het geneesmiddel.
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
Risperidon
Een benzisoxazoolderivaat met een hoge affiniteit voor serotonine- en dopamine-Dj-receptoren, met een dominant effect op het serotoninesysteem. Het geneesmiddel heeft een breed scala aan indicaties, waaronder verlichting van exacerbaties, anti-recidiefbehandeling, behandeling van de eerste psychotische episode en correctie van negatieve symptomen van schizofrenie. Het geneesmiddel is aangetoond het cognitief functioneren bij patiënten met schizofrenie te verbeteren. Voorlopige gegevens tonen aan dat risperidon ook comorbide affectieve symptomen bij patiënten met schizofrenie vermindert en mogelijk een voorkeursgeneesmiddel is bij de behandeling van bipolaire affectieve stoornissen.
Bijwerkingen van risperidontherapie, met name extrapiramidale stoornissen, zijn dosisafhankelijk en treden vaker op bij doses hoger dan 6 mg/dag. Andere bijwerkingen zijn misselijkheid, braken, angst, slaperigheid en verhoogde serumprolactinespiegels. Langdurig gebruik van risperidon kan leiden tot gewichtstoename en de ontwikkeling van diabetes mellitus type 2, maar met een lagere kans dan bij clozapine en olanzapine.
Overdosering kan slaperigheid, epileptische aanvallen, verlenging van het QT-interval en verbreding van het QRS-complex, en arteriële hypotensie veroorzaken. Er zijn gevallen met fatale afloop beschreven als gevolg van een overdosis risperidon.
Het onbetwiste voordeel van het medicijn is de beschikbaarheid van vloeibare en snel oplosbare (sublinguale) vormen, waarvan het gebruik de opname van het medicijn in het lichaam van de patiënt versnelt en de controle over de inname vergemakkelijkt. Er bestaat ook een verlengde vorm van het medicijn: poeder voor de bereiding van een suspensie voor intramusculaire toediening (consta-risperidon in microsferen). Het wordt aanbevolen voor onderhoudsbehandeling van patiënten met schizofrenie, met name voor patiënten met een slechte therapietrouw. Er moet rekening mee worden gehouden dat het medicijn ongeveer drie weken nodig heeft om in de bloedbaan te komen. Daarom moet de patiënt bij aanvang van de behandeling met consta-risperidon gedurende ten minste drie weken na de eerste injectie ook de orale vorm van risperidon gebruiken.
Olanzapine
Qua farmacologische werking is het vergelijkbaar met clozapine, aangezien het een pleiomorf receptorprofiel heeft met een significante affiniteit voor serotonine-, muscarine-, α1-adrenerge en histaminereceptoren. De therapeutische activiteit van olanzapine vertoont vergelijkbare kenmerken als die van clozapine en risperidon wat betreft de impact op positieve, negatieve en depressieve symptomen van schizofrenie. Tegelijkertijd zijn er gegevens verkregen over de grotere effectiviteit van olanzapine in vergelijking met andere atypische antipsychotica bij patiënten met de eerste psychotische episode en bij de correctie van cognitieve functie-indicatoren. Er moet rekening mee worden gehouden dat aan het begin van de behandeling met de tabletvorm van het geneesmiddel een snel desinhiberend effect kan optreden met verhoogde psychomotorische agitatie en angst. Daarom is het gebruik van de injectievorm van het geneesmiddel geïndiceerd bij de behandeling van aanvallen die gepaard gaan met ernstige psychomotorische agitatie.
Olanzapine veroorzaakt zelden extrapiramidale stoornissen of tardieve dyskinesie; de meest voorkomende bijwerkingen zijn stofwisselingsstoornissen en gewichtstoename. Het is vastgesteld dat patiënten die olanzapine gebruiken vrij vaak verhoogde cholesterol- en plasmalipidenwaarden en een aanleg voor diabetes type 2 ervaren, maar dergelijke effecten kwamen even vaak voor bij patiënten die zowel olanzapine als clozapine kregen. Tegelijkertijd zijn er gegevens verzameld waaruit blijkt dat gewichtstoename correleert met een positieve respons op olanzapine (d.w.z. dient als een belangrijke prognostische indicator voor de behandeling) en zich slechts bij 20-30% van de patiënten die tijdens de behandeling overgewicht hebben gekregen, ontwikkelt tot obesitas.
Overdosering kan sedatie, toxische anticholinerge effecten, epileptische aanvallen en arteriële hypotensie veroorzaken. Er zijn momenteel geen overtuigende gegevens om het risico op overlijden door overdosering te beoordelen.
Quetiapine
Het is geclassificeerd als een dibenzothiazepine. Het receptorprofiel ervan is grotendeels vergelijkbaar met dat van clozapine. De binding van quetiapine aan D2-receptoren is laag (minder dan 50%) en van korte duur, zelfs bij hoge doses. Het geneesmiddel is effectief bij de behandeling van positieve, negatieve en algemene symptomen van schizofrenie. Er zijn aanwijzingen voor succesvol gebruik ervan, zowel bij hoge therapieresistentie als voor het verbeteren van het cognitief functioneren van patiënten, wat het recht geeft om het aan te bevelen als eerstelijns antipsychoticum voor onderhoudstherapie van schizofrenie. Ten slotte heeft quetiapine een matige antidepressieve, activerende werking. Daarom is het geïndiceerd voor de behandeling van depressieve waanaanvallen en stoornissen van de senesto-hypochondrische cirkel.
De bewezen hoge thymotrope werking van quetiapine verklaart waarom het geregistreerd is als middel voor de verlichting en secundaire preventie van depressieve stoornissen. Voor de behandeling van manische episodes binnen bipolaire stoornissen type I en II wordt quetiapine als aanvullend middel gebruikt. Het ontbreken van injectievormen beperkt het gebruik ervan bij patiënten met agitatie en agressief gedrag.
Quetiapine wordt goed verdragen en veroorzaakt praktisch geen extrapiramidale syndromen, behalve in gevallen waarin de maximale dosering wordt gebruikt. Quetiapine veroorzaakt geen hyperprolactinemie, maar leidt, minder vaak dan olanzapine en clozapine, tot gewichtstoename en een verminderde glucosetolerantie.
Ziprasidon
Heeft een uniek profiel van receptoractiviteit. Als krachtige antagonist van 5HT2a-receptoren en D2-receptoren is het ook een actieve remmer van de heropname van serotonine en noradrenaline. Klinische studies hebben aangetoond dat ziprasidon significant beter werkt op psychotische symptomen en agressie-uitingen dan haloperidol. Er zijn ook gegevens over het positieve effect van ziprasidon op de cognitieve functies van patiënten met schizofrenie, evenals op comorbide affectieve symptomen en indicatoren van sociaal functioneren. Ziprasidon wordt doorgaans goed verdragen en veroorzaakt zeer zelden extrapiramidale syndromen, gewichtstoename en stofwisselingsstoornissen. Vaker treedt er een verlenging van het QT-interval op van meer dan 460 ms. Daarom is het raadzaam dat patiënten die dit geneesmiddel krijgen, zowel vóór het voorschrijven van het geneesmiddel als tijdens de behandeling een ECG-onderzoek ondergaan. Bijzondere aandacht moet worden besteed aan gelijktijdige therapie (het nemen van anti-aritmica), die de verlenging van het QT-interval kan verergeren en kan leiden tot de ontwikkeling van hartritmestoornissen en ventrikelfibrilleren.
Sertindol
Behoort tot de derivaten van fenylindol. Het heeft een hoog functioneel antagonisme ten opzichte van D2-, serotonine- (met name 5-HT2a-) en a1-adrenerge receptoren. Volgens elektroneurochemische studies remt sertindol selectief dopaminereceptoren in de ventrale segmentale regio. Deze selectiviteit zorgt naar alle waarschijnlijkheid voor een laag risico op extrapiramidale syndromen en hyperprolactinemie bij gebruik van het geneesmiddel. De resultaten van vergelijkende studies hebben aangetoond dat sertindol qua antipsychotische activiteit vergelijkbaar is met haloperidol. Het geneesmiddel heeft een uitgesproken ontremmend effect bij patiënten met negatieve en depressieve symptomen, dat superieur is aan een vergelijkbaar effect van rispolept. Er zijn ook aanwijzingen dat sertindol effectief is bij de correctie van cognitieve stoornissen bij patiënten met schizofrenie. Sertindol wordt over het algemeen goed verdragen door patiënten, veroorzaakt zelden sedatie en wordt daarom aanbevolen als vervangend geneesmiddel wanneer er bijwerkingen optreden tijdens de behandeling met andere moderne antipsychotica.
Ernstige bijwerkingen zijn onder meer het vermogen van het geneesmiddel om het QT-interval te verlengen, wat kan leiden tot hartritmestoornissen. Analyse van postmarketingstudies toonde aan dat het hartprofiel van sertindol niet verschilt van dat van andere nieuwe-generatie antipsychotica.
Aripiprazol
Het heeft een antipsychotische werking die vergelijkbaar is met die van andere atypische middelen, maar heeft een sterker effect op de cognitieve functies van patiënten met schizofrenie. De bovengenoemde unieke farmacologische werking van het geneesmiddel – een partiële agonist van D2-receptoren – maakt het mogelijk het risico op extrapiramidale syndromen en hyperprolactinemie te verminderen.
 [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
[ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
Amisulpride
Behoort tot de klasse van gesubstitueerde benzamiden. Het geneesmiddel bindt selectief aan de subtypen van dopaminerge receptoren D2 en D3, maar heeft geen affiniteit voor de subtypen D1, D4 en D5, en ook niet voor serotonine-, H1-histamine-, a1-adrenerge en cholinerge receptoren. Bij gebruik in hoge doses blokkeert het postsynaptische D2-receptoren. Bij lage doses manifesteert het ontremmende effect zich door blokkering van presynaptische D2- en D3-receptoren, waardoor het ook effectief is bij de behandeling van negatieve symptomen, hoewel het geen gecombineerde antagonist is van D2- en serotoninereceptoren. De resultaten van een aantal onderzoeken wijzen op een uitgesproken antipsychotische werking van het geneesmiddel bij gebruik in hoge doses, die superieur is aan die van traditionele geneesmiddelen.
 [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
[ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
Bijwerkingen van antipsychotische therapie
In de tabel staan de belangrijkste bijwerkingen van atypische antipsychotische therapie vermeld.
Voorbereiding |
Extrapiramidale |
Geleidingsstoornis op ECG |
Stofwisselingsstoornissen (gewichtstoename, verhoogde glucose-, cholesterol- en triglyceridenspiegels in het bloed) |
||
Clozapine |
. |
++ |
++ |
++- |
|
Risperidon |
++ |
+/- |
++ |
+/- |
|
Olanzapine |
+ |
+/- |
+++ |
++ |
+++ |
Quetiapine |
+/- |
+ |
+/- |
--- |
|
Ziprasidon |
+ |
++ |
+/- |
+/- |
+/- |
Sertindol |
++ |
-- |
+/- |
-- |
|
Ariliprazol |
-- |
--- |
+/- |
-- |
-- |
Amisulpride |
++ |
+/- |
|||
Let op. Ernst van de bijwerkingen: "+++" - hoog; "++" - gemiddeld; "+" - laag; "+/-" - twijfelachtig; "-" - afwezig.
Extrapiramidale syndromen
Een van de belangrijkste kenmerken van atypische antipsychotica, in tegenstelling tot traditionele middelen, is hun geringe vermogen om extrapiramidale syndromen te veroorzaken, wat een doorbraak betekende in de onderhoudsfarmacotherapie van schizofrenie. Zoals blijkt uit de gegevens in de tabel, kunnen dergelijke symptomen echter optreden bij gebruik van afzonderlijke geneesmiddelen uit deze serie (risperidon, amisulpride), wat speciale aandacht vereist bij het voorschrijven ervan.
 [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
ECG-afwijkingen
De kans op cardiale bijwerkingen vormt een ernstig probleem bij het gebruik van sommige moderne antipsychotica. In deze gevallen gaat het om verlenging van het QT-interval, wat kan leiden tot het ontstaan van aritmie. Geleidingsstoornissen, met name verlenging van het QT-interval, worden het vaakst waargenomen tijdens behandeling met clozapine, sertindol en ziprasidon. Gelijktijdige aandoeningen zoals bradycardie, atrioventriculair blok en hypothyreoïdie kunnen bijdragen aan het optreden van deze complicatie tijdens behandeling met de bovengenoemde geneesmiddelen. Momenteel wordt ECG-monitoring ongeveer eens per drie maanden aanbevolen bij patiënten die een onderhoudsbehandeling met atypische antipsychotica ondergaan.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Endocriene aandoeningen
De grootste zorg bestaat momenteel uit het vermogen van atypische antipsychotica om gewichtstoename te veroorzaken. Een verhoogd lichaamsgewicht, verhoogde glucose- en triglyceridenwaarden in het bloed kunnen leiden tot stofwisselingsstoornissen en de ontwikkeling van diabetes type 2. Bijzondere voorzichtigheid en wekelijkse controle van biochemische parameters zijn noodzakelijk tijdens de behandeling met clozapine en olanzapine. Volgens J. Geddes et al. (2000), PB Jones, PF Buckley (2006), dient het als gepast te worden beschouwd om patiënten grondig te onderzoeken alvorens hen een bepaald antipsychoticum van de moderne generatie voor te schrijven, aangezien bekend is dat stofwisselingsstoornissen vaker voorkomen bij patiënten met een erfelijke aanleg, overgewicht, lipidenspectrumstoornissen en hyperglykemie vóór aanvang van de behandeling. Het monitoringalgoritme voorgesteld door PB Jones, PF Buckley (2006) omvat verschillende punten.
- Verzamelen van medische geschiedenis en familiefactoren met betrekking tot het risico op stofwisselingsstoornissen.
- Registratie van de Body Mass Index, ECG, bloeddruk en pols vóór aanvang van de behandeling.
- Verzamelen van laboratoriumgegevens (glucose, lipidenprofiel, cholesterol) vóór aanvang van de therapie.
- Regelmatige controle van de Body Mass Index en de vitale functies tijdens de behandeling.
- Controle van laboratoriumgegevens tijdens de behandeling.
Hyperprolactinemie tijdens antipsychotische therapie wordt veroorzaakt door centrale blokkade van dopaminereceptoren in de hypothalamus, wat leidt tot de afgifte van prolactine uit de hypofyse. Hyperprolactinemie treedt het vaakst op bij behandeling met olanzapine, risperidon en amisulpride.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Agranulocytose
Een andere ernstige complicatie van antipsychotische therapie. Deze kan worden waargenomen tijdens behandeling met clozapine en olanzapine. Volgens J. Geddes et al. (2000) werd deze bij 1-2% van de patiënten die deze geneesmiddelen gebruikten, vastgesteld in de eerste 3 maanden. In dit verband worden wekelijkse bloedonderzoeken aanbevolen voor patiënten die deze geneesmiddelen gebruiken gedurende de eerste 18 weken van de behandeling en maandelijkse controle daarna. Het is aangetoond dat wanneer de dosis van de bovengenoemde neuroleptica wordt verlaagd, de klinische bloedwaarden weer normaal worden. Tegelijkertijd moet worden erkend dat er tot op heden geen duidelijke strategie is voor patiënten die de bovengenoemde bijwerkingen ervaren die gepaard gaan met stofwisselingsstoornissen. Meestal wordt één atypisch antipsychoticum vervangen door een ander. Een andere veelbelovende richting is het voorschrijven van speciale corrigerende therapie, met name het gebruik van bromocriptine om hyperprolactinemie te corrigeren. In het ideale geval wordt de patiënt met dergelijke aandoeningen verzorgd met periodieke betrokkenheid van internisten, met name endocrinologen, cardiologen en andere specialisten.
Concluderend kan worden opgemerkt dat, als de gegeven algoritmen voor het voorschrijven en monitoren van niet alleen de mentale maar ook de fysieke toestand van de patiënt worden gevolgd, het gebruik van geneesmiddelen van de tweede generatie veiliger is dan typische neuroleptica.
Een aantal andere antipsychotica bevindt zich momenteel in de ontwikkelingsfase. Geneesmiddelen van de volgende generatie zullen waarschijnlijk een ander werkingsmechanisme hebben (bijvoorbeeld een GABA-erge profiel) en verschillende manifestaties van schizofrenie kunnen beïnvloeden, waaronder deficiëntiestoornissen.
Aandacht!
Om de perceptie van informatie te vereenvoudigen, werd deze instructie voor het gebruik van het medicijn "Neuroleptica of antipsychotica " vertaald en gepresenteerd in een speciale vorm op basis van de officiële instructies voor medisch gebruik van het medicijn. Lees vóór gebruik de annotatie die rechtstreeks naar de medicatie is gekomen.
Beschrijving verstrekt voor informatieve doeleinden en is geen handleiding voor zelfgenezing. De behoefte aan dit medicijn, het doel van het behandelingsregime, de methoden en dosering van het medicijn wordt uitsluitend bepaald door de behandelende arts. Zelfmedicatie is gevaarlijk voor je gezondheid.

