Medisch expert van het artikel
Nieuwe publicaties
T-cel lymfoom: perifeer, angioimmunoblastisch, non-Hodgkin, anaplastisch lymfoom
Laatst beoordeeld: 04.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
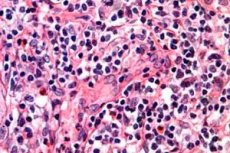
Kanker wordt beschouwd als een van de gevaarlijkste menselijke ziekten. En als je dan ook nog bedenkt dat verschillende dodelijke ziekten die het leven van veel mensen hebben bekort, schuilgaan achter een vreselijke diagnose, dan zul je onvermijdelijk geïnteresseerd raken in dit onderwerp om een soortgelijk lot te voorkomen. Neem bijvoorbeeld een van de gevaarlijkste vormen van bloedkanker, die het lymfestelsel en de huid aantast: T-cellymfoom. Door deze aandoening overleven veel ouderen hun langverwachte pensioen niet of genieten ze er maar kort van. Hoewel, eerlijk gezegd, niet alleen ouderen tot de risicogroep voor het ontwikkelen van deze aandoening zouden moeten behoren.
Epidemiologie
Wat de statistieken van lymfomen betreft, neemt T-cellymfoom een prominente plaats in onder de kankerachtige bloedpathologieën die op oudere leeftijd worden waargenomen. Het kan echter nauwelijks een ziekte van ouderen worden genoemd, aangezien er herhaaldelijk gevallen van de ziekte zijn geregistreerd, zelfs bij kinderen en adolescenten. Tegelijkertijd zijn mannen vatbaarder voor de ziekte dan vrouwen.
Het epidermotrope karakter van de pathologie suggereert dat de ziekte zich voornamelijk in de huid, orgaanmembranen en nabijgelegen lymfeklieren bevindt. De meest voorkomende vorm van de ziekte wordt beschouwd als T-cellymfoom van de huid, en met name fungoïde mycose.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
Oorzaken T-cel lymfoom
Lymfoom is een tumor die bestaat uit gemodificeerde cellen van het lymfestelsel. Bij T-cellymfoom zijn T-cellen (T-lymfocyten) betrokken bij het pathologische proces. Deze ontwikkelen zich in de thymus uit prethymocyten, die zich in het rode beenmerg bevinden en van daaruit naar de thymus migreren.
T-lymfocyten spelen een rol bij de immuunrespons van het lichaam op verschillende externe invloeden en reguleren de processen die zich daarbinnen afspelen. Elk ontstekingsproces in het lichaam veroorzaakt een herverdeling van T-lymfocyten, die zich in de buurt van de laesie langs de lymfestroom ophopen. Nadat de ontsteking is gestopt, krijgen de lymfeklieren hun oorspronkelijke grootte en elasticiteit terug. Helaas gebeurt dit niet altijd.
Wetenschappers zijn nog niet klaar om een volledig antwoord te geven op de vraag wat de ongecontroleerde ophoping van lymfocyten op één punt zonder duidelijke reden veroorzaakt, en wat de mutatie van lymfestelselcellen veroorzaakt, die zich intensief gaan delen (prolifereren), wat leidt tot ongewenste weefselgroei in het lichaam. Ongecontroleerde celproliferatie leidt tot een toename van de lymfeklieren en organen, die worden aangevoerd door de gemuteerde T-lymfocyten. Dit alles veroorzaakt gevaarlijke verstoringen in de werking van organen en klieren, met de dood van de patiënt tot gevolg.
De meeste wetenschappers zijn geneigd te geloven dat T-cellymfoom een gevolg is van een niet nader omschreven leukemie. Leukemie wordt gekenmerkt door de vorming van gemodificeerde cellen, gevormd uit onrijpe hemocytoblasten in het beenmerg, de voorlopercellen van bloedcellen. Bij T-celleukemie worden mutaties waargenomen in lymfoblasten en prothymocyten, de voorlopercellen van T-lymfocyten.
Dergelijke kwaadaardige klonen uit het rode beenmerg kunnen ook de thymus binnendringen en van daaruit, in de vorm van gemuteerde T-lymfocyten die vatbaar zijn voor ongecontroleerde proliferatie, in het lymfestelsel terechtkomen. T-celleukemie type 1 (ook bekend als HTLV 1 – Humaan T-lymfotroop virus 1), dat behoort tot de familie van retrovirussen, is dan ook de meest waarschijnlijke oorzaak van de ontwikkeling van T-cellymfoom.
Deze theorie verklaart echter niet de maligniteit van volwassen T-lymfocyten, die aanvankelijk niet pathogeen waren. Het blijkt dat ze de negatieve invloed ondervonden van andere factoren dan het HTLV-1-virus, wat leidde tot mutaties.
Een van de theorieën over het ontstaan van T-cellymfoom is de hypothese van de negatieve impact van bepaalde virussen (bijvoorbeeld herpesvirussen type 6 en type 4, hepatitisvirus en hiv) op de kwaliteit van lymfocyten. Deze virussen worden vaak aangetroffen bij patiënten met bloedkanker, waardoor hun invloed niet kan worden uitgesloten.
Omdat de productie van T-lymfocyten wordt aangestuurd door het immuunsysteem, kan elke afwijking in de werking ervan leiden tot een verhoogde productie van T-lymfocyten uit beenmergcellen die niet rijpen en een grotere kans op chromosomale mutaties in deze cellen. Een inadequate reactie van het immuunsysteem op irriterende stoffen kan zich ook uiten in de vorm van een ophoping van snel delende lymfocytklonen in de epitheellagen van de huid, wat leidt tot de vorming van microabcessen, zoals waargenomen bij T-cellymfoom van de huid.
Tegelijkertijd met de proliferatie van lymfocyten neemt de activiteit van cellen die bescherming bieden tegen tumoren af.
Lymfocyten en sommige andere cellen in het lichaam zijn in staat om speciale informatiemoleculen te produceren, cytokinen genaamd. Deze moleculen zorgen, afhankelijk van hun type, voor de interactie tussen cellen, bepalen hun levensduur, stimuleren of remmen celgroei, celdeling, -activiteit en celdood (apoptose). Ze zorgen ook voor de coördinatie van het immuunsysteem, het zenuwstelsel en de endocriene klieren. Onder de cytokinen bevinden zich moleculen die ontstekings- en tumorprocessen remmen, en moleculen die de immuunrespons reguleren. Een afname van de activiteit van deze moleculen kan de weg vrijmaken voor tumorvorming.
Risicofactoren
Risicofactoren voor de ontwikkeling van T-cellymfoom zijn onder meer:
- Ontstekingsprocessen in het lichaam die een overeenkomstige reactie van het immuunsysteem veroorzaken en leiden tot de ophoping van lymfocyten in het aangetaste gebied.
- De aanwezigheid van een virusinfectie in het lichaam (herpesvirussen type 1, 4 en 8, hepatitis B- en C-virussen, lymfocytair virus, HIV-infectie en zelfs Halicobacter pylori).
- Onvoldoende functioneren van het immuunsysteem als gevolg van reeds bestaande mutaties en structurele veranderingen. We hebben het over auto-immuunziekten, de toediening van immunosuppressiva aan het lichaam die de werking van het immuunsysteem onderdrukken.
- Langdurig contact met kankerverwekkende stoffen.
- Erfelijke aanleg en aangeboren immuundeficiëntie.
- Langdurige blootstelling aan ioniserende en ultraviolette straling en bepaalde chemicaliën die mutaties in lymfocyten veroorzaken.
- Chronisch beloop van verschillende soorten dermatosen (psoriasis, atopische dermatitis, enz.), wat leidt tot een langdurige aanwezigheid van lymfocyten in het getroffen gebied, wat leidt tot een afname van de immuniteit en proliferatie van kwaadaardige klonen in het lokale gebied. Dit kan leiden tot de vorming van een kwaadaardig proces op de huid.
- Gevorderde leeftijd.
Meestal wordt de ontwikkeling van de ziekte niet veroorzaakt door één oorzaak, maar door een combinatie van meerdere factoren. Dit kan de reden zijn waarom specifieke manifestaties van de ziekte zich vooral voordoen op volwassen leeftijd, nadat het lichaam langdurig negatief is beïnvloed door verschillende factoren.
 [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Symptomen T-cel lymfoom
Bij het bespreken van de symptomen van de ziekte is het belangrijk te begrijpen dat de verschillende typen T-cellymfoom hun stempel drukken op het klinische beeld van de ziekte in elk specifiek geval. Er zijn echter enkele veelvoorkomende symptomen die kenmerkend zijn voor veel oncologische pathologieën.
De eerste, zij het niet-specifieke, tekenen van de ontwikkeling van de ziekte zijn:
- oorzaakloos verlies van eetlust, verstoring van het spijsverteringsproces,
- gewichtsverlies, ondanks het feit dat de hoeveelheid en de calorische inhoud van het voedsel geen significante veranderingen ondergingen,
- chronische zwakte, verminderde prestaties,
- apathie ten opzichte van wat er om ons heen gebeurt,
- verhoogde reactie op stressfactoren,
- toegenomen zweten (hyperhidrose), vooral 's nachts,
- constante licht verhoogde temperatuur (subfebriele temperatuurmetingen liggen binnen het bereik van 37-37,5 graden),
- chronische constipatie, als de tumor zich in het bekkengebied bevindt,
Specifieke symptomen van T-cellymfoom zijn onder meer:
- aanhoudende vergroting en verharding van de lymfeklieren,
- een toename van de grootte van de interne organen (meestal de lever en de milt),
- roodheid en branderigheid van de huid, het verschijnen van snelgroeiende laesies in de vorm van zweren, plaques, papels,
- verstoring van de structuur (vernietiging) van botweefsel.
Vormen
De ziekte kan verschillende beloop hebben. Daarom worden de volgende vormen van pathologie onderscheiden:
- Acute vorm.
Het wordt gekenmerkt door een snelle ontwikkeling van de ziekte. Tussen het verschijnen van de eerste tekenen en het volledig openbaren van alle symptomen duurt het niet langer dan twee weken. Een dergelijk verloop van de ziekte wordt waargenomen bij meer dan de helft van alle patiënten met de diagnose T-cellymfoom.
Vergroting van de lymfeklieren is bij deze vorm van pathologie meestal afwezig. De dood treedt binnen zes maanden na het begin van de ziekte op door complicaties zoals longontsteking, infectie van de aangetaste huid, botvernietiging met vergiftiging van het lichaam met afbraakproducten, verminderde immuniteit, leptomeningitis met psychische stoornissen, enz.
- Lymfomateuze vorm.
Vergelijkbaar met het hierboven genoemde klinische beeld. Een van de symptomen van de pathologie is echter vergrote lymfeklieren. Dit ziekteverloop wordt waargenomen bij een vijfde van de patiënten.
- Chronische vorm.
Het klinische beeld ontwikkelt zich pas na langere tijd en is minder uitgesproken. Het zenuwstelsel, het spijsverteringsstelsel en het skelet worden pas aangetast als de ziekte acuut wordt. Patiënten leven ongeveer twee jaar met de pathologie.
- Smeulende vorm.
De zeldzaamste vorm van de ziekte, kenmerkend voor 5 op de 100 patiënten. Er wordt een klein aantal gemuteerde T-lymfocyten waargenomen, de proliferatie verloopt langzamer dan bij andere vormen van lymfoom. Desondanks zijn er duidelijke symptomen van schade aan de huid en longen. De levensverwachting van patiënten is ongeveer 5 jaar.
We gaan dieper in op de verschijnselen van T-cellymfoom, waarbij we de verschillende soorten pathologie en hun kenmerkende beloop onderzoeken.
Omdat T-cellymfomen niet alleen kunnen verschillen in de locatie van het pathologische proces, maar ook in de externe manifestaties en het mechanisme van ontstaan, is het gebruikelijk om ze in de volgende typen te classificeren:
De oorzaak van het ontstaan van dergelijke neoplasmata wordt toegeschreven aan mutaties van volwassen T-lymfocyten onder invloed van ongunstige factoren (virussen, straling, brandwonden), waardoor ze de mogelijkheid krijgen om zich actief te vermenigvuldigen en clusters van gemuteerde klonen te vormen in de opperhuidlaag.
Klinisch beeld: er zijn verschillende soorten huiduitslag op de huid (plaques, blaren, vlekken, papels, enz.).
De pathologie ontwikkelt zich meestal in drie stadia. Aan het begin van de ziekte merken patiënten de verschijning van eczeemachtige plekjes die beginnen te jeuken en te vervellen, waarna plaque-achtige formaties op hun plaats verschijnen, die geleidelijk groeien en boven het lichaamsoppervlak uitsteken. Vervolgens voegen mutante klonen die door het lymfestelsel circuleren zich bij de "verkeerde" lymfocyten in de huid, waardoor de kanker uitzaait, wat binnen 2-5 jaar tot de dood van de patiënt leidt.
- Perifeer T-cellymfoom.
Dit concept omvat alle tumorelementen die gevormd worden door T- of NK-lymfocyten (ontstekingsremmende elementen en natuurlijke killercellen met een antitumoreffect). Alleen volwassen cellen die vatbaar zijn voor overmatige proliferatie, zijn bij het proces betrokken. Dergelijke lymfomen kunnen zich vormen in lymfeklieren en in inwendige organen in de buurt van de aangetaste lymfeklieren. Ze beïnvloeden de bloedkwaliteit, de conditie van de huid en het beenmerg en leiden tot vernietiging van botweefsel.
Klinisch beeld: vergrote lymfeklieren in de hals, liezen en oksels. Dit type pathologie wordt gekenmerkt door niet-specifieke symptomen van de hierboven beschreven ziekte, plus enkele onaangename verschijnselen die gepaard gaan met vergrote organen (meestal de lever en milt). Patiënten merken ademhalingsproblemen, terugkerende, onterechte hoest en een zwaar gevoel in de maag.
Artsen stellen zelden de diagnose 'perifeer lymfoom' als ze de pathologie niet als een specifiek type kunnen classificeren. Perifeer lymfoom wordt gekenmerkt door een acuut (agressief) beloop met uitzaaiingen naar andere organen.
- Angioimmunoblastisch T-cellymfoom.
Kenmerkend is de vorming van afdichtingen in de lymfeklieren met een infiltraat in de vorm van immunoblasten en plasmacellen. In dit geval wordt de structuur van de lymfeklier vernietigd, maar vormt zich eromheen een groot aantal pathologische bloedvaten, wat het ontstaan van nieuwe pathologieën veroorzaakt.
De ziekte heeft een acuut verloop. Er is direct sprake van een verdikking van verschillende lymfekliergroepen, lever en milt, huiduitslag en andere kankerverschijnselen. Plasmacellen zijn te vinden in het bloed.
- T-cellymfoblastisch lymfoom, dat in zijn beloop lijkt op acute T-lymfoblastische leukemie.
T-lymfocyten met een onregelmatige structuur nemen deel aan de ontwikkeling van het tumorproces. Ze hebben geen tijd om te rijpen, waardoor ze een onvolmaakte celkern hebben en zich snel beginnen te delen, waarbij ze dezelfde onregelmatige structuren vormen.
Dit is een vrij zeldzame aandoening met een redelijk goede prognose, mits de ziekte wordt ontdekt voordat deze het beenmergsysteem aantast.
T-cellymfomen van verschillende typen doorlopen gewoonlijk vier stadia in hun ontwikkeling:
- In het eerste stadium van de pathologie wordt een toename in slechts één lymfeklier of lymfeklieren van één groep waargenomen.
- In het tweede stadium is er sprake van een toename van lymfeklieren van verschillende groepen, gelegen aan één kant van het middenrif.
- Het derde stadium van de ziekte wordt gekenmerkt door vergrote lymfeklieren aan beide zijden van het middenrif, wat erop wijst dat het kwaadaardige proces zich heeft uitgebreid.
- De vierde fase is de verspreiding van metastasen. Kanker tast niet alleen het lymfestelsel en de huid aan, maar verspreidt zich ook naar inwendige organen (nieren, longen, lever, maag-darmkanaal, beenmerg, enz.).
Hoe eerder lymfoom wordt ontdekt, hoe groter de kans dat iemand de ziekte aankan. In stadium 4 zijn deze kansen vrijwel nihil.
Mediastinaal T-cellymfoom
Het aantal kankergevallen neemt helaas toe. Elk jaar worden oncologische klinieken overspoeld met steeds meer patiënten, waaronder het leeuwendeel van de patiënten met de diagnose mediastinaal T-cellymfoom.
Voor degenen die niet helemaal bekend zijn met de medische terminologie en de menselijke anatomie, zullen we uitleggen dat het mediastinum niet één van de organen is, maar het gebied tussen het borstbeen en de wervelkolom, waar alle organen van de borstkas zich bevinden (slokdarm, bronchiën, longen, hart, thymusklier, longvlies, vele zenuwen en bloedvaten).
Als ongecontroleerde deling van T-lymfocyten leidt tot de ontwikkeling van een tumor in een van de organen van de borstkas, spreekt men van een mediastinaal lymfoom. Het gevaar schuilt in het feit dat het proces zich snel naar andere organen kan verspreiden. Kankercellen verplaatsen zich immers gemakkelijk door het lymfestelsel en spoelen verschillende organen aan (inclusief de door de ziekte aangetaste organen), ten minste binnen één groep lymfeklieren en verder.
Symptomen van een mediastinaal lymfoom zijn over het algemeen typerend voor alle oncologische aandoeningen (zwakte, misselijkheid, gewichtsverlies, kortademigheid, enz.). Een specifiek symptoom dat de lokalisatie van het pathologische proces aangeeft, is een toename van lymfeklieren in de borstkas en daarbuiten (hals, oksels, liezen, buik). Belangrijk is dat de patiënt geen pijn voelt bij het drukken op de gezwollen lymfeklieren, wat niet wijst op een ontstekingsproces, maar op een kwaadaardig proces.
In het beloop van het mediastinaal T-lymfoom zijn er niet vier, maar vijf stadia:
- Het verschijnen van verschillende verdachte vlekken op de huid
- Het aantal huidletsels neemt toe, maar de lymfeklieren blijven onveranderd
- Er ontstaat zwelling in het gebied van de vlekken,
- De vlekken beginnen ontstoken en rood te worden,
- Het proces verspreidt zich naar binnen, naar de organen in het mediastinum.
Mediastinaal T-cellymfoom wordt het vaakst vastgesteld bij mensen van middelbare leeftijd en ouderen. Bij ouderen is de ziekte ernstiger en zaait deze snel uit door het hele lichaam.
 [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
[ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
Diversiteit van cutane T-cellymfomen
Het bijzondere aan dit type lymfoom is dat de ongecontroleerde celdeling niet ontstaat in de lymfeklieren en organen, maar in de huid, van waaruit het proces zich verspreidt naar het lichaam. Binnen cutane T-cellymfomen kunnen er zowel snelgroeiende (agressieve) subtypes als varianten met een traag beloop voorkomen.
Artsen classificeren de volgende lymfomen als agressieve lymfomen die snel uitzaaien naar andere organen en klieren:
- Syndroom van Sézary, een pathologie waarbij het aantal eosinofielen in het bloed stijgt. In dit geval zijn er noodzakelijkerwijs drie symptomen aanwezig: erytrodermie (roodheid van de huid met lamellaire vervelling, uitgebreide rode huiduitslag), lymfadenopathie (vergrote lymfeklieren) en de aanwezigheid van specifieke cellen met geplooide kernen in het bloed, die worden gedetecteerd tijdens laboratoriumonderzoek en biopsie.
- T-celleukemie-lymfoom bij volwassenen is een huidtumor die wordt veroorzaakt door het retrovirus HTLV-1. Symptomen: huid- en lymfeklierafwijkingen, vergroting van lever en milt (hepatosplenomegalie), volledige, niet-gecompenseerde resorptie van botweefsel door metastasering (osteolyse).
- Neustype extranodaal T-cellymfoom (polymorfe reticulose). Ontwikkelt zich uit NK-achtige T-leukocyten met een onregelmatige vorm. Beïnvloedt de huid, de bovenste luchtwegen (bronchiën, luchtpijp, longen) en het maag-darmkanaal, en structuren in het midden van de schedel in het aangezicht (gehemelte, neus, sommige delen van het centrale zenuwstelsel). Huidletsels in de vorm van zegels (plaques) met een bruinblauwe kleur worden al waargenomen in stadium 3 van de ziekte.
- Perifeer ongespecificeerd T-cellymfoom van de huid. Gekenmerkt door het verschijnen van laesies in de epidermale lagen en vergroting van de lymfeklieren, kan het proces zich vervolgens diep in het lichaam verspreiden.
- Primair cutaan agressief epidermotroop CD8+ T-cellymfoom. Polymorfe elementen (noduli, plaques, vlekken) worden op de huid gevormd, vaak met ulceraties in het centrum. Het infiltraat is ook te vinden in de longen, testikels bij mannen, slijmvliezen en het centrale zenuwstelsel.
- Cutaan γ/δ T-cellymfoom, waarbij necrotische noduli en tumoren voornamelijk op de extremiteiten voorkomen, soms op de slijmvliezen. Beenmerg, lymfeklieren en milt worden zelden aangetast.
Dit is een onvolledige lijst van snelgroeiende lymfomen, waarvan de levensverwachting van patiënten niet meer dan 2 jaar bedraagt. Snelle ontwikkeling is kenmerkender voor perifere lymfomen. Dit komt waarschijnlijk doordat de lymfe zich van de periferie naar het centrum verplaatst, waardoor "zieke" leukocyten snel naar verschillende inwendige organen worden getransporteerd, waar ze zich snel kunnen vestigen en vermenigvuldigen.
Een trage voortgang van het proces wordt waargenomen bij pathologieën zoals:
- Mycosis fungoides, die veel patiënten niet eens associëren met een kankergezwel vanwege de gelijkenis met sommige dermatologische aandoeningen. Symptomen: het verschijnen van plaques van verschillende vormen en groottes op de huid (soms bedekt met schilfers en jeukend, wat lijkt op psoriasis), die geleidelijk in omvang toenemen en zich ontwikkelen tot een tumor. Daarnaast zijn er zwelling van de huid, vergrote lymfeklieren (lymfadenopathie), verdikking van de huid op de handpalmen en voetzolen (hyperkeratose), haaruitval, verslechtering van de nagels, zwelling en eversie van de oogleden, vergroting van de lever en milt.
- Primair anaplastisch T-cellymfoom, een subtype van de pathologie met de algemene naam "grootcellig lymfoom", wordt gekenmerkt door de verschijning van paarsrode knobbeltjes van verschillende grootte (1-10 cm) op de huid. Dit kunnen enkele huiduitslagen zijn, maar het verschijnen van een groot aantal knobbeltjes komt ook vrij vaak voor.
- Panniculitis-achtig T-cellymfoom subcutaan. Het tumorproces begint in het onderhuidse weefsel. Symptomen: verhoogde eosinofielen in het bloed, jeuk en huiduitslag, aanhoudende koorts, vergrote lever en milt, vergrote lymfeklieren, geelzucht, oedeemsyndroom, gewichtsverlies.
- Primair cutaan CD4+-pleomorf T-cellymfoom. Het infiltraat bestaat uit kleine en grote cellen. Plaque en nodulaire laesies zijn zichtbaar op het gezicht, de hals en het bovenlichaam.
Bij deze en enkele andere subtypes van cutaan T-cellymfoom kunt u 5 jaar of langer met de ziekte leven.
Complicaties en gevolgen
Wat betreft T-celtumorpathologieën, die geclassificeerd worden als kwaadaardige non-Hodgkinlymfomen, is het niet zozeer de pathologie zelf die angstaanjagend is, maar de complicaties ervan. In de vroege stadia tast T-cellymfoom alleen de huid en het lymfestelsel aan, wat zich manifesteert in lichte ongemakken. Maar de toename van de tumorgrootte en uitzaaiingen naar andere organen verstoren geleidelijk de werking van het hele lichaam, wat leidt tot de dood van patiënten.
Een sterk vergrote lymfeklier kan de vena cava superior (vena cava superior) comprimeren, die bloed levert aan het hart, de slokdarm en het spijsverteringskanaal, de luchtwegen, de urinewegen en de galwegen, waardoor de doorstroming van vocht, lucht en voedsel wordt beperkt. Compressie van het ruggenmerg leidt tot pijn en verminderde gevoeligheid van de ledematen, wat hun bewegingsvrijheid beïnvloedt.
Kankercellen kunnen zich via het lymfestelsel verspreiden naar de botten, hersenen, ruggenmerg, botten, lever en andere organen, waar lymfe door een van de lymfekliergroepen stroomt. De tumor vergroot het orgaan, waardoor het inwendige volume afneemt of de structuur ervan wordt vernietigd, wat noodzakelijkerwijs de functionaliteit beïnvloedt.
De afbraak van een groot aantal tumorcellen leidt tot vergiftiging van het lichaam met een verhoging van de temperatuur, zwakte en verstoring van de gewrichtsfunctie als gevolg van de ophoping van urinezuur in de cellen (gevormd als gevolg van de ontbinding van de celkern).
Elke oncologische ziekte ontwikkelt zich tegen de achtergrond van een algemene afname van de immuniteit, waardoor verschillende soorten infecties (bacteriën, virussen, schimmels) vrijelijk het lichaam kunnen binnendringen. Zo kan lymfoom gecompliceerd worden door infectieziekten.
De gevolgen van T-cellymfomen hangen af van de mate van maligniteit van het proces, de snelheid van verspreiding, de nauwkeurigheid van de diagnose en de tijdigheid van de behandeling.
 [ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ], [ 42 ]
[ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ], [ 42 ]
Diagnostics T-cel lymfoom
Ondanks de overeenkomsten tussen veel soorten T-cellymfoom, kunnen de kenmerken van hun progressie en de behandeling ervan verschillen. Dit betekent dat de arts de diagnose van de ziekte bijzonder zorgvuldig moet benaderen om het type en het ontwikkelingsstadium ervan nauwkeurig te bepalen en een strategie te ontwikkelen om deze vreselijke ziekte te bestrijden.
De diagnose van T-cellymfoom begint, zoals gebruikelijk, met een onderzoek door een oncoloog. Het is erg belangrijk om de arts te informeren over alle symptomen en het tijdstip waarop ze zich voordoen. Dit is noodzakelijk om het stadium van de ziekte en de prognose nauwkeurig te bepalen. Het is ook belangrijk om gevallen van oncologische aandoeningen in de familie te vermelden.
Tijdens de afspraak palpeert de arts de vergrote lymfeklieren en bepaalt de mate van pijn. Bij kankerpathologieën zijn de lymfeklieren pijnloos.
De patiënt wordt vervolgens doorverwezen voor onderzoek. In eerste instantie wordt een verwijzing gegeven voor een bloedonderzoek (algemeen en biochemisch) en een urineonderzoek, waarmee ontstekingsprocessen in het lichaam, veranderingen in de concentratie van verschillende bloedcomponenten (bijvoorbeeld een toename van eosinofielen), de aanwezigheid van vreemde of gewijzigde componenten en toxische stoffen kunnen worden opgespoord.
Daarnaast wordt er een immunologisch bloedonderzoek uitgevoerd. Als een dergelijke analyse te weinig IgG aantoont, is de kans groot dat er sprake is van een kwaadaardig tumorproces in het lymfestelsel. Een bloedtest op antistoffen kan de aanwezigheid van virussen in het lichaam aantonen die de ontwikkeling van lymfoom kunnen veroorzaken.
Optioneel kunt u in privéklinieken een uitgebreid moleculair genetisch onderzoek laten uitvoeren, waarbij bloed- en urinetests, PCR-analyse, testen op hormonen, infecties, virussen, etc. of nog beter, screening op lichaamskanker worden uitgevoerd.
Vervolgens wordt bij huidpathologieën een afkrabsel van het aangetaste gebied genomen en bij vergrote lymfeklieren of vermoeden van schade aan inwendige organen een punctiebiopsie uitgevoerd. Het verkregen materiaal wordt opgestuurd voor cytologisch onderzoek.
Instrumentele diagnostiek van T-cellymfoom omvat:
- Röntgenfoto,
- Computer- en magnetische resonantiebeeldvorming (MRI), waarmee u de toestand van het lichaam van binnenuit vanuit verschillende hoeken kunt bekijken.
- Echografie van de buikholte bij verdenking op mediastinaal lymfoom.
- Scintigrafie voor het opsporen van metastasen en botweefselletsels.
- Computeraxiale tomografie.
Afhankelijk van het type T-cellymfoom en het stadium waarin het zich bevindt, selecteert de oncoloog de meest geschikte diagnostische methoden voor de ziekte.
Differentiële diagnose
Differentiële diagnostiek is een belangrijk punt bij het stellen van een accurate diagnose, met name bij cutane lymfomen, die in veel opzichten lijken op dermatologische aandoeningen (bijvoorbeeld eczeem, psoriasis, dermatitis), en aandoeningen die gepaard gaan met lymfadenopathie. Dit laatste punt is zeer belangrijk, aangezien de vergroting van lymfeklieren zowel kwaadaardig (bij lymfomen) als goedaardig (bij ontstekingsprocessen in het lichaam) kan zijn.
Met wie kun je contact opnemen?
Behandeling T-cel lymfoom
Oncologische pathologieën zijn nooit als gemakkelijk te behandelen beschouwd, maar T-cellymfoom is, ondanks alle gevaren van de situatie, geen reden om op te geven. De behandelmethode en, in grotere mate, het behandelresultaat hangt altijd af van de tijdigheid van antitumormaatregelen en het type T-celpathologie.
De belangrijkste methoden om kwaadaardige lymfekliertumoren te bestrijden zijn:
- Systemische therapie met chemische medicijnen die de tumorgroei stoppen (chemotherapie).
- Blootstelling van de tumor aan ioniserende straling (elektronentherapie, de enige fysiotherapeutische behandelingsmethode voor kwaadaardige lymfomen).
- Het gebruik van corticosteroïden (ontstekingsremmende therapie),
- Het nemen van medicijnen die antitumorprocessen in het lichaam activeren (biotherapie). De medicijnen worden rechtstreeks uit de celstructuren van de patiënt gemaakt.
- Beenmergtransplantatie. In dit geval wordt eerst intensieve chemotherapie (myeloablatieve therapie) toegediend, gericht op het volledig vernietigen van kankercellen en het onderdrukken van het immuunsysteem om afstoting van het transplantaat te voorkomen. Vervolgens krijgt de patiënt gezonde stamcellen van een donor of van zichzelf, afgenomen vóór de start van de chemotherapie.
- Het nemen van medicijnen die het immuunsysteem stimuleren en vitamines om de immuniteit te versterken.
- Chirurgische behandeling. Tumorverwijdering wordt alleen operatief uitgevoerd bij geïsoleerde laesies, vooral wanneer de tumor zich in het maag-darmkanaal bevindt. Om terugkeer van de tumor na verwijdering te voorkomen, is chemotherapie met meerdere antitumormiddelen tegelijk geïndiceerd (polychemotherapie).
Chirurgische behandeling van T-cellymfoom is niet altijd gerechtvaardigd. Ten eerste worden in de meeste gevallen meerdere laesies gevonden, en de migratie van pathologische cellen door het lymfestelsel draagt bij aan de vrij snelle verspreiding van de ziekte naar andere organen (metastasen), waarvoor soms niet één, maar meerdere operaties nodig zijn. En als we bedenken dat kanker het lichaam aanzienlijk verzwakt, dan kan niet elke patiënt één, laat staan meerdere, chirurgische ingrepen doorstaan.
De behandelaanpak kan uiteraard variëren, afhankelijk van de lokalisatie en prevalentie van het proces. Zo zijn voor de behandeling van een milde vorm van mycosis fungoides (erythemateuze mycosis) corticosteroïden en interferonpreparaten geïndiceerd. Chemotherapie wordt niet voorgeschreven en bestraling wordt niet toegepast.
Bij andere vormen van T-cellymfomen van de huid kan zowel systemische als lokale behandeling worden voorgeschreven. Lokale behandeling van T-pathologieën van huidkanker kan worden uitgevoerd met het medicijn in de vorm van een gel, "Valchlor", geproduceerd in de VS. Helaas is dit medicijn in ons land nog steeds niet verkrijgbaar.
De werkzame stof van het geneesmiddel is mechlorethamine. Geneesmiddelen met deze werkzame stof (bijvoorbeeld Embikhin) worden gebruikt voor systemische behandeling van T-celvormen van huidkanker. Ook antitumormiddelen zoals Vinblastine, Fludarabine, Dacarbazine, Chlorbutine, Adriamycine, Vincristine, Cyclofosfamide en andere kunnen worden gebruikt als onderdeel van polychemotherapie.
Bij huidpathologieën worden ook antitumorantibiotica (bijvoorbeeld rubomycine), corticosteroïden (bijvoorbeeld prednisolon, triamcinolon) en lichttherapie (meestal PUVA-therapie) gebruikt.
Bij de biotherapie van T-cellymfomen kunnen zowel patiëntcelpreparaten als monoklonale antilichamen in de vorm van Rituxan, MabThera, Campath, Campath, Avastin en Bexar worden gebruikt.
Behandeling van de gevolgen van hooggedoseerde myeloablatieve therapie wordt uitgevoerd met de geneesmiddelen "Filstim", "Zarcio", "Neupomax", enz.
Medicijnen kunnen oraal of intraveneus worden toegediend. De meeste medicijnen zijn bedoeld voor infuustoediening. De behandeling dient onder strikt toezicht van een oncoloog te worden uitgevoerd.
Radiotherapie voor T-cellymfoom duurt meestal 21-40 dagen. De bestraling vindt lokaal plaats, zonder andere lichaamsdelen te beschadigen. De duur en dosis van de bestraling worden bepaald door een radioloog, afhankelijk van de lokalisatie en het stadium van het tumorproces.
In de beginfase van de pathologie kan radiotherapie als zelfstandige behandelmethode worden voorgeschreven, daarna wordt het in combinatie met chemotherapie gebruikt.
Bij sluimerende vormen van T-lymfoom hebben artsen geen haast met het voorschrijven van een conservatieve behandeling, maar nemen ze een afwachtende houding aan. De patiënt wordt regelmatig gecontroleerd door een oncoloog en bij exacerbatie krijgt hij een effectieve therapie voorgeschreven, afgestemd op het type pathologie.
Medicijnen voor T-cellymfoom
Het is belangrijk om meteen te vermelden dat de behandeling van kanker, ongeacht de oorzaak, een serieuze zaak is die door specialisten moet worden behandeld. Welke medicijnen effectief zijn voor een specifieke pathologie en welk behandelschema moet worden gebruikt, wordt bepaald door een specialist. Artsen raden het ten zeerste af om zelf een behandeling voor te schrijven.
Er zijn tegenwoordig heel wat medicijnen voor de behandeling van tumorziekten. Wat hun effectiviteit betreft, is het belangrijk om op te merken dat een tijdige start van de therapie in de meeste gevallen positieve resultaten oplevert. Het is duidelijk dat vergevorderde kankerstadia zelfs buiten het bereik van chemotherapie vallen. Bovendien is elk organisme uniek, en wat de ene patiënt de gewenste verlichting brengt, redt niet altijd het leven van een andere patiënt.
Laten we eens een paar van de medicijnen bekijken die artsen gebruiken om T-cellymfomen van verschillende oorsprong te behandelen.
"Embikhin" is een alkylerend cytostatisch geneesmiddel waarvan de werking gericht is op de vernietiging van de celstructuur van T-lymfocytklonen met genmutaties.
Het medicijn wordt intraveneus toegediend volgens een van de twee volgende schema's:
- De shockmethode is ontworpen voor een vierdaagse chemotherapiekuur. Dagelijks, eenmaal daags, krijgt de patiënt het medicijn toegediend in een dosering van 0,1 mg per kilogram lichaamsgewicht. Soms wordt het medicijn in één keer in de volledige dosering voorgeschreven.
- Fractionele methode. Het medicijn wordt 3 keer per week toegediend. De gebruikelijke dosering is 5-6 mg. De kuur bestaat uit 8 tot 20 toedieningen.
Het kan in de pleuraholte en de buikholte worden toegediend.
Het medicijn wordt niet voorgeschreven bij gecompliceerde gevallen van de ziekte, ernstige bloedarmoede en sommige bloedziekten (leukopenie en trombocytopenie). De vraag of het medicijn wel gebruikt kan worden, zal ook rijzen bij ernstige nier- en leverschade, evenals bij cardiovasculaire aandoeningen.
Vaak voorkomende bijwerkingen zijn onder meer veranderingen in de bloedeigenschappen, symptomen van bloedarmoede, maag-darmklachten en soms zwakte en hoofdpijn. Als het geneesmiddel tijdens de injectie onder de huid terechtkomt, kan dit leiden tot infiltratie en weefselnecrose op de injectieplaats. De ernst van de belangrijkste bijwerkingen tijdens intensieve therapie is veel ernstiger dan bij fractionele toediening van het geneesmiddel.
Vinblastine is een antineoplastisch geneesmiddel op basis van de alkaloïde maagdenpalm. Het heeft een antitumoreffect doordat het de celdeling blokkeert.
Het medicijn kan alleen intraveneus worden toegediend, waarbij moet worden vermeden dat het onder de huid terechtkomt. De dosis wordt gekozen op basis van het gekozen chemotherapieregime. De standaarddosering is 5,5 tot 7,4 mg per vierkante meter lichaamsoppervlak (kinderdosis van 3,75 tot 5 mg per vierkante meter). Het medicijn wordt eenmaal per week voorgeschreven, soms eenmaal per twee weken.
Er is een ander toedieningsschema, waarbij de behandeling begint met de minimale pediatrische dosis en deze geleidelijk verhoogt tot 18,5 mg per vierkante meter lichaamsoppervlak. Voor kinderen is de startdosis 2,5 mg en de maximale dosis 12,5 mg per vierkante meter lichaamsoppervlak.
De behandeling met het medicijn hangt af van het aantal witte bloedcellen in het bloed.
Het geneesmiddel mag niet worden gebruikt bij ernstige beenmergdepressie, infectieziekten, zwangerschap en borstvoeding. Het geneesmiddel mag niet worden gebruikt bij overgevoeligheid voor de bestanddelen.
Vaak voorkomende bijwerkingen: leukopenie en granulocytopenie. Verstoringen in andere organen en systemen worden veel minder vaak waargenomen.
"Rubomycine" is een geneesmiddel dat behoort tot de categorie antitumormiddelen, dat wil zeggen dat het tegelijkertijd kanker- en bacteriecellen bestrijdt.
Het medicijn wordt ook intraveneus toegediend om infiltratie en necrose van huidweefsel te voorkomen. Het medicijn wordt voorgeschreven voor een kuur van 5 dagen, waarbij de patiënt het medicijn krijgt in een dosering van 0,8 mg per 1 kg lichaamsgewicht. De kuur wordt na 7-10 dagen herhaald. Nu wordt het medicijn voorgeschreven voor een periode van 3 tot 5 dagen in een dosering van 0,5-1 mg per 1 kg lichaamsgewicht per dag. De dosering voor kinderen bedraagt 1 tot 1,5 mg per 1 kg lichaamsgewicht per dag.
Er bestaan veel kankerbehandelingen waarbij het medicijn in combinatie met andere antitumormiddelen wordt gebruikt. De dosering en toedieningsfrequentie kunnen hierbij verschillen.
Contra-indicaties voor het gebruik van het geneesmiddel zijn ernstige aandoeningen van het hart, de bloedvaten, de lever en de nieren, onderdrukking van de beenmergfunctie, zwangerschap en borstvoeding. Bij acute infectieziekten bestaat het risico op diverse complicaties. Alcoholgebruik is verboden.
De meest voorkomende bijwerkingen zijn granulocytopenie en trombocytopenie (een daling van de concentratie granulocyten en bloedplaatjes in het bloed).
"Campas" is een medicijn op basis van monoklonale antilichamen die zich aan lymfocyten binden en deze oplossen, terwijl beenmergstamcellen onaangetast blijven. De productie van T-lymfocyten lijdt er dus niet onder. Rijpe en kwaadaardige lymfocyten sterven af.
Het medicijn wordt via een infuus in het lichaam toegediend. Het intraveneuze infuus is een langdurig proces dat minstens twee uur duurt. Om allergische reacties en pijn te voorkomen, worden vóór de infusie pijnstillers en antihistaminica ingenomen.
Het medicijn wordt gedurende 3 dagen toegediend volgens een schema met oplopende doseringen: 3, 10 en 30 mg, terwijl de reactie van het lichaam op het medicijn constant wordt gecontroleerd. Daarna wordt het medicijn om de dag toegediend gedurende 1-3 maanden. De maximale dosering blijft 30 mg per dag.
Als het medicijn slecht wordt verdragen en er bijwerkingen optreden, wordt de dosis pas geleidelijk verhoogd nadat de reactie op het medicijn weer normaal is.
Het gebruik van het geneesmiddel is verboden bij patiënten met een acute infectieuze pathologie van systemische aard, waaronder gevallen van hiv-infectie, niet-lymfocytaire tumoren, tijdens zwangerschap en borstvoeding, en bij overgevoeligheid voor de bestanddelen. Het gebruik van het geneesmiddel moet worden gestaakt indien toxische reacties worden waargenomen of verdere progressie van de ziekte wordt waargenomen.
Er is onvoldoende informatie over de werking van het medicijn op het lichaam van het kind.
De meest voorkomende bijwerkingen van het medicijn zijn: koude rillingen, koorts, vermoeidheid, een verlaagde bloeddruk en hoofdpijn. Veel mensen ervaren gastro-intestinale reacties in de vorm van misselijkheid, soms met braken, en diarree, veranderingen in de bloedsamenstelling (verminderde granulocyten en bloedplaatjes, bloedarmoede), hyperhidrose en allergische reacties. Sepsis, herpes simplex en longontsteking kunnen ook optreden. Patiënten melden vaak een gevoel van kortademigheid (dyspnoe).
"Neupomax" is een geneesmiddel dat de aanmaak van leukocyten stimuleert, de werkzame stof is filgrastim.
Toediening van hoge doses chemotherapie vóór een beenmergtransplantatie leidt vaak tot een afname van de aanmaak van witte bloedcellen, wat vóór de ingreep gecorrigeerd moet worden. Hetzelfde fenomeen kan worden waargenomen na conventionele chemotherapie. Daarom krijgen patiënten met neutropenie (onvoldoende aanmaak van neutrofiele witte bloedcellen) medicijnen op basis van filgrastim voorgeschreven.
Het medicijn wordt één dag na de chemotherapie voorgeschreven in een dosering van 5 mcg per dag. Het medicijn wordt subcutaan toegediend. De behandelingsduur is maximaal 14 dagen. De therapie wordt voortgezet totdat het optimale aantal neutrofielen in het bloed is bereikt.
Bij myeloablatieve therapie wordt het medicijn voorgeschreven in een dosering van 10 mcg gedurende 4 weken. Het wordt intraveneus toegediend via een infuus.
Het geneesmiddel wordt niet gebruikt bij ernstige congenitale neutropenie (Kastmann-syndroom) en overgevoeligheid voor de bestanddelen van het geneesmiddel. Voorzichtigheid is geboden bij sikkelcelanemie.
Bijwerkingen van het medicijn zijn onder meer: dyspeptische symptomen, myalgie en artralgie, vergrote lever en milt, longinfiltratie, bronchiale spasmen en kortademigheid. Soms worden ook een afname van de botdichtheid, bloeddrukstijgingen, een verhoogde hartslag, gezichtsoedeem, neusbloedingen en zwakte waargenomen. In sommige gevallen worden veranderingen in de bloedsamenstelling waargenomen: een daling van het aantal bloedplaatjes en een toename van leukocyten (trombocytopenie en leukocytose). Eiwit en bloed kunnen in de urine worden aangetroffen (proteïnurie en hematurie).
 [ 54 ], [ 55 ], [ 56 ], [ 57 ], [ 58 ]
[ 54 ], [ 55 ], [ 56 ], [ 57 ], [ 58 ]
Alternatieve kankerbehandelingen
Het lijkt erop dat er effectieve methoden bestaan om kanker te bestrijden (dezelfde bestraling en chemotherapie), en dat er voldoende medicijnen zijn die kwaadaardige cellen kunnen doden, maar niet iedereen kan zich zo'n behandeling veroorloven. Bovendien laten traditionele geneeswijzen veel nieuwe problemen achter die opnieuw behandeld moeten worden.
De gevolgen van chemotherapie zijn bijvoorbeeld te zien in de vorm van alopecia (actief haarverlies), gewichtstoename door toegenomen eetlust, hartritmestoornissen en het ontstaan van hartfalen. In sommige gevallen wordt een nieuwe diagnose (meestal een andere vorm van bloedkanker) aan de bestaande diagnose toegevoegd. Bij mannen kan chemotherapie de onvruchtbaarheid (onvruchtbaarheid) bedreigen.
Complicaties na radiotherapie zijn ook niet ongewoon. Dit kan zijn: verminderde schildklierfunctie (hypothyreoïdie ontwikkelt zich meestal), het ontstaan van radiotherapiepneumonitis, gekenmerkt door littekenvorming in het longweefsel, ontsteking van de darmen of blaas (colitis en cystitis), onvoldoende speekselproductie en stralingsverbranding.
Het blijkt dat we één ding behandelen, maar een ander verlammen. Deze tijd en de hoge kosten van therapie voor T-cellymfoom en andere oncologische aandoeningen dwingen mensen om steeds meer nieuwe behandelmethoden voor deze vreselijke ziekte te zoeken.
Er zijn veel berichten op internet over kankerbehandeling met alternatieve methoden. Sommige mensen wijzen de traditionele behandeling af, omdat ze beweren dat het hun vrienden niet heeft gered, terwijl anderen het actief gebruiken en goede resultaten behalen. We zullen geen standpunt innemen, maar alleen wat informatie verstrekken over de medicijnen die buiten het oncologisch ziekenhuis worden gebruikt.
Veel voorstanders van alternatieve kankerbehandelingen (waaronder veel artsen!) zijn het erover eens dat de oorzaak van kwaadaardige tumoren de zure omgeving van het lichaam is, die zuurstofgebrek heeft voor een normale celfunctie. Door de pH-waarde van de interne omgeving te verhogen, verbetert de celademhaling en stopt de celproliferatie. Het blijkt dat producten die de zuurgraad van het lichaam verlagen en de zuurstoftoevoer naar cellen verbeteren, de ontwikkeling van kwaadaardige processen kunnen stoppen.
Een bijzondere rol in dit opzicht is weggelegd voor een product dat in vrijwel elke keuken aanwezig is: baking soda. Als alkali is het in staat de zuurgraad van elke omgeving te verlagen, inclusief het interne milieu van het lichaam. Het wordt aanbevolen om soda zowel oraal te gebruiken (het alkaliseert het maag-darmkanaal en komt in zekere mate in het bloed terecht) als in de vorm van injecties, waardoor de alkali via het bloed in alle lichaamsdelen terechtkomt. Het is echter aan te raden om de soda vooraf met kokend water te blussen.
Volgens de methode van de Italiaanse arts (!) Tulio Simoncini moet frisdrank tweemaal daags een half uur voor de maaltijd worden ingenomen (de dosis geleidelijk verhogend van 1/5 naar 2 theelepels), verdund met heet water en weggespoeld met een glas vloeistof (water, melk). De frisdrankoplossing moet in direct contact komen met kankercellen; daarom worden lotions, inhalaties, injecties en douches ook gebruikt om verschillende soorten kanker te behandelen.
Een van de aanhangers van deze kankerbehandelingsmethode is onze landgenoot professor Ivan Pavlovich Neumyvakin, die een systeem ontwikkelde voor de behandeling van verschillende soorten kanker met soda en waterstofperoxide. In dit geval wordt geen zuivere peroxide gebruikt, maar een oplossing ervan (1 tot 10 druppels 3% waterstofperoxide worden ingenomen per 50 ml water). Het middel wordt driemaal daags een uur voor de maaltijd ingenomen, waarbij het aantal druppels peroxide elke dag met 1 wordt verhoogd (de eerste dag - 1 druppel, de tweede - twee, enz.). Na 10 dagen behandeling wordt een pauze van 5 dagen ingenomen.
Overigens, om de zuurgraad van de interne omgeving te verlagen en de ontwikkeling van kanker te blokkeren, adviseren wetenschappers die voorstanders zijn van alkalisering van het lichaam om speciale aandacht te besteden aan uw dieet, aangezien ons dieet producten bevat die de pH-waarde kunnen verhogen of verlagen. Alkaliserende producten zijn onder andere bladgroenten, fruit (behalve zeer zoete), gedroogde abrikozen, amandelen, melk en zuivelproducten, bessen en groenten. Maar vlees, worst en gerookt vlees, vis en zeevruchten, eieren, gebak, druivensap, jam en conserven verhogen daarentegen de zuurgraad van het lichaam. Overigens wordt citroen zonder suiker beschouwd als een alkaliserend product, ondanks de zuurgraad, maar als u het met suiker eet, zal het effect juist het tegenovergestelde zijn.
Interessant is een methode om kanker te bestrijden, zoals het drinken van bietensap. Dit verbetert ook de celademhaling en kan de groei en ontwikkeling van kankercellen stoppen. En als we ook rekening houden met de rijke vitamine- en mineralensamenstelling van de felrode wortelgroente, kunnen we met zekerheid stellen dat behandeling met bietensap het immuunsysteem, het zenuwstelsel en andere systemen van het lichaam zal versterken. Dit geeft het lichaam de mogelijkheid om zelfstandig verschillende ziekten, waaronder kanker, te bestrijden.
Het drinken van bietensap gaat goed samen met traditionele behandelingen en vermindert zelfs de negatieve effecten ervan. Maar er is ook informatie over het genezen van kanker met alleen bietensap, wat veel goedkoper is dan een behandeling in een oncologisch ziekenhuis.
Gebruik voor de behandeling versgeperst sap, minimaal 2 uur in de koelkast bewaard, gemaakt van felgekleurde tafelsap. Voor een voldoende antitumoreffect moet u gedurende de dag 600 ml sap drinken. Drink het sap licht opgewarmd een half uur voor de maaltijd. U kunt het mengen met wortelsap.
Drink dagelijks bietensap in kleine slokjes, 100 ml per dosis. De behandeling is langdurig (1 jaar of langer). Om de aandoening te stabiliseren, drinkt u 1 glas sap per dag.
Het is ook nuttig om gekookte bieten te eten, omdat ze bij een korte hittebehandeling vrijwel geen van hun gunstige eigenschappen verliezen.
Overigens kozen volksgenezers niet voor niets voor rode biet. De antitumorwerking ervan wordt erkend door de officiële geneeskunde. Een van de antitumormedicijnen is zelfs ontwikkeld op basis van rode biet.
Veel planten hebben ook antitumoreigenschappen en hoewel de kruidenbehandeling van T-cellymfoom en andere soorten kanker nog niet wijdverbreid is, zijn er positieve beoordelingen over deze behandeling.
Zelfs in de officiële geneeskunde worden planten die caryoclastische gifstoffen bevatten die pathogene cellen kunnen doden, erkend als antitumormiddelen. Tot deze gifstoffen behoren alkaloïden, lactonen en hartglycosiden die in veel planten voorkomen:
- alkaloïdebevattende: Colchicum lucidum en Colchicum magnificum (knollen), stinkende gouwe, berberis, wijnruit, alsem, gele moerasspirea en enkele andere,
- lactonbevattende: Podophila peltata en Himalaya podophila, eucommia, helenium, Vernonia amandel, gaillardia.
- Bevat hartglycosiden: witte heester, tweehuizige en zwarte appelbes, wilde komkommer, duizendknoop, medicinale avran, enz.
Het is belangrijk om te beseffen dat de hierboven genoemde planten giftige stoffen bevatten. De dosering hiervan is daarom strikt beperkt.
De vruchten van de Japanse pagodeboom, radijszaad, klaver, vlierbes en moerasspirea staan ook bekend om hun ontstekingsremmende en antitumorale effecten. Als immunomodulatoren bij T-cellymfoom kunt u extracten van ginseng, echinacea en eleutherococcus gebruiken. Populaire planten zoals brandnetel, calendula, weegbree, paardenbloem en successie blijven niet ver achter.
Homeopathie is niet gericht op de volledige genezing van agressieve kwaadaardige tumoren, maar sommige middelen zijn zeer geschikt als aanvullende en preventieve behandeling. Bijvoorbeeld, als na een traditionele behandeling van kwaadaardig lymfoom exacerbaties worden waargenomen, kan een homeopathisch arts langdurig gebruik van de homeopathische preparaten barium carbonicum (5 korrels onder de tong, 2 keer per dag) en conium (7 korrels voor het slapengaan) voorschrijven.
Carcinosinum en Phytolacca hebben zich bewezen als effectieve antitumormedicijnen, en Echinacea compositum, Mucosa compositum, Edas-308, Galium-Hel en andere homeopathische geneesmiddelen worden gebruikt als immuunstimulantia.
Het voorkomen
Het voorkomen van oncologische aandoeningen met een hoge mortaliteit, waaronder T-cellymfoom, is een complexe kwestie. Eerlijk gezegd hebben wetenschappers nog steeds geen eenduidig antwoord op de vraag: hoe kanker voorkomen kan worden.
Als we kijken naar de factoren die de kans op het ontwikkelen van oncologische aandoeningen vergroten, kunnen we begrijpen dat we ze niet allemaal uit ons leven kunnen weren. Mensen met erfelijke aanleg en immuundeficiënties zullen zich enorm moeten inspannen om het lot van hun naasten met oncologische aandoeningen te vermijden.
Het is belangrijk om te beseffen dat het risico op kanker lager is voor mensen die ontstekingsziekten (inclusief dermatologische) tijdig behandelen, chronische aandoeningen voorkomen, niet met kankerverwekkende stoffen werken, in een ecologisch verantwoord gebied wonen en niet aan straling worden blootgesteld. Er is dus iets om over na te denken, want je leven staat op het spel.
De behandeling van aandoeningen die zich kunnen ontwikkelen tot kanker (precancereuze aandoeningen) speelt ook een grote rol in kankerpreventie. Fytotherapeuten hebben zelfs een kruidenmengsel ontwikkeld dat ongecontroleerde celdeling voorkomt. Het bevat: brandnetel- en weegbreebladeren 5 g per stuk, moerasspireabloemen en berkenkatjes 10 g per stuk, zoethoutwortels 3 g.
Meng de grondig gemalen grondstoffen, neem 10 g van de samenstelling en giet er 1 kopje kokend water over. Laat het ongeveer 20 minuten in een waterbad staan. Na het zeven blijkt dat het glas niet vol is. Je moet het bijvullen met kokend water.
De resulterende infusie moet dagelijks driemaal daags worden gedronken. 1 glas medicijn is voldoende voor 1 dag. Het moet een half uur voor de maaltijd worden gedronken, gedurende 1 tot 2 maanden.
Hoe dan ook, het is beter om alle mogelijke maatregelen te nemen om kanker te voorkomen, dan om na het horen van een vreselijke diagnose keihard voor je leven te vechten.
Prognose
De prognose voor T-cellymfoom is niet erg rooskleurig, vooral niet voor de agressieve vormen, waarvoor soms simpelweg geen tijd is om te vechten. Hoe eerder de ziekte wordt ontdekt, hoe groter de kans om deze te overwinnen. Als de ziekte in een vroeg stadium wordt ontdekt, bedraagt de kans op nog eens 5 jaar of langer, afhankelijk van het type pathologie en de leeftijd van de patiënt, 85-90%.
De prognose is het slechtst voor angio-immunoblastische en T-lymfoblastische lymfomen als het proces zich heeft verspreid naar het beenmerg en andere organen. Bij angio-immunoblastisch T-cellymfoom overlijden patiënten meestal na 2-3 jaar en leeft slechts iets meer dan 30% langer. Verbetering bij gecompliceerde lymfoblastische lymfomen is slechts bij een vijfde van de patiënten waarneembaar. Hoewel, als de ziekte in een vroeg stadium wordt behandeld, is de prognose in de meeste gevallen vrij gunstig.
Bij mycosis fungoides hangt alles af van de vorm en het stadium van de pathologie. De klassieke vorm wordt gekenmerkt door de beste prognose. Tijdige behandeling zonder complicaties kan patiënten 10 jaar of langer leven. Bij gecompliceerde pathologieën wordt de levensverwachting teruggebracht tot 2-5 jaar. Maar bij de Vidal-Brock-vorm overlijden de meeste patiënten binnen een jaar.
T-cellymfoom voedt zich, net als andere kankerpathologieën, met onze angst. De prognose voor het leven hangt daarom grotendeels af van de houding van de patiënt. In de medische praktijk zijn gevallen van "wonderbaarlijke" genezingen bekend, waarbij mensen die op de rand van de afgrond stonden en die artsen niet meer konden helpen, enkel herstelden omdat ze geloofden in de mogelijkheid om de dodelijke ziekte te overwinnen. Hoe de omstandigheden zich ook ontwikkelen, je mag nooit opgeven, want het leven is de grootste waarde voor een mens en het is de moeite waard om ervoor te vechten.
 [ 65 ]
[ 65 ]

