Medisch expert van het artikel
Nieuwe publicaties
Waldenström's B-cel lymfoplasmacytisch lymfoom
Laatst beoordeeld: 12.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
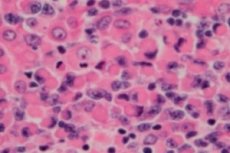
Een maligne lymfoproliferatieve (immunoproliferatieve) aandoening, lymfoplasmacytair lymfoom of macroglobulinemie van Waldenström is een cellulair neoplasma van kleine B-lymfocyten – B-cellen die de beschermende functies van het lymfestelsel en de humorale immuniteit van het lichaam verzorgen. De diagnose dient alleen te worden gesteld na uitsluiting van alle andere kleine B-cellymfomen. Macroglobulinemie van Waldenström werd in 1944 beschreven door Jan G. Waldenström, die ongebruikelijke manifestaties van lymfadenopathische bloeding, bloedarmoede, verhoogde bezinkingssnelheid, hyperviscositeit en hypergammaglobulinemie rapporteerde bij twee patiënten. [ 1 ], [ 2 ]
Epidemiologie
Dit type lymfoom is een zeldzame, langzaam groeiende hematologische maligniteit en volgens klinische statistieken wordt de detectiegraad ervan in deze groep ziekten geschat op ongeveer 2%. Bovendien zijn er bijna twee keer zoveel mannelijke als vrouwelijke patiënten.
Volgens sommige gegevens bedraagt de incidentie van jaarlijkse gevallen van lymfoplasmacytair lymfoom in Europese landen één op de 102 duizend mensen, en in de VS één op de 260 duizend. [ 3 ]
Oorzaken lymfoplasmacytair lymfoom
Tot op heden is de etiologie van de meeste oncologische ziekten nog onbekend, maar het onderzoek naar de genetische basis van sommige ervan gaat door. Door de oorzaken van kwaadaardige plasmacelziekten, waaronder B-cellymfoplasmacytair lymfoom – macroglobulinemie van Waldenström, te bestuderen, hebben onderzoekers een verband ontdekt tussen pathologische proliferatie (celdeling) van B- lymfocyten in een laat stadium van hun differentiatie en de aanwezigheid van bepaalde moleculair-genafwijkingen die fundamentele cellulaire functies beïnvloeden.
Bij patiënten met de ziekte van Waldenström zijn veranderingen in enkele genen vastgesteld - somatische mutaties, dat wil zeggen mutaties die alleen weefsels aantasten, waarbij de genen van een afzonderlijke klonale populatie van cellen zijn beschadigd en er varianten van hun genoom ontstaan, wat leidt tot cyclische en structurele stoornissen op cellulair niveau.
In de eerste plaats zijn dit somatische mutaties van het gen MYD88 (L265P) en CXCR4, dat codeert voor een cytosool eiwit dat belangrijk is voor de aangeboren en adaptieve immuunrespons: als adapter zorgt het voor de overdracht van signalen van de pro-inflammatoire mediator IL-1 (interleukine-1) en Toll-like receptor-cellen die de immuunrespons activeren. Als gevolg van somatische mutatie ontstaan er afwijkingen in de polypeptideketen van het molecuul van dit eiwit - de structurele basis ervan. [ 4 ]
Risicofactoren
Naast de algemene risicofactoren (blootstelling aan verhoogde stralingsniveaus, kankerverwekkende stoffen, enz.) worden de volgende factoren beschouwd als voorspellers van een verhoogde kans op het ontwikkelen van Waldenström-macroglobulinemie als een laaggradige lymfoproliferatieve aandoening:
- ouderdom (ouder dan 65 jaar);
- de aanwezigheid van familieleden met deze diagnose, evenals met B-cel non-Hodgkin-lymfoom of chronische lymfatische leukemie;
- chronische hepatitis C;
- een voorgeschiedenis van goedaardige monoklonale gammopathie, een idiopathische hematologische ziekte waarvan de essentie bestaat uit de productie van abnormaal veranderde gammaglobulinen van het type M door lymfocytplasmacellen;
- auto-immuunziekten, met name het syndroom van Sjögren.
Pathogenese
Bij contact met een antigeen of stimulatie door T-lymfocyten transformeren sommige B-lymfocyten in plasmacellen – lymfocytische plasmacellen – die na bepaalde transformaties beschermende bolvormige eiwitten beginnen te produceren, d.w.z. gammaglobulinen (immunoglobulinen of antilichamen).
De pathogenese van lymfoplasmacytair lymfoom/Waldenström-macroglobulinemie omvat hyperproliferatie van B-cellen, een overmaat aan lymfocytaire plasmacelkloon en overmatige productie van immunoglobuline M (IgM), ook wel monoklonaal immunoglobuline of M-eiwit genoemd, in het bloed. Dit is het belangrijkste antilichaam met een hoog moleculair gewicht en pentamere structuur, geproduceerd tijdens de eerste aanval op specifieke bacteriële of virale antigenen. [ 5 ]
Bijna alle symptomen van deze ziekte worden geassocieerd met de activiteit van het M-proteïne, dat de reologische eigenschappen van het bloed kan verstoren, de viscositeit ervan kan verhogen, de lymfoïde en myeloïde weefsels van het beenmerg kan doordringen en zich kan ophopen in perifere lymfoïde weefsels (met de vorming van langzaam groeiende neoplasmata die druk kunnen uitoefenen op omliggende organen, zenuwvezels of bloedvaten).
Hoewel chronische lymfatische leukemie, macroglobulinemie van Waldenström of lymfoplasmacytair lymfoom en multipel myeloom afzonderlijke ziekten zijn, gaan ze allemaal gepaard met een verhoogde proliferatie van B-lymfocyten.
Symptomen lymfoplasmacytair lymfoom
De eerste tekenen van de ziekte zijn niet-specifiek en kunnen bestaan uit zwakte en toegenomen vermoeidheid (als gevolg van de ontwikkeling van normochrome anemie), gewichtsverlies, kortademigheid, nachtelijke hyperhidrose en terugkerende subfebriele koorts.
Bovendien treedt in het beginstadium van de ziekte een verstoring op van de gevoeligheid van de handen en voeten, treedt er perifere neuropathie op (gevoelloosheid of tintelingen in de voeten en benen), ontstaan er kleine focale bloedingen van de huidcapillairen (purpura) en koude urticaria (als gevolg van de vorming en aggregatie van abnormale cryoglobuline-eiwitten in het bloedserum).
Symptomen die gepaard gaan met het hyperviscositeitssyndroom zijn onder andere hoofdpijn en duizeligheid, netvliesschade en verlies van gezichtsvermogen, oorsuizen en gehoorverlies, krampen, spierpijn, hoge bloeddruk, spontane neusbloedingen en bloedend tandvlees. Vrouwen kunnen baarmoederbloedingen ervaren.
Ook waargenomen: vergrote lymfeklieren (lymfadenopathie); vergrote milt (splenomegalie); hartfalen met cardialgie en hartritmestoornissen. Hoewel viscerale infiltratie zeldzaam is, kunnen de maag en darmen worden aangetast, met de ontwikkeling van diarree (vaak met vette ontlasting). [ 6 ], [ 7 ]
Vormen
De classificatie van tumoren van hematopoëtische en lymfoïde weefsels door de Wereldgezondheidsorganisatie uit 2017 stelt vier diagnostische criteria vast voor Waldenström-macroglobulinemie, waaronder:
- Aanwezigheid van monoklonale IgM-gammopathie
- Infiltratie van beenmerg door kleine lymfocyten die plasmacytoïde of plasmaceldifferentiatie vertonen
- Beenmerginfiltratie met intertrabeculaire structuur
- Immunofenotype dat overeenkomt met de macroglobulinemie van Waldenström, dat oppervlakte-IgM+, CD19+, CD20+, CD22+, CD25+, CD27+, FMC7+, variabele CD5, CD10-, CD23-, CD103- en CD108- omvat
Complicaties en gevolgen
Patiënten met lymfoplasmacytair lymfoom ontwikkelen complicaties en gevolgen in de vorm van:
- verminderde immuniteit;
- beenmergfalen met verstoring van de hematopoëtische functies en de ontwikkeling van bloedarmoede;
- tekort aan gevormde bloedbestanddelen zoals rode bloedcellen, leukocyten en bloedplaatjes;
- laesies van het maag-darmkanaal met chronische diarree en verminderde intestinale absorptie (malabsorptiesyndroom);
- ontsteking van de wanden van de bloedvaten (complexe immuunvasculitis);
- verhoogde broosheid van de botten (osteoporose);
- visuele en auditieve beperkingen;
- secundaire amyloïdose van inwendige organen;
- progressie naar paraproteïnemische hemoblastose in de vorm van multipel myeloom;
- transformatie naar een zeer kwaadaardig type lymfoom – diffuus grootcellig B-cellymfoom.
Diagnostics lymfoplasmacytair lymfoom
De diagnose lymfoplasmacytair lymfoom/Waldenström-macroglobulinemie is meestal moeilijk vanwege het ontbreken van specifieke morfologische, immunofenotypische of chromosomale veranderingen. Dit tekort maakt het onderscheiden van deze ziekte van andere kleincellige B-cellymfomen een kwestie van uitsluiting.[ 8 ]
Naast het beoordelen van de bestaande symptomen zijn voor de diagnose van lymfoplasmacytair lymfoom een algemeen en biochemisch bloedonderzoek, een coagulogram, immuno-elektroforese van bloedproteïnen met bepaling van het niveau van immunoglobuline M in het bloed en een algemeen urineonderzoek noodzakelijk. [ 9 ]
Een beenmergpunctie is nodig en vereist een biopsie van het beenmerg.
Er worden instrumentele diagnostiek verricht: echografie van de lymfeklieren en de milt, röntgenfoto's van de botten, CT-scan van de borstkas en de buikholte, oftalmoscopie.
Differentiële diagnose
Lymfoplasmacytair lymfoom wordt beschouwd als een uitsluitingsdiagnose, daarom wordt differentiële diagnose gesteld bij chronische lymfatische leukemie van de B-cel, multipel myeloom, folliculair lymfoom, verschillende subtypes van non-Hodgkin-lymfoom, plasmacytoom, reactieve plasmacytose, angiofolliculaire lymfoïde hyperplasie (ziekte van Castleman), etc.
Met wie kun je contact opnemen?
Behandeling lymfoplasmacytair lymfoom
Men dient er rekening mee te houden dat de ziekte van Waldenström of het lymfoplasmacytair lymfoom jarenlang asymptomatisch kan zijn en dat de diagnose kan worden gesteld aan de hand van een verhoogd M-proteïnegehalte in het bloed.
Indien er geen symptomen zijn, wordt er actief toezicht gehouden door middel van regelmatige onderzoeken en tests.
Op basis van de bestaande symptomen en de uitslagen van laboratoriumonderzoek wordt besloten om met een behandeling te beginnen. Dit hangt van veel factoren af (bijvoorbeeld leeftijd, ziekteverloop, etc.).
Volgens het protocol bestaat de eerste behandeling van patiënten met dit type lymfoom gewoonlijk uit een combinatie van radiotherapie en chemotherapie met toediening van cytostatica, zoals cyclofosfamide, doxorubicine, vincristine, en corticosteroïden - metprednisolon of dexamethason (dexason).
De effectiviteit van chemotherapie met medicijnen uit de groep van de monoklonale antilichamen, in het bijzonder Rituximab, is bewezen. [ 10 ]
Bij gegeneraliseerde ziekte wordt rituximab gebruikt in combinatie met antitumor nucleoside analogen (pentostatine, cladribine). Bij langzaam progressieve ziekte met lage niveaus van monoklonaal immunoglobuline M wordt naast rituximab ook het cytostaticum chloorambucil (Leukeran) gebruikt. [ 11 ]
Om de viscositeit van het bloed te verlagen en het niveau van de gevormde elementen te stabiliseren, wordt therapeutische hemaferese gebruikt.
Wanneer het niveau van antilichamen in het bloed kritisch laag is, wordt vervangende therapie met immunoglobulinen uitgevoerd om gelijktijdige herhaalde infecties te voorkomen.
Zoals oncohematologen opmerken, ervaren de meeste patiënten, ondanks het feit dat behandeling kan leiden tot remissie van de ziekte, een terugval. Als dit eerder dan 24 maanden gebeurt, kan een antitumormedicijn zoals Ibrutinib (in tabletvorm) worden gebruikt. Bij latere terugvallen wordt de behandeling volgens het oorspronkelijke schema uitgevoerd. [ 12 ], [ 13 ], [ 14 ]
Het voorkomen
Deskundigen bepalen de prognose van de uitkomst van lymfoplasmacytair lymfoom volgens het internationale prognostische systeem voor het beoordelen van de belangrijkste parameters: de leeftijd van de patiënt en de serumniveaus van hemoglobine, bloedplaatjes, bèta-2-microglobuline en monoklonaal immunoglobuline. [ 15 ], [ 16 ]
De gemiddelde overlevingskans bij deze diagnose bedraagt ongeveer vijf jaar, maar bijna 40% van de patiënten leeft tien jaar of langer.

