Medisch expert van het artikel
Nieuwe publicaties
Polycysteus ovariumsyndroom.
Laatst beoordeeld: 04.07.2025

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
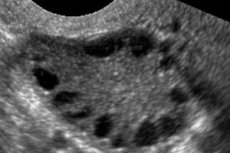
Polycysteus-ovariumsyndroom is een multifactoriële, heterogene aandoening die wordt gekenmerkt door menstruatiecyclusstoornissen, chronische anovulatie, hyperandrogenisme, cystische veranderingen in de eierstokken en onvruchtbaarheid. Het polycysteus-ovariumsyndroom wordt gekenmerkt door matige obesitas, onregelmatige menstruatie of amenorroe en symptomen van een teveel aan androgeen (hirsutisme, acne). De eierstokken bevatten meestal veel cysten. De diagnose wordt gesteld op basis van zwangerschapstesten, hormoonspiegels en onderzoek om een viriliserende tumor uit te sluiten. De behandeling is symptomatisch.
Oorzaken polycysteus ovariumsyndroom
Polycysteus-ovariumsyndroom is een veelvoorkomende endocriene aandoening van het voortplantingssysteem, die voorkomt bij 5-10% van de patiënten. Het wordt gekenmerkt door anovulatie en een overmaat aan androgenen van onbekende oorzaak. De eierstokken kunnen normaal van grootte zijn of vergroot, met een glad, verdikt kapsel. In de regel bevatten de eierstokken veel kleine, 26 mm grote folliculaire cysten; soms worden grote cysten met atretische cellen aangetroffen. De oestrogeenspiegels stijgen, wat leidt tot een verhoogd risico op endometriumhyperplasie en uiteindelijk endometriumkanker. De androgeenspiegels zijn vaak verhoogd, wat het risico op metabool syndroom en hirsutisme verhoogt.
 [ 13 ]
[ 13 ]
Pathogenese
Vrouwen met polycysteus-ovariumsyndroom (PCOS) hebben afwijkingen in het androgeen- en oestrogeenmetabolisme en een verstoorde androgeensynthese. De ziekte gaat gepaard met hoge serumconcentraties van androgeenhormonen zoals testosteron, androsteendion, dehydroepiandrosteronsulfaat en (DHEA-S). Soms kunnen echter normale androgeenspiegels worden vastgesteld.
PCOS wordt ook geassocieerd met insulineresistentie, hyperinsulinemie en obesitas. Hyperinsulinemie kan ook leiden tot onderdrukking van de SHBG-synthese, wat op zijn beurt de androgene eigenschappen kan versterken.
Bovendien wordt insulineresistentie bij PCOS in verband gebracht met adiponectine, een hormoon dat door adipocyten wordt afgescheiden en dat het lipidenmetabolisme en de bloedglucosespiegel reguleert.
Verhoogde androgeenspiegels gaan gepaard met een toename van het stimulerende effect van luteïniserend hormoon (LH), afgescheiden door de hypofyse, wat leidt tot groei van de thecacellen in de eierstokken. Deze cellen verhogen op hun beurt de synthese van androgenen (testosteron, androsteendion). Door een verlaagde follikelstimulerend hormoon (FSH)-spiegel ten opzichte van LH kunnen de granulaire cellen in de eierstokken androgenen niet aromatiseren tot oestrogenen, wat leidt tot een daling van de oestrogeenspiegel en daaropvolgende anovulatie.
Sommige onderzoeken suggereren dat patiënten een functionele stoornis hebben van cytochroom P450c17, 17-hydroxylase, wat de androgeenbiosynthese remt.
Polycysteus-ovariumsyndroom is een genetisch heterogeen syndroom. Studies bij familieleden met PCOS bewijzen autosomaal dominante overerving. Onlangs is een genetisch verband tussen PCOS en obesitas bevestigd. Een variant van het FTO-gen (rs9939609, dat predisponeert tot algemene obesitas) is significant geassocieerd met de vatbaarheid voor het ontwikkelen van PCOS. Polymorfismen van de 2p16-locus (2p16.3, 2p21 en 9q33.3) die geassocieerd zijn met polycysteus-ovariumsyndroom zijn geïdentificeerd, evenals het gen dat codeert voor de receptor van luteïniserend hormoon (LH) en humaan choriongonadotrofine (hCG).
Symptomen polycysteus ovariumsyndroom
Symptomen van polycysteus-ovariumsyndroom beginnen tijdens de puberteit en nemen na verloop van tijd af. Regelmatige menstruatie gedurende enige tijd na de menarche sluit de diagnose polycysteus-ovariumsyndroom uit. Bij onderzoek wordt meestal overvloedig baarmoederhalsslijm gevonden (wat wijst op een hoge oestrogeenspiegel). De diagnose polycysteus-ovariumsyndroom kan worden vermoed als een vrouw ten minste twee typische symptomen heeft (matige obesitas, hirsutisme, onregelmatige menstruatie of amenorroe).
De meest voorkomende combinatie van klinische symptomen is:
- menstruatiecyclusstoornissen (oligomenorroe, disfunctioneel baarmoederbloeden, secundaire amenorroe);
- anovulatie;
- onvruchtbaarheid;
- hirsutisme;
- stoornis van de vetstofwisseling (obesitas en metabool syndroom);
- suikerziekte;
- obstructief slaapapneusyndroom.
Wat zit je dwars?
Diagnostics polycysteus ovariumsyndroom
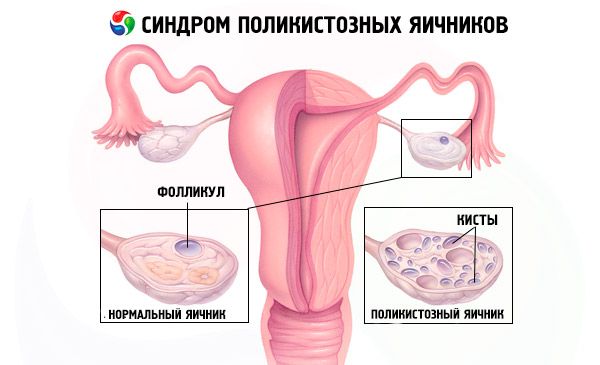
De diagnose wordt gesteld door zwangerschap uit te sluiten (zwangerschapstest) en door de concentraties oestradiol, FSH, TSH en prolactine in het bloedserum te onderzoeken. De diagnose wordt bevestigd door echografie, waarbij meer dan 10 follikels in de eierstok zichtbaar zijn; de follikels bevinden zich meestal aan de periferie en lijken op een parelsnoer. Als er follikels in de eierstokken en hirsutisme worden gevonden, moeten de testosteron- en DHEAS-waarden worden bepaald. Pathologische waarden worden beoordeeld zoals bij amenorroe.
 [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ]
[ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ]
Anamnese en lichamelijk onderzoek
Door zorgvuldige anamnese worden erfelijke factoren voor het ontstaan van polycysteus-ovariumsyndroom geïdentificeerd. Tijdens het onderzoek worden de body mass index en de taille-heupverhouding (normaal ≤ 0,8) berekend om overgewicht en obesitas te diagnosticeren.
Het polycysteus-ovariumsyndroom wordt gekenmerkt door een polymorfisme van de klinische en laboratoriumsymptomen.
Speciale diagnostische methoden voor polycysteus ovariumsyndroom
Een hormoononderzoek is verplicht op de 3e tot en met 5e dag van de menstruatieachtige reactie: de bloedwaarden van LH, FSH, prolactine, testosteron, bijnierandrogenen - DHEAS en 17-hydroxyprogesteron worden bepaald. Het polycysteus-ovariumsyndroom wordt gekenmerkt door een hoge LH/FSH-index -> 2,5-3 (als gevolg van een verhoogde LH-spiegel) en hyperandrogenisme.
Om de bron van hyperandrogenisme te achterhalen, wordt een ACTH-test uitgevoerd voor differentiële diagnostiek met hyperandrogenisme veroorzaakt door een mutatie van het gen dat codeert voor het 21-hydroxylase-enzym in de bijnieren (diagnose van latente en latente vormen van het adrenogenitaal syndroom). Techniek: om 9 uur 's ochtends wordt bloed afgenomen uit de vena cubitalis, vervolgens wordt 1 mg van het geneesmiddel synacthen-depot intramusculair toegediend en na 9 uur wordt opnieuw bloed afgenomen. De concentratie cortisol en 17-hydroxyprogesteron wordt in beide bloedmonsters bepaald, waarna met behulp van een speciale formule een coëfficiënt wordt berekend waarvan de waarden niet hoger mogen zijn dan 0,069. In deze gevallen is de test negatief en is de vrouw (of man) geen drager van de 21-hydroxylase-genmutatie.
De difeninetest wordt uitgevoerd om centrale vormen van het polycysteus-ovariumsyndroom op te sporen en de mogelijkheid van behandeling met neurotransmitters te bepalen. Testtechniek: de initiële concentratie LH en testosteron in het bloed wordt bepaald, waarna gedurende 3 dagen 3 keer per dag 1 tablet difenine wordt ingenomen. Daarna wordt de concentratie van deze hormonen opnieuw in het bloed bepaald. De test wordt als positief beschouwd als de LH- en testosteronspiegel daalt.
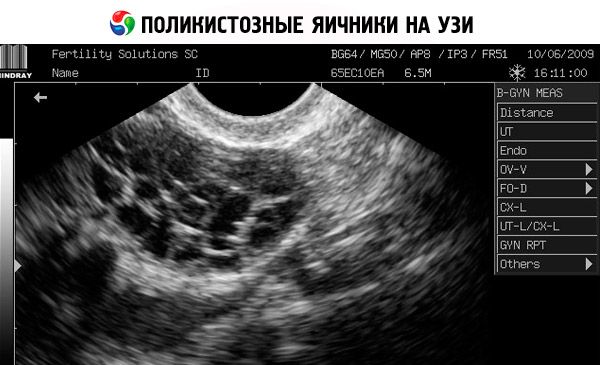
- Bij een echo van de geslachtsorganen zijn vergrote eierstokken (10 cm3 of meer) te zien, evenals meerdere follikels met een diameter tot 9 mm, een verdikking van het stroma van de eierstokken en een verdikking van het kapsel.
- Als er een vermoeden bestaat van insulineresistentie, wordt bovendien een glucosetolerantietest uitgevoerd om de insuline- en glucosespiegels voor en na het sporten te bepalen.
- Indien het vermoeden bestaat dat er sprake is van polycysteus-ovariumsyndroom aan de bijnieren, worden erfelijkheidsadvies en HLA-genotypering aanbevolen.
- Hysterosalpingografie.
- Laparoscopie.
- Evaluatie van de vruchtbaarheid van het sperma van de partner.
In november 2015 hebben de American Association of Clinical Endocrinologists (AACE), het American College of Endocrinology (ACE) en de Androgen Excess and PCOS Society (AES) nieuwe richtlijnen gepubliceerd voor de diagnose van PCOS. Deze richtlijnen zijn:
- Diagnostische criteria voor PCOS moeten een van de volgende drie criteria omvatten: chronische anovulatie, klinische hyperandrogenisme en polycysteus ovariumsyndroom.
- Naast de klinische bevindingen moeten ook de serumspiegels van 17-hydroxyprogesteron en anti-Müllerhormoon worden gemeten om PCOS te diagnosticeren.
- De hoeveelheid vrij testosteron is gevoeliger voor het detecteren van een teveel aan androgeen dan de hoeveelheid totaal testosteron.
Wat moeten we onderzoeken?
Met wie kun je contact opnemen?
Behandeling polycysteus ovariumsyndroom
Bij vrouwen met anovulatoire menstruatiecycli (een voorgeschiedenis van uitblijvende of onregelmatige menstruatie en geen bewijs van progesteronproductie), zonder hirsutisme en zonder zwangerschapswens, wordt een intermitterend progestageen (bijvoorbeeld medroxyprogesteron 5 tot 10 mg oraal eenmaal daags gedurende 10 tot 14 dagen per maand gedurende 12 maanden) of orale anticonceptiva voorgeschreven om het risico op endometriumhyperplasie en kanker te verkleinen en de circulerende androgeenspiegels te verlagen.
Bij vrouwen met polycysteus-ovariumsyndroom met anovulatoire cycli, hirsutisme en geen zwangerschapswens is de behandeling gericht op het verminderen van hirsutisme en het reguleren van de serumtestosteron- en DHEAS-spiegels. Vrouwen die zwanger willen worden, ondergaan een vruchtbaarheidsbehandeling.
De behandeling van onvruchtbaarheid bij polycysteus-ovariumsyndroom bestaat uit twee fasen:
- Fase 1 - voorbereidend;
- Fase 2 – stimulatie van de ovulatie.
De behandeling in de voorbereidende fase is afhankelijk van de klinische en pathogenetische vorm van het polycysteus-ovariumsyndroom.
- Bij polycysteus-ovariumsyndroom en obesitas wordt aangeraden om medicijnen voor te schrijven die de insulineresistentie helpen verminderen. Het voorkeursmedicijn is metformine, oraal in te nemen in een dosering van 500 mg, 3 maal daags, gedurende 3 tot 6 maanden.
- Bij de ovariële vorm van het polycysteus-ovariumsyndroom en hoge LH-spiegels worden medicijnen gebruikt die helpen de gevoeligheid van het hypothalamus-hypofyse-systeem voor volledige onderdrukking van de ovariële functie te verminderen (serumestradiolspiegel < 70 pmol/l):
- buserelinespray, 150 mcg in elk neusgat 3 keer per dag vanaf de 21e of 2e dag van de menstruatiecyclus, kuur 1–3 maanden, of
- busereline depot intramusculair 3,75 mg eenmaal per 28 dagen vanaf de 21e of 2e dag van de menstruatiecyclus, kuur 1–3 maanden, of
- leuproreline subcutaan 3,75 mg eenmaal per 28 dagen vanaf de 21e of 2e dag van de menstruatiecyclus, kuur 1–3 maanden, of
- triptoreline subcutaan 3,75 mg eenmaal per 28 dagen of 0,1 mg eenmaal per dag vanaf de 21e of 2e dag van de menstruatiecyclus, kuur 1–3 maanden.
Het maakt in principe niet uit vanaf welke dag (21e of 2e) van de menstruatiecyclus GnRH-agonisten worden voorgeschreven. Voorschrijven vanaf de 21e dag heeft echter de voorkeur, omdat in dat geval geen ovariumcysten ontstaan. Bij voorschrijven vanaf de 2e dag van de cyclus valt de activeringsfase voorafgaand aan de suppressiefase in het werkingsmechanisme van de GnRH-agonist samen met de folliculaire fase van de cyclus en kan de vorming van ovariumcysten veroorzaken.
Alternatieve medicijnen:
- ethinylestradiol/dienogest oraal 30 mcg/2 mg eenmaal daags van de 5e tot de 25e dag van de menstruatiecyclus, kuur 3–6 maanden of
- ethinylestradiol/cyproteronacetaat oraal 35 mcg/2 mg eenmaal daags van de 5e tot de 25e dag van de menstruatiecyclus, kuur 3–6 maanden.
- Bij de bijnierschorsvorm van het polycysteus-ovariumsyndroom is de toediening van glucocorticoïde geneesmiddelen geïndiceerd:
- dexamethason oraal 0,25–1 mg eenmaal daags, kuur 3–6 maanden, of
- methylprednisolon oraal 2–8 mg eenmaal daags, kuur 3–6 maanden, of
- prednisolon oraal 2,5–10 mg eenmaal daags, kuur 3–6 maanden.
- Bij de centrale vorm van polycysteus-ovariumsyndroom worden anticonvulsiva gebruikt:
- difenine 1 tablet oraal 1-2 maal per dag;
- carbamazepine oraal 100 mg 2 maal daags, kuur 3-6 maanden.
In de 2e fase wordt de ovulatie gestimuleerd.
De keuze van de medicijnen en hun toedieningsschema's worden bepaald op basis van klinische en laboratoriumgegevens. Tijdens de ovulatie-inductie worden zorgvuldige echografie en hormonale monitoring van de gestimuleerde cyclus uitgevoerd.
Het is onaanvaardbaar om de ovulatie op te wekken met medicijnen zonder echografie. Het is niet gepast om ovulatie-inductie te starten bij cysten in de eierstokken met een diameter > 15 mm en een endometriumdikte > 5 mm.
Ovulatie-inductie met clomifeen is geïndiceerd bij jonge vrouwen met een korte voorgeschiedenis van de ziekte en voldoende oestrogeenspiegels (serumestradiol < 150 pmol/l) en lage LH-spiegels (> 15 IE/l).
Clomifeen wordt oraal voorgeschreven in een dosering van 100 mg eenmaal daags vanaf de 5e tot en met de 9e dag van de menstruatiecyclus op hetzelfde tijdstip van de dag.
Op de 10e dag van de cyclus wordt een controle-echo gemaakt, waarbij de diameter van de dominante follikel en de dikte van het endometrium worden beoordeeld. Onderzoeken worden om de dag uitgevoerd, in de periovulatoire periode dagelijks. Niet de dag van de cyclus is doorslaggevend, maar de grootte van de leidende follikel: als de diameter meer dan 16 mm is, is het noodzakelijk om dagelijks een echo te maken totdat deze een grootte van 20 mm bereikt.
Alternatieve behandelingsregimes (met uitgesproken anti-oestrogene werking):
Schema 1:
- clomifeen oraal 100 mg 1 keer per dag van de 5e tot de 9e dag van de menstruatiecyclus op hetzelfde tijdstip van de dag +
- ethinylestradiol (EE) oraal 50 mcg 2 maal daags van de 10e tot de 15e dag van de menstruatiecyclus of
- estradiol oraal 2 mg 2 maal per dag van de 10e tot de 15e dag van de menstruatiecyclus.
Schema 2:
- clomifeen oraal 100 mg 1 keer per dag van de 3e tot de 7e dag van de menstruatiecyclus op hetzelfde tijdstip van de dag +
- menotropinen intramusculair 75–150 IE eenmaal daags op hetzelfde tijdstip vanaf de 7e–8e dag van de menstruatiecyclus of
- follitropine alfa intramusculair 75–150 IE eenmaal daags op hetzelfde tijdstip, te beginnen vanaf de 7e–8e dag van de menstruatiecyclus.
Ovulatie-inductie met clomifeencitraat is niet geïndiceerd in de volgende situaties:
- bij hypo-oestrogenisme (serumestradiolspiegel < 150 pmol/l);
- na voorlopige voorbereiding met GnRH-agonisten (als gevolg van verminderde gevoeligheid van het hypothalamus-hypofyse-ovariumsysteem ontwikkelt zich hypo-oestrogeenisme);
- Bij vrouwen in de vruchtbare leeftijd, met een lange voorgeschiedenis van de ziekte en hoge serum-LH-spiegels (> 15 IE/L). Het is niet wenselijk om de dosis clomifeen te verhogen tot 150 mg/dag tijdens herhaalde stimulatiekuren, aangezien het negatieve perifere anti-oestrogene effect toeneemt.
Het wordt afgeraden om meer dan 3 opeenvolgende kuren clomifeenstimulatie uit te voeren. Indien de behandeling niet effectief is, dienen gonadotrofinen te worden gebruikt.
Ovulatiestimulatie met gonadotropinen is geïndiceerd bij afwezigheid van adequate folliculogenese na stimulatie met clomifeen, bij aanwezigheid van een uitgesproken perifeer anti-oestrogeen effect en bij onvoldoende oestrogene saturatie. Het kan zowel bij jonge patiënten als in de late vruchtbare leeftijd worden toegepast.
Medicijnen van keuze:
- menotropinen intramusculair 150–225 IE eenmaal daags vanaf de 3e–5e dag van de menstruatiecyclus op hetzelfde tijdstip, kuur 7–15 dagen of
- urofollitropine intramusculair 150–225 IE eenmaal daags vanaf de 3e–5e dag van de menstruatiecyclus op hetzelfde tijdstip, kuur 7–15 dagen.
Alternatieve geneesmiddelen (bij een hoog risico op het ontwikkelen van ovarieel hyperstimulatiesyndroom):
- Follitropine alfa intramusculair, 100-150 IE eenmaal daags vanaf de 3e tot en met de 5e dag van de menstruatiecyclus, gelijktijdig toegediend, met een kuur van 7-15 dagen. Inductie van de ovulatie met gonadotropinen met behulp van GnRH-analogen is geïndiceerd bij polycysteus-ovariumsyndroom met hoge LH-waarden in het bloedserum (> 15 IE/L).
Medicijnen van keuze:
- busereline in de vorm van een spray van 150 mcg in elk neusgat 3 maal daags vanaf de 21e dag van de menstruatiecyclus of
- busereline depot intramusculair 3,75 mg eenmaal op de 21e dag van de menstruatiecyclus;
- leuproreline subcutaan 3,75 mg eenmaal op de 21e dag van de menstruatiecyclus;
- triptoreline subcutaan 3,75 mg eenmaal op de 21e dag van de menstruatiecyclus of 0,1 mg eenmaal daags vanaf de 21e dag van de menstruatiecyclus +
- menotropinen intramusculair 225–300 IE eenmaal daags vanaf de 2e–3e dag van de volgende menstruatiecyclus op hetzelfde tijdstip.
Alternatieve geneesmiddelen (bij een hoog risico op het ontwikkelen van ovarieel hyperstimulatiesyndroom):
- menotropinen intramusculair 150–225 IE eenmaal daags vanaf de 2e–3e dag van de menstruatiecyclus op hetzelfde tijdstip of
- follitropine alfa intramusculair 150–225 IE eenmaal daags vanaf de 2e–3e dag van de menstruatiecyclus op hetzelfde tijdstip +
- ganirelix subcutaan 0,25 mg eenmaal daags, te beginnen vanaf de 5e tot en met de 7e dag van het gebruik van gonadotropine (wanneer de dominante follikel een grootte van 13-14 mm bereikt);
- cetrorelix subcutaan 0,25 mg eenmaal daags, te beginnen vanaf de 5e–7e dag van het gebruik van gonadotropine (wanneer de dominante follikel een grootte van 13–14 mm bereikt).
Inductie van de ovulatie bij patiënten in de late vruchtbare leeftijd (met een zwakke ovariële respons op gonadotrope geneesmiddelen).
Medicijnen van keuze:
- menotropines intramusculair 225 IE eenmaal daags vanaf de 3e tot en met de 5e dag van de menstruatiecyclus op hetzelfde tijdstip +
- triptoreline subcutaan 0,1 mg eenmaal daags vanaf de 2e dag van de menstruatiecyclus.
Alternatieve medicijnen:
- triptoreline subcutaan 0,1 mg eenmaal daags vanaf de 2e dag van de menstruatiecyclus +
- follitropine alfa intramusculair 200–225 IE eenmaal daags vanaf de 3e tot en met de 5e dag van de menstruatiecyclus op hetzelfde tijdstip.
Bij alle schema's met gonadotrofinen wordt de adequaatheid van de dosis beoordeeld aan de hand van de dynamiek van de follikelgroei (normaal gesproken 2 mm/dag). Bij een trage groei van de follikels wordt de dosis met 75 IE verhoogd, bij een te snelle groei met 75 IE.
Bij alle behandelschema's wordt de behandeling stopgezet als er een rijpe follikel is van 18–20 mm en de dikte van het endometrium ten minste 8 mm bedraagt. Vervolgens wordt humaan choriongonadotrofine intramusculair toegediend in een eenmalige dosis van 10.000 IE.
Nadat de ovulatie is bevestigd, wordt de luteale fase van de cyclus ondersteund.
Medicijnen van keuze:
- dydrogesteron oraal 10 mg 1-3 maal daags, kuur 10-12 dagen of
- Progesteron oraal 100 mg 2-3 keer per dag, of vaginaal 100 mg 2-3 keer per dag, of intramusculair 250 mg 1 keer per dag, kuur van 10-12 dagen. Alternatief medicijn (bij afwezigheid van symptomen van ovariële hyperstimulatie):
- humaan choriongonadotrofine intramusculair 1500–2500 IE eenmaal daags op dag 3,5 en 7 van de luteale fase.
Andere medicijnen die worden gebruikt bij de behandeling van PCOS:
- Antiandrogenen (bijv. spironolacton, leuprolide, finasteride).
- Hypoglycemische medicijnen (bijv. metformine, insuline).
- Selectieve oestrogeenreceptor-modulatoren (bijv. clomifeencitraat).
- Medicijnen tegen acne (bijv. benzoylperoxide, tretinoïnecrème (0,02-0,1%)/gel (0,01-0,1%)/oplossing (0,05%), adapaleencrème (0,1%)/gel (0,1%, 0,3%)/oplossing (0,1%), erytromycine 2%, clindamycine 1%, natriumsulfetamide 10%).
Bijwerkingen van de behandeling
Bij gebruik van clomifeen ontwikkelen de meeste patiënten een perifeer anti-oestrogeen effect, dat bestaat uit een achterblijvende groei van het endometrium ten opzichte van de follikelgroei en een afname van de hoeveelheid cervixslijm. Bij gebruik van gonadotropinen, met name humaan menopauzaal gonadotropine (menotropinen), kan het ovarieel hyperstimulatiesyndroom (OHSS) ontstaan; bij gebruik van recombinant FSH (follitropine alfa) is het risico op ovarieel hyperstimulatiesyndroom lager. Bij gebruik van behandelingen met GnRH-agonisten (triptoreline, busereline, leuproreline) neemt het risico op ovarieel hyperstimulatiesyndroom toe en kan het gebruik van GnRH-agonisten symptomen van oestrogeendeficiëntie veroorzaken, zoals opvliegers, een droge huid en slijmvliezen.
Prognose
De doeltreffendheid van de behandeling van onvruchtbaarheid bij het polycysteus-ovariumsyndroom hangt af van de klinische en hormonale kenmerken van het beloop van de ziekte, de leeftijd van de vrouw, de adequaatheid van de voorbereidende therapie en de juiste keuze van het ovulatie-inductieregime.
Bij 30% van de jonge vrouwen met een korte voorgeschiedenis van de ziekte kan een zwangerschap worden bereikt na voorbereidende behandeling zonder ovulatie-inductie.
De effectiviteit van ovulatiestimulatie met clomifeen bedraagt bij vrouwen niet meer dan 30%; 40% van de patiënten met polycysteus-ovariumsyndroom zijn clomifeenresistent.
Door het gebruik van menotropinen en urofollitropine kan bij 45-50% van de vrouwen een zwangerschap worden bereikt, maar deze medicijnen verhogen het risico op het ontwikkelen van het ovarieel hyperstimulatiesyndroom.
Het meest effectief zijn de schema's met GnRH-agonisten, die "parasitaire" LH-pieken kunnen vermijden: tot 60% van de zwangerschappen per vrouw. Bij gebruik van deze medicijnen is het risico op complicaties echter het hoogst: ernstige vormen van ovarieel hyperstimulatiesyndroom, meerlingzwangerschap. Het gebruik van GnRH-antagonisten is niet minder effectief, maar gaat niet gepaard met een hoog risico op ovarieel hyperstimulatiesyndroom.
 [ 34 ]
[ 34 ]

