Medisch expert van het artikel
Nieuwe publicaties
B-cel lymfoplasmacytisch lymfoom van Waldenström
Laatst beoordeeld: 12.03.2022

Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
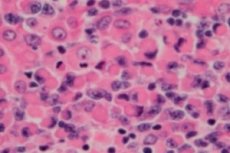
Met betrekking tot de categorie van kwaadaardige lymfoproliferatieve (immunoproliferatieve) ziekten, is lymfoplasmacytisch lymfoom of Waldenström's macroglobulinemie een cellulair neoplasma van kleine B-lymfocyten - B-cellen die beschermende functies van het lymfestelsel en humorale immuniteit van het lichaam bieden. De diagnose mag pas worden gesteld nadat alle andere kleine B-cellymfomen zijn uitgesloten. De macroglobulinemie van Waldenström werd in 1944 beschreven door Jan G. Waldenstrom, die bij twee patiënten ongebruikelijke manifestaties van lymfadenopathie, bloedarmoede, verhoogde sedimentatiesnelheid, hyperviscositeit en hypergammaglobulinemie rapporteerde. [1], [2]
Epidemiologie
Dit type lymfoom is een zeldzame, indolente hematologische maligniteit en klinische statistieken schatten de incidentie in deze groep ziekten op ongeveer 2%. Bovendien zijn er bijna twee keer zoveel mannelijke patiënten als vrouwelijke patiënten.
Volgens sommige rapporten is de frequentie van jaarlijkse gevallen van lymfoplasmacytisch lymfoom in Europa één per 102 duizend mensen en in de Verenigde Staten één per 260 duizend. [3]
Oorzaken lymfoplasmacytisch lymfoom
Tot op heden blijft de etiologie van de meeste kankers onbekend, maar het onderzoek naar de genetische basis van sommige van hen gaat door. Bij het bestuderen van de oorzaken van kwaadaardige plasmacelziekten , waaronder B-cel lymfoplasmacytisch lymfoom - Waldenström 's macroglobulinemie, hebben onderzoekers een verband gevonden tussen pathologische proliferatie (celdeling) van B - lymfocyten in een laat stadium van hun differentiatie met de aanwezigheid van bepaalde moleculaire genafwijkingen die de basale cellulaire functies veranderen.
Bij patiënten met Waldenström's macroglobulinemie werden veranderingen in sommige genen aan het licht gebracht - somatische mutaties, dat wil zeggen, die alleen weefsels aantasten met schade aan de genen van een afzonderlijke klonale celpopulatie en varianten van hun genoom vormen, die leiden tot cyclische en structurele stoornissen aan de cellulair niveau.
Allereerst zijn dit somatische mutaties van het MYD88 (L265P)-gen en CXCR4, dat codeert voor een cytosolisch eiwit dat belangrijk is voor de aangeboren en adaptieve immuunrespons: als adapter zorgt het voor signalering van de pro-inflammatoire mediator IL-1 (interleukine-1) en Toll-like cellen receptoren die de immuunrespons activeren. Als gevolg van een somatische mutatie treden anomalieën op van de polypeptideketen van een bepaald eiwitmolecuul, de structurele basis ervan. [4]
Risicofactoren
Naast algemene risicofactoren (blootstelling aan verhoogde stralingsniveaus, kankerverwekkende chemicaliën, enz.), zijn voorspellers van een verhoogde kans op het ontwikkelen van Waldenström's macroglobulinemie als een laaggradige lymfoproliferatieve ziekte:
- ouderdom (ouder dan 65 jaar);
- de aanwezigheid van familieleden met deze diagnose, evenals met B-cel non-Hodgkin-lymfoom of chronische lymfatische leukemie;
- chronische hepatitis C ;
- een voorgeschiedenis van goedaardige monoklonale gammopathie, een idiopathische hematologische ziekte, waarvan de essentie de productie is van abnormaal veranderde type M-gammaglobulinen door lymfocytische plasmocyten;
- auto- immuunziekten, in het bijzonder het syndroom van Sjögren .
Pathogenese
Bij contact met een antigeen of stimulatie van T-lymfocyten, verandert een deel van B-lymfocyten in plasmacellen - lymfocytische plasmocyten, die na bepaalde transformaties beschermende bolvormige eiwitten beginnen te produceren, dat wil zeggen gamma-globulinen (immunoglobulinen of antilichamen).
De pathogenese van lymfoplasmacytisch lymfoom/Waldenström-macroglobulinemie ligt in de hyperproliferatie van B-cellen, een overmaat van het normale niveau van een kloon van lymfocytische plasmacellen en een overmaat in het bloed van hun geproduceerde immunoglobuline M (IgM), ook wel monoklonaal immunoglobuline of M genoemd -eiwit. Het is een belangrijk pentamerisch antilichaam met hoog molecuulgewicht dat wordt geproduceerd bij de eerste aanval door specifieke bacteriële of virale antigenen. [5]
Bijna alle symptomen van deze ziekte zijn geassocieerd met manifestaties van de activiteit van het M-eiwit, dat de reologische eigenschappen van het bloed kan verstoren, de viscositeit ervan kan verhogen; impregneren van lymfoïde en myeloïde weefsels van het beenmerg, accumuleren in perifere lymfoïde weefsels (met de vorming van langzaam groeiende neoplasieën die druk kunnen uitoefenen op omliggende organen, zenuwvezels of bloedvaten).
Hoewel chronische lymfatische leukemie, Waldenström's macroglobulinemie of lymfoplasmacytisch lymfoom en multipel myeloom afzonderlijke ziekten zijn, worden ze allemaal veroorzaakt door een verhoogde proliferatie van B-lymfocyten.
Symptomen lymfoplasmacytisch lymfoom
De eerste tekenen van de ziekte zijn niet-specifiek en kunnen zich manifesteren door zwakte en vermoeidheid (als gevolg van de ontwikkeling van normochrome anemie), gewichtsverlies, kortademigheid, nachtelijke hyperhidrose en terugkerende lichte koorts.
Bovendien is er in het beginstadium van de ziekte een schending van de gevoeligheid van de handen en voeten, treedt perifere neuropathie op (gevoelloosheid of tintelingen in de voeten en benen), verschijnen er kleine focale bloedingen van de huidcapillairen (purpura), evenals koude urticaria (vanwege de vorming en aggregatie van abnormale cryoglobuline-eiwitten in serum).
Symptomen die verband houden met het hyperviscositeitssyndroom zijn hoofdpijn en duizeligheid, schade aan het netvlies en wazig zien, tinnitus en gehoorverlies, toevallen, spierpijn, hoge bloeddruk, spontane bloedneuzen en bloedend tandvlees. Bij vrouwen is baarmoederbloeding mogelijk.
Ook waargenomen: een toename van lymfeklieren (lymfadenopathie); vergroting van de milt (splenomegalie); hartfalen met cardialgie en hartritmestoornissen. Hoewel viscerale infiltratie zeldzaam is, kunnen de maag en darmen worden aangetast, wat kan leiden tot diarree (vaak met vette ontlasting). [6], [7]
Vormen
De classificatie van de Wereldgezondheidsorganisatie van 2017 van hematopoëtische en lymfoïde weefseltumoren stelt vier diagnostische criteria vast voor Waldenström-macroglobulinemie, waaronder:
- Aanwezigheid van monoklonale IgM-gammopathie
- Beenmerginfiltratie met kleine lymfocyten die plasmacytoïde of plasmaceldifferentiatie vertonen
- Beenmerginfiltratie met intertrabeculaire structuur
- Immunofenotype dat de macroglobulinemie van Waldenström ondersteunt, waaronder oppervlakte-IgM+, CD19+, CD20+, CD22+, CD25+, CD27+, FMC7+, variabele CD5, CD10-, CD23-, CD103- en CD108-
Complicaties en gevolgen
Patiënten met lymfoplasmacytisch lymfoom ontwikkelen complicaties en gevolgen in de vorm van:
- afname van de immuniteit;
- insufficiëntie van het beenmerg met een schending van zijn hematopoëtische functies en de ontwikkeling van bloedarmoede;
- deficiëntie van dergelijke gevormde bloedelementen zoals erytrocyten, leukocyten, bloedplaatjes;
- schade aan de structuren van het maagdarmkanaal met chronische diarree en verminderde intestinale absorptie (malabsorptiesyndroom);
- ontsteking van de wanden van bloedvaten (complexe immuunvasculitis);
- verhoogde botfragiliteit (osteoporose);
- visuele en auditieve beperkingen;
- secundaire amyloïdose van inwendige organen;
- progressie naar paraproteïnemische hemoblastose in de vorm van multipel myeloom;
- transformatie in een zeer kwaadaardig type lymfoom - diffuus grootcellig B-cellymfoom.
Diagnostics lymfoplasmacytisch lymfoom
De diagnose van lymfoplasmacytisch lymfoom/Waldenström's macroglobulinemie is gewoonlijk moeilijk vanwege de afwezigheid van specifieke morfologische, immunofenotypische of chromosomale veranderingen. Dit tekort maakt differentiatie van deze ziekte van andere kleine B-cellymfomen op basis van uitsluiting. [8],
Naast het beoordelen van de bestaande symptomen, zijn voor de diagnose van lymfoplasmacytisch lymfoom, algemene en biochemische bloedonderzoeken, een coagulogram, immuno- elektroforese van bloedeiwitten met de bepaling van het niveau van immunoglobuline M in het bloed noodzakelijk ; algemene urineanalyse. [9]
Een beenmergbiopsie is vereist, waarvoor de punctie wordt uitgevoerd.
Instrumentele diagnostiek wordt uitgevoerd: echografie van de lymfeklieren en milt, röntgenfoto van de botten, CT van de borst- en buikholte, oftalmoscopie.
Differentiële diagnose
Lymfoplasmacytisch lymfoom wordt beschouwd als een uitsluitingsdiagnose, daarom wordt differentiële diagnose uitgevoerd met B-cel chronische lymfatische leukemie, multipel myeloom, folliculair lymfoom, verschillende subtypes van non-Hodgkin-lymfoom, plasmacytoom, reactieve plasmacytose, angiofolliculaire lymfoïde hyperplasie (ziekte van Castleman), enzovoort.
Met wie kun je contact opnemen?
Behandeling lymfoplasmacytisch lymfoom
Houd er rekening mee dat Waldenström's macroglobulinemie of lymfoplasmacytisch lymfoom gedurende vele jaren asymptomatisch kan zijn en kan worden gediagnosticeerd met een verhoging van het M-eiwit in het bloed.
Als er geen symptoom is, wordt actief gecontroleerd met regelmatige onderzoeken en tests.
Op basis van de bestaande symptomen en de resultaten van laboratoriumtesten wordt besloten om de therapie te starten, wat van veel factoren afhankelijk is (bijvoorbeeld leeftijd, progressie van de ziekte, etc.).
Volgens het protocol is de initiële behandeling van patiënten met dit type lymfoom meestal een combinatie van bestralingstherapie en chemotherapie met de introductie van cytostatica, bijvoorbeeld Cyclofosfamide , Doxorubicine, Vincristine, evenals corticosteroïden - Metprednisolon of Dexamethason (Dexason).
De effectiviteit van chemotherapiemedicijnen van de groep van monoklonale antilichamen, in het bijzonder rituximab, is bewezen . [10]
In gevallen van gegeneraliseerde ziekte wordt rituximab gebruikt in combinatie met antitumor-nucleoside-analogen (pentostatine, cladribine). Bij een langzaam progressieve ziekte met een laag monoklonaal immunoglobuline M wordt naast rituximab het cytostatische chloorambucil (Leukeran) gebruikt. [11]
Om de viscositeit van het bloed te verminderen en het niveau van de gevormde elementen te stabiliseren, wordt therapeutische hemaferese gebruikt .
Bij een kritisch laag gehalte aan antilichamen in het bloed - om gelijktijdige herinfecties te voorkomen - wordt een immunoglobuline-vervangingstherapie uitgevoerd.
Volgens oncohematologen ervaren de meeste patiënten een terugval, ondanks het feit dat behandeling kan leiden tot remissie van de ziekte. Als het eerder dan 24 maanden optreedt, kan een geneesmiddel tegen kanker zoals Ibrutinib (in tabletvorm) worden gebruikt. Bij latere recidieven wordt de behandeling uitgevoerd volgens het oorspronkelijke schema. [12]. [13]_ [14]
Het voorkomen
Specialisten bepalen de prognose van de uitkomst van lymfoplasmacytisch lymfoom volgens het internationale prognostische systeem voor het beoordelen van de belangrijkste parameters: de leeftijd van de patiënt en serumspiegels van hemoglobine, bloedplaatjes, bèta-2-microglobuline en monoklonaal immunoglobuline. [15], [16]
De gemiddelde overlevingskans voor deze diagnose is ongeveer vijf jaar, maar bijna 40% van de patiënten leeft tien jaar of langer.

